
Struktura trzeciorzędowych alkoholi, właściwości, przykłady
ZA alkohol trzeciorzędowy to taki, w którym grupa hydroksylowa, OH, jest przyłączona do trzeciorzędowego węgla. Jego formuła nadal jest ROH, podobnie jak inne alkohole; ale jest łatwo rozpoznawalny, ponieważ OH jest blisko X w strukturze molekularnej. Podobnie jego łańcuch węglowy jest zwykle krótszy, a jego masa cząsteczkowa jest wyższa..
Tak więc trzeciorzędowy alkohol jest cięższy, jest bardziej rozgałęziony, a także jest najmniej reaktywny pod względem utleniania ze wszystkich; to znaczy, nie można go przekształcić w keton lub kwas karboksylowy, jak ma to miejsce odpowiednio w przypadku alkoholi drugorzędowych i pierwszorzędowych..
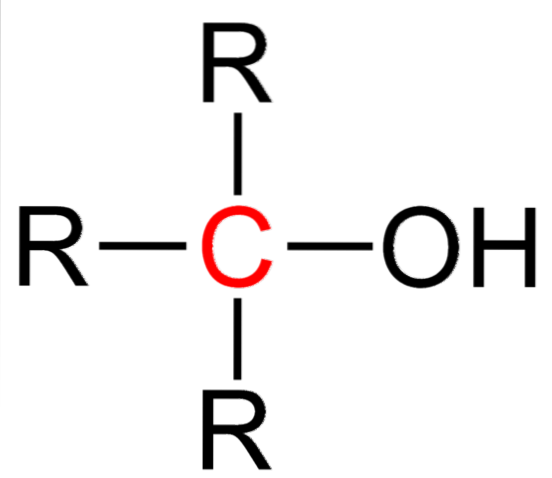
Powyższy obrazek przedstawia ogólny wzór strukturalny trzeciorzędowego alkoholu. Zgodnie z nią można by napisać nową formułę typu R.3COH, gdzie R może oznaczać grupę alkilową lub arylową; grupa metylowa, CH3, albo krótki lub długi łańcuch węglowy.
Jeśli trzy grupy R są różne, centralny atom węgla trzeciorzędowego alkoholu będzie chiralny; to znaczy, alkohol będzie wykazywał aktywność optyczną. Z tego powodu chiralne trzeciorzędowe alkohole są przedmiotem zainteresowania w przemyśle farmaceutycznym, ponieważ te alkohole o bardziej złożonej strukturze są syntetyzowane z ketonów o aktywności biologicznej..
Indeks artykułów
- 1 Struktura trzeciorzędowego alkoholu
- 1.1 Przeszkoda steryczna
- 2 Właściwości
- 2.1 Fizyczne
- 2.2 Kwasowość
- 2.3 Reaktywność
- 3 Nazewnictwo
- 4 Przykłady
- 5 Referencje
Struktura trzeciorzędowego alkoholu
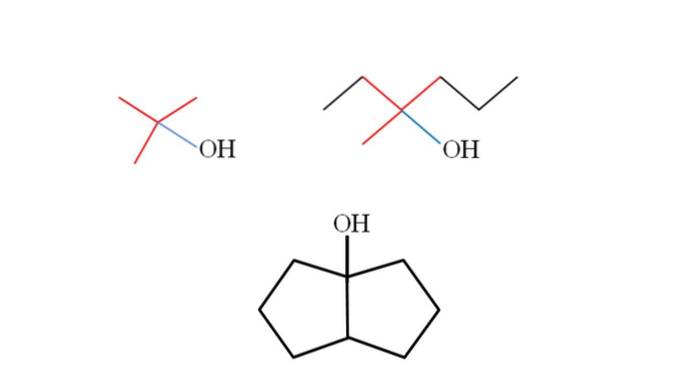
Rozważ struktury wyższych alkoholi trzeciorzędowych, aby nauczyć się je rozpoznawać bez względu na to, jaki jest związek. Węgiel związany z OH musi być również połączony z trzema innymi atomami węgla. Jeśli przyjrzysz się uważnie, osiągną to wszystkie trzy alkohole..
Pierwszy alkohol (po lewej) składa się z trzech grup CH3 związany z centralnym węglem, którego wzór byłby (CH3)3COH. Grupa alkilowa (CH3)3C- jest znany jako tertbutyl, jest obecny w wielu trzeciorzędowych alkoholach i można go łatwo rozpoznać po kształcie litery T (czerwone T na zdjęciu).
Drugi alkohol (po prawej) ma grupy CH przyłączone do centralnego węgla3, CH3CHdwa i CHdwaCHdwaCH3. Ponieważ te trzy grupy są różne, alkohol jest chiralny i dlatego wykazuje aktywność optyczną. Tutaj nie obserwuje się T, ale X blisko OH (czerwony i niebieski).
A w trzecim alkoholu (tym poniżej i bez kolorów) OH jest połączony z jednym z dwóch atomów węgla, które łączą dwa cyklopentany. Ten alkohol nie ma aktywności optycznej, ponieważ dwie z grup przyłączonych do centralnego węgla są identyczne. Podobnie jak w przypadku drugiego alkoholu, jeśli przyjrzysz się uważnie, znajdziesz również X (raczej czworościan).
Przeszkoda przestrzenna
Trzy wyższe alkohole mają coś więcej wspólnego niż X: centralny węgiel jest zawadzony przestrzennie; to znaczy, że jest wiele atomów otaczających go w przestrzeni. Bezpośrednią tego konsekwencją jest to, że nukleofile żądni ładunków dodatnich mają trudności z zbliżeniem się do tego węgla..
Z drugiej strony, ponieważ istnieją trzy atomy węgla związane z centralnym węglem, przekazują one część gęstości elektronów, którą odejmuje od niej elektroujemny atom tlenu, dodatkowo stabilizując go przed atakami nukleofilowymi. Jednak trzeciorzędowy alkohol może ulec podstawieniu poprzez utworzenie karbokokacji.
Nieruchomości
Fizyczny
Trzecie alkohole mają na ogół silnie rozgałęzione struktury. Pierwszą tego konsekwencją jest to, że grupa OH jest utrudniona, a zatem jej moment dipolowy ma mniejszy wpływ na sąsiednie cząsteczki..
Skutkuje to słabszymi oddziaływaniami molekularnymi w porównaniu z alkoholami pierwszorzędowymi i drugorzędowymi..
Na przykład rozważmy izomery strukturalne butanolu:
CH3CHdwaCHdwaOH (n-butanol, Peb = 117 ° C)
(CH3)dwaCHdwaOH (alkohol izobutylowy, temperatura wrzenia = 107 ° C)
CH3CHdwaCH (OH) CH3 (alkohol sec-butylowy, temperatura wrzenia = 98 ° C)
(CH3)3COH (alkohol tert-butylowy, bp = 82ºC)
Zwróć uwagę, jak spada temperatura wrzenia, gdy izomer staje się bardziej rozgałęziony.
Na początku wspomniano, że w strukturach III alkoholi obserwuje się X, co samo w sobie wskazuje na silne rozgałęzienie. Dlatego te alkohole mają zwykle niższe temperatury topnienia i / lub wrzenia..
Nieco podobnie jest w przypadku jego mieszalności z wodą. Im bardziej utrudniony jest OH, tym mniej mieszalny będzie trzeci alkohol z wodą. Jednak wymieniona mieszalność zmniejsza się, im dłuższy jest łańcuch węglowy; W takim przypadku trzeciorzędowy alkohol butylowy jest lepiej rozpuszczalny i mieszalny z wodą niż n-butanol.
Kwasowość
Alkohole trzeciorzędowe wydają się być najmniej kwaśne ze wszystkich. Powody są liczne i powiązane. Krótko mówiąc, ujemny ładunek jego pochodnego alkoholanu, RO-, będzie odczuwać silny odpychanie dla trzech grup alkilowych przyłączonych do centralnego węgla, osłabiając anion.
Im bardziej niestabilny anion, tym niższa kwasowość alkoholu.
Reaktywność
Trzecie alkohole nie mogą ulec utlenieniu do ketonów (R.dwaC = O) lub aldehydy (RCHO) lub kwasy karboksylowe (RCOOH). Po pierwsze, musiałbyś stracić jeden lub dwa węgle (w postaci COdwa) utleniać się, co zmniejsza jego reaktywność wobec utleniania; z drugiej strony brakuje mu wodoru, który mógłby utracić, tworząc inne wiązanie z tlenem.
Jednak mogą ulegać substytucji i eliminacji (tworzenie podwójnego wiązania, alkenu lub olefiny).
Nomenklatura
Nazewnictwo tych alkoholi nie różni się od pozostałych. Istnieją nazwy pospolite lub tradycyjne, a także nazwy systematyczne podlegające IUPAC.
Jeśli główny łańcuch i jego rozgałęzienia składają się z uznanej grupy alkilowej, używa się jej jako tradycyjnej nazwy; gdy nie jest to możliwe, stosuje się nomenklaturę IUPAC.
Weźmy na przykład pod uwagę następujący trzeciorzędowy alkohol:
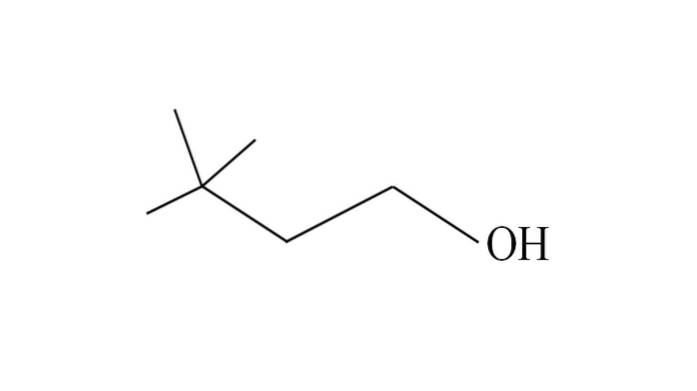
Węgle zaczynają być numerowane od prawej do lewej. W C-3 są dwie grupy CH3 podstawników, stąd nazwa tego alkoholu to 3,3-dimetylo-1-butanol (łańcuch główny ma cztery atomy węgla).
Podobnie cały łańcuch i jego odgałęzienia składają się z grupy neoheksylowej; dlatego jego tradycyjną nazwą może być alkohol neoheksylowy lub neoheksanol.
Przykłady
Na koniec wymieniono kilka przykładów trzeciorzędowych alkoholi:
-2-metylo-2-propanol
-3-metylo-3-heksanol
-Bicyklo [3.3.0] oktan-1-ol
-2-metylo-2-butanol: CH3CHdwaCOH (CH3)dwa
Na pierwszym obrazku przedstawiono formuły trzech pierwszych alkoholi.
Bibliografia
- Carey F. (2008). Chemia organiczna. (Wydanie szóste). Mc Graw Hill.
- Morrison, R. T. and Boyd, R, N. (1987). Chemia organiczna. (Wydanie 5). Od redakcji Addison-Wesley Interamericana.
- Graham Solomons T.W., Craig B. Fryhle. (2011). Chemia organiczna. Aminy. (Wydanie 10.). Wiley plus.
- Gunawardena Gamini. (31 stycznia 2016). Alkohol trzeciorzędowy. Chemia LibreTexts. Źródło: chem.libretexts.org
- Ashenhurst James. (16 czerwca 2010). Alkohole (1) - Nazewnictwo i właściwości. Odzyskane z: masterorganicchemistry.com
- Clark J. (2015). Przedstawiamy alkohole. Źródło: chemguide.co.uk
- Chemia organiczna. (s.f.). Część 3. Alkohole. [PDF]. Odzyskany z: sinorg.uji.es
- Nilanjana Majumdar. (03 marca 2019). Synteza chiralnego trzeciorzędowego alkoholu: znaczące zmiany. Odzyskane z: 2.chemistry.msu.edu


Jeszcze bez komentarzy