
Budowa grupy acylowej, charakterystyka, związki i pochodne
Plik grupa acylowa Jest to fragment molekularny, który w chemii organicznej zwykle pochodzi z kwasów karboksylowych. Jego wzór to RCO, gdzie R to podstawnik węglowy, alkilowy lub arylowy, kowalencyjnie i bezpośrednio połączony z grupą karbonylową, C = O. Zwykle jest to tylko ułamek struktury związku organicznego, takiego jak biocząsteczka..
Mówi się, że pochodzi od kwasu karboksylowego RCOOH, ponieważ wystarczy usunąć grupę hydroksylową OH, aby otrzymać grupę acylową RCO. Należy zauważyć, że ta grupa obejmuje szeroką rodzinę związków organicznych (i nieorganicznych). Ta rodzina jest ogólnie znana jako związki acylowe (a nie azyl).

Na górnym obrazku mamy wzór strukturalny grupy acylowej. Łatwo go rozpoznać, obserwując dowolną strukturę molekularną, ponieważ zawsze znajduje się na końcach i jest wskazywany przez grupę karbonylową. Przykład tego zobaczymy w cząsteczce acetylo-CoA, niezbędnej dla cyklu Krebsa.
Włączenie tej grupy do cząsteczki jest znane jako reakcja acylowania. Grupa acylowa jest częścią rutynowej pracy w syntezach organicznych.
Indeks artykułów
- 1 Struktura i charakterystyka grupy acylowej
- 2 Związki i pochodne
- 2.1 - Chlorki
- 2.2 - Radykalne
- 2.3 - Kationy
- 2.4 - Amidy
- 2,5 - Aldehydy
- 2.6 - Ketony i estry
- 2.7 - Komentarz ogólny
- 3 Przykłady grupy acylowej
- 4 Odnośniki
Struktura i charakterystyka grupy acylowej
Struktura grupy acylowej zależy od tożsamości R. Atom węgla wspomnianego łańcucha bocznego R, jak również C = O, do którego jest przyłączony, znajdują się w tej samej płaszczyźnie. Segment RCO pierwszego obrazu jest zatem płaski.
Jednak fakt ten mógłby wydawać się nieistotny, gdyby nie charakterystyka elektronowa C = O: atom węgla ma niewielki deficyt elektronów. To sprawia, że jest podatny na atak czynników nukleofilowych bogatych w elektrony. Zatem grupa acylowa jest reaktywna, będąc specyficznym miejscem, w którym przeprowadzane są syntezy organiczne..
Związki i pochodne
W zależności od łańcuchów R lub atomów, które są umieszczone po prawej stronie RCO, otrzymuje się różne związki lub pochodne grupy acylowej.
- Chlorki
Załóżmy na przykład, że atom chloru jest umieszczony na prawo od RCO. To teraz zastępuje falistość przedstawioną na pierwszym obrazie, pozostając jako: RCOCl. Mamy wtedy kilka pochodnych zwanych chlorkami acylowymi.
Teraz, zmieniając tożsamość R w RCOCl, otrzymujemy kilka chlorków acylu:
-HCOCl, R = H, chlorek metanoilu, związek drastycznie niestabilny
-CH3COCl, R = CH3, chlorek acetylu
-CH3CHdwaCOCl, R = CHdwaCH3, chlorek propionylu
-do6H.5COCl, R = C6H.5 (pierścień benzenowy), chlorek benzoilu
To samo dotyczy fluorków, bromków i jodków acylu. Związki te są używane w reakcjach acylowania, w celu włączenia RCO jako podstawnika do większej cząsteczki; na przykład do pierścienia benzenowego.
- Rodnik
Acyl może istnieć przez chwilę jako rodnik RCO •, pochodzący z aldehydu. Gatunek ten jest bardzo niestabilny i jest natychmiastowo nieproporcjonalny do rodnika alkilowego i tlenku węgla:
RC • = O → R • + C≡O
- Kation
Grupa acylowa może również występować jako kation, RCO+, będąc związkiem pośrednim, który reaguje w celu acylowania cząsteczki. Gatunek ten zawiera dwie struktury rezonansowe przedstawione na poniższym obrazku:
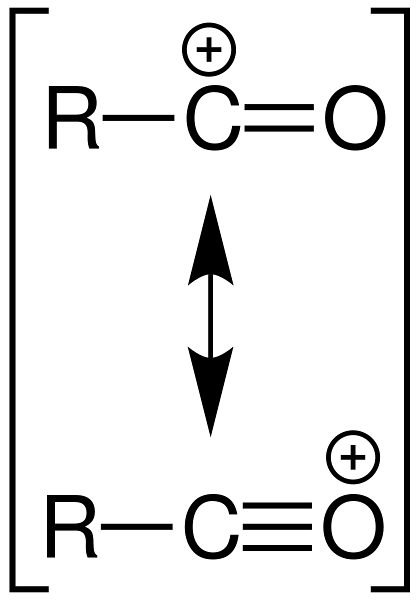
Zwróć uwagę, jak dodatni ładunek cząstkowy rozkłada się między atomami węgla i tlenu. Spośród tych dwóch struktur [R-C≡O+], z dodatnim ładunkiem tlenu, dominuje.
- Amidy
Teraz przypuśćmy, że zamiast atomu Cl umieścimy grupę aminową NHdwa. Będziemy wtedy mieli amid, RCONHdwa, RC (O) NHdwa lub RC = ONHdwa. W ten sposób ostatecznie zmieniając tożsamość R, otrzymamy rodzinę amidów.
- Aldehydy
Jeśli zamiast NHdwa umieścimy atom wodoru, otrzymamy aldehyd, RCOH lub RCHO. Zauważ, że grupa acylowa jest nadal obecna, nawet jeśli przeszła na drugi plan. Zarówno aldehydy, jak i amidy są związkami acylowymi.
- Ketony i estry
Kontynuując to samo rozumowanie, możemy zastąpić H innym łańcuchem bocznym R, co spowoduje powstanie ketonu, RCOR 'lub RC (O) R'. Tym razem grupa acylowa jest bardziej „ukryta”, ponieważ każdy z dwóch końców można uznać za RCO lub R'CO.
Z drugiej strony R 'można również zastąpić OR', dając początek estru RCOOR '. W estrach grupa acylowa jest rozpoznawana gołym okiem, ponieważ znajduje się po lewej stronie grupy karbonylowej.
- Ogólny komentarz
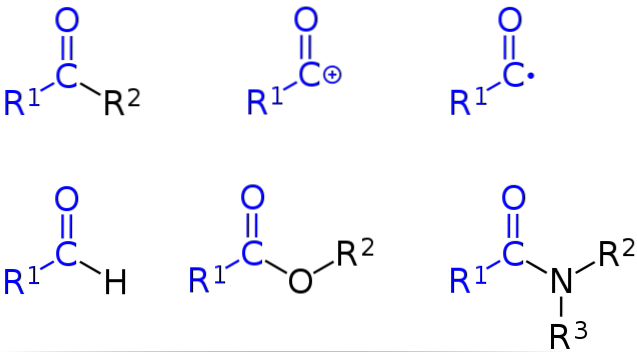
Górny obraz globalnie przedstawia wszystko, co zostało omówione w tej sekcji. Grupa acylowa jest zaznaczona na niebiesko i zaczynając od górnego rogu od lewej do prawej mamy: ketony, kation acylowy, rodnik acylowy, aldehyd, estry i amidy.
Chociaż grupa acylowa jest obecna w tych związkach, a także w kwasach karboksylowych i tioestrach (RCO-SR '), grupie karbonylowej przypisuje się zwykle większe znaczenie przy definiowaniu jej momentów dipolowych. RCO budzi większe zainteresowanie, gdy występuje jako podstawnik lub gdy jest bezpośrednio połączony z metalem (acylami metali).
W zależności od związku, RCO może mieć różne nazwy, jak widać w podsekcji dotyczącej chlorków acylu. Na przykład CH3CO jest znany jako acetyl lub etanoil, podczas gdy CH3CHdwaCO, propionyl lub propanoil.
Przykłady grup acylowych

Jednym z najbardziej reprezentatywnych przykładów związków acylowych jest acetylo-CoA (górne zdjęcie). Zwróć uwagę, że jest on natychmiast identyfikowany, ponieważ jest podświetlony na niebiesko. Grupa acylowa acetylo-CoA, jak sama nazwa wskazuje, to acetyl, CH3WSPÓŁ. Chociaż może się na to nie wydawać, ta grupa jest niezbędna w cyklu Krebsa naszego ciała.
Aminokwasy również zawierają grupę acylową, ale ponownie, zwykle pozostaje ona niezauważona. Na przykład dla glicyny NHdwa-CHdwa-COOH, jego grupa acylowa staje się segmentem NHdwa-CHdwa-CO i nazywa się glicylem. Tymczasem dla lizyny jej grupa acylowa staje się NHdwa(CHdwa)4CHNHdwaCO, który jest nazywany lizylem.
Chociaż zwykle nie jest to omawiane bardzo regularnie, grupy acylowe mogą również pochodzić z kwasów nieorganicznych; to znaczy, centralny atom nie musi być węglem, ale może również składać się z innych pierwiastków. Na przykład grupą acylową może być również RSO (RS = O), pochodząca z kwasu sulfonowego lub RPO (RP = O), pochodząca z kwasu fosfonowego..
Bibliografia
- Morrison, R. T. i Boyd, R, N. (1987). Chemia organiczna. Wydanie 5. Od redakcji Addison-Wesley Interamericana.
- Carey F. (2008). Chemia organiczna. (Wydanie szóste). Mc Graw Hill.
- Graham Solomons T.W., Craig B. Fryhle. (2011). Chemia organiczna. (Wydanie 10.). Wiley plus.
- Wikipedia. (2020). Grupa acylowa. Odzyskane z: en.wikipedia.org
- Helmenstine, dr Anne Marie (11 lutego 2020). Definicja i przykłady grupy acylowej. Odzyskany z: thinkco.com
- Laura Foist. (2020). Grupa acylowa: definicja i struktura. Nauka. Odzyskany z: study.com
- Steven A. Hardinger. (2017). Ilustrowany słownik chemii organicznej: grupa acylowa. Odzyskany z: chem.ucla.edu



Jeszcze bez komentarzy