
Formuły maszynowe Carnota, jak to działa i zastosowania

Plik maszyna Carnot jest to idealny model cykliczny, w którym ciepło jest wykorzystywane do pracy. System można rozumieć jako tłok poruszający się wewnątrz cylindra sprężającego gaz. Ćwiczony cykl to cykl Carnota, ogłoszony przez ojca termodynamiki, francuskiego fizyka i inżyniera Nicolasa Léonarda Sadi Carnota..
Carnot ogłosił ten cykl na początku XIX wieku. Maszyna jest poddawana czterem zmianom stanu, naprzemiennym warunkom, takim jak temperatura i stałe ciśnienie, w których zmiana objętości jest wykazana podczas sprężania i rozprężania gazu.
Indeks artykułów
- 1 Formuły
- 1.1 Rozszerzalność izotermiczna (A → B)
- 1.2 Rozszerzalność adiabatyczna (B → C)
- 1.3 Kompresja izotermiczna (C → D)
- 1.4 Kompresja adiabatyczna (D → A)
- 2 Jak działa maszyna Carnot?
- 3 Aplikacje
- 4 Odnośniki
Formuły
Według Carnota, poddając idealną maszynę zmianom temperatury i ciśnienia, można zmaksymalizować uzyskiwaną wydajność.
Cykl Carnota należy analizować oddzielnie w każdej z jego czterech faz: rozprężania izotermicznego, rozszerzania adiabatycznego, ściskania izotermicznego i ściskania adiabatycznego..
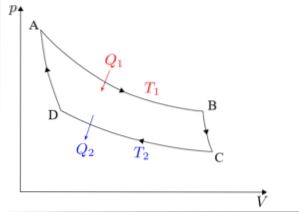
Formuły związane z każdą z faz cyklu przeprowadzonego w maszynie Carnota zostaną szczegółowo opisane poniżej..
Rozszerzalność izotermiczna (A → B)
Założenia tej fazy są następujące:
- Objętość gazu: przechodzi od minimalnej do średniej objętości.
- Temperatura maszyny: stała temperatura T1, wysoka wartość (T1> T2).
- Ciśnienie w maszynie: spada z P1 do P2.
Proces izotermiczny oznacza, że temperatura T1 nie zmienia się w tej fazie. Przenikanie ciepła indukuje rozszerzanie się gazu, co wywołuje ruch na tłoku i powoduje pracę mechaniczną.
Gdy gaz rozszerza się, ma tendencję do ochładzania się. Jednak pochłania ciepło wyemitowane przez źródło temperatury i podczas jego rozprężania utrzymuje stałą temperaturę..
Ponieważ podczas tego procesu temperatura pozostaje stała, energia wewnętrzna gazu nie zmienia się, a całe pochłonięte przez gaz ciepło jest skutecznie przekształcane w pracę. A) Tak:
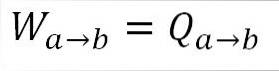
Ze swojej strony na końcu tej fazy cyklu możliwe jest również uzyskanie wartości ciśnienia za pomocą równania gazu doskonałego. Tak więc mamy:
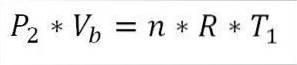
W tym wyrażeniu:
P.dwa: Ciśnienie na końcu fazy.
Vb: Objętość w punkcie b.
n: Liczba moli gazu.
O: Uniwersalna stała gazów doskonałych. R = 0,082 (atm * litr) / (mole * K).
T1: Początkowa temperatura bezwzględna, stopnie Kelvina.
Ekspansja adiabatyczna (B → C)
W tej fazie procesu ekspansja gazu odbywa się bez konieczności wymiany ciepła. W związku z tym przesłanki są szczegółowo opisane poniżej:
- Objętość gazu: przechodzi od średniej do maksymalnej objętości.
- Temperatura maszyny: spada z T1 do T2.
- Ciśnienie maszyny: stałe ciśnienie P2.
Proces adiabatyczny oznacza, że ciśnienie P2 nie zmienia się podczas tej fazy. Temperatura spada, a gaz nadal się rozszerza, aż osiągnie swoją maksymalną objętość; to znaczy, tłok osiąga opór.
W tym przypadku wykonana praca pochodzi z energii wewnętrznej gazu i jej wartość jest ujemna, ponieważ energia zmniejsza się w trakcie tego procesu..
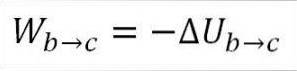
Zakładając, że jest to gaz doskonały, teoria głosi, że cząsteczki gazu mają tylko energię kinetyczną. Zgodnie z zasadami termodynamiki można to wywnioskować z następującego wzoru:
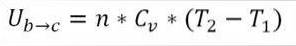
W tym wzorze:
∆Ub → c: Zmiana energii wewnętrznej gazu doskonałego między punktami b i c.
n: Liczba moli gazu.
Cv: Molowa pojemność cieplna gazu.
T1: Początkowa temperatura bezwzględna, stopnie Kelvina.
T2: Absolutna temperatura końcowa, stopnie Kelvina.
Kompresja izotermiczna (C → D)
W tej fazie rozpoczyna się sprężanie gazu; to znaczy tłok przesuwa się do cylindra, za pomocą którego gaz zmniejsza swoją objętość.
Warunki właściwe dla tej fazy procesu opisano szczegółowo poniżej:
- Objętość gazu: przechodzi od maksymalnej do pośredniej objętości.
- Temperatura maszyny: stała temperatura T2, wartość zredukowana (T2 < T1).
- Ciśnienie maszyny: wzrasta z P2 do P1.
Tutaj ciśnienie na gaz rośnie, więc zaczyna się kompresować. Jednak temperatura pozostaje stała, a zatem wahania energii wewnętrznej gazu są zerowe.
Analogicznie do rozszerzania izotermicznego, wykonana praca jest równa ciepłu systemu. A) Tak:
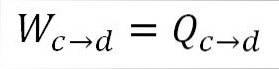
Możliwe jest również wyznaczenie ciśnienia w tym punkcie za pomocą równania gazu doskonałego.
Kompresja adiabatyczna (D → A)
Jest to ostatnia faza procesu, w której system powraca do swoich warunków początkowych. W tym celu brane są pod uwagę następujące warunki:
- Objętość gazu: przechodzi od objętości pośredniej do objętości minimalnej.
- Temperatura maszyny: rośnie od T2 do T1.
- Ciśnienie maszyny: ciśnienie stałe P1.
Źródło ciepła włączone do systemu w poprzedniej fazie jest usuwane, aby gaz idealny podnosił swoją temperaturę, o ile ciśnienie pozostaje stałe..
Gaz powraca do początkowych warunków temperaturowych (T1) i do swojej objętości (minimum). Po raz kolejny wykonana praca pochodzi z wewnętrznej energii gazu, więc musisz:
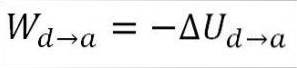
Podobnie jak w przypadku ekspansji adiabatycznej, możliwe jest uzyskanie zmiany energii gazu za pomocą następującego wyrażenia matematycznego:
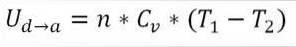
Jak działa maszyna Carnot?
Silnik Carnota pracuje jako silnik, w którym osiągi są maksymalizowane przez różne procesy izotermiczne i adiabatyczne, naprzemiennie fazy rozprężania i sprężania idealnego gazu..
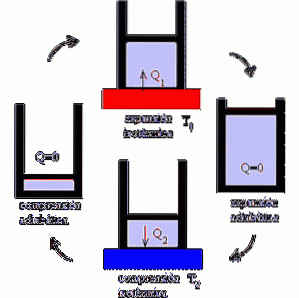
Mechanizm można rozumieć jako idealne urządzenie, które wykonuje pracę poddawaną zmianom ciepła, biorąc pod uwagę istnienie dwóch źródeł temperatury.
W pierwszej kolejności system jest wystawiony na działanie temperatury T1. Jest to wysoka temperatura, która obciąża system i powoduje rozszerzanie się gazu..
To z kolei przekłada się na wykonanie pracy mechanicznej, która pozwala na mobilizację tłoka poza cylinder, a której zatrzymanie jest możliwe tylko poprzez ekspansję adiabatyczną..
Następnie pojawia się drugie ognisko, w którym układ jest wystawiony na działanie temperatury T2, niższej niż T1; to znaczy mechanizm poddawany jest chłodzeniu.
Powoduje to pobieranie ciepła i kruszenie gazu, który po sprężeniu adiabatycznym osiąga swoją początkową objętość..
Aplikacje
Maszyna Carnota znalazła szerokie zastosowanie dzięki swojemu wkładowi w zrozumienie najważniejszych aspektów termodynamiki.
Model ten pozwala na jasne zrozumienie zmian idealnych gazów podlegających zmianom temperatury i ciśnienia, co czyni go metodą referencyjną podczas projektowania rzeczywistych silników..
Bibliografia
- Cykl silnika Carnot Heat i II zasada (patrz dalej). Odzyskany z: nptel.ac.in
- Castellano, G. (2018). Maszyna Carnota. Odzyskany z: famaf.unc.edu.ar
- Cykl Carnota (s.f.) Ecured. Hawana Kuba. Odzyskany z: ecured.cu
- Cykl Carnota (s.f.). Odzyskany z: sc.ehu.es
- Fowler, M. (s.f.). Silniki cieplne: cykl Carnota. Odzyskany z: galileo.phys.virginia.edu
- Wikipedia, wolna encyklopedia (2016). Maszyna Carnota. Odzyskane z: es.wikipedia.org



Jeszcze bez komentarzy