
Charakterystyka, zastosowania i toksyczność p-nitrofenolu
Plik p-nitrofenol lub 4-nitrofenol jest organicznym związkiem fenolowym, ponieważ ma pierścień benzenowy przyłączony do grupy hydroksylowej. Litera „p” oznacza „dla” i wskazuje, że jego rodniki znajdują się w pozycji 1 i 4 pierścienia benzenowego.
Obecne grupy to hydroksyl w pozycji 1 i grupa nitrowa w pozycji 4. Wzór chemiczny p-nitrofenolu to C6H.5NIE3. P-nitrofenol jest bezbarwnym wskaźnikiem pH przy pH poniżej 5,4 i żółtym powyżej 7,5.
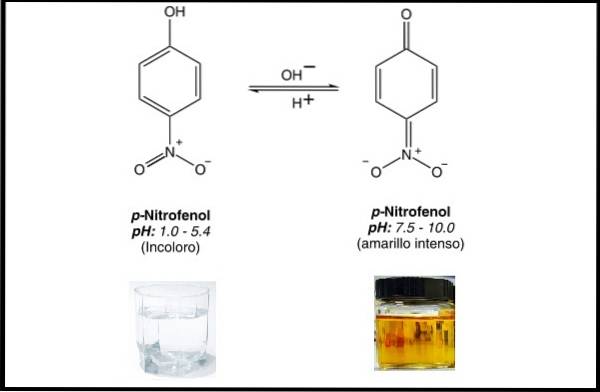
Z drugiej strony związek ten służy do syntezy różnych ważnych dla zdrowia substancji, takich jak paracetamol (znany również jako acetaminofen), który jest uznanym środkiem przeciwbólowym i przeciwgorączkowym..
Służy również jako prekursor do syntezy fenetydyny, która działa przeciwdrgawkowo, oraz acetofenetydyny, która służy jako środek przeciwbólowy. Inne substancje, które można uzyskać z p-nitrofenolu, to różne surowce niezbędne do produkcji niektórych fungicydów i pestycydów..
Poza tym jest również surowcem do produkcji barwników, służących do przyciemniania skór..
Jednak pomimo swoich zalet p-nitrofenol jest substancją, z którą należy obchodzić się bardzo ostrożnie, gdyż stwarza duże zagrożenie dla zdrowia. Ma niewielką palność i umiarkowaną reaktywność, zgodnie ze wskazaniami NFPA (National Fire Protection Association).
Indeks artykułów
- 1 Funkcje
- 2 Zastosowania
- 2.1 Wskaźnik pH
- 2.2 Prekursor w syntezie związków
- 2.3 Tworzenie p-nitrofenolu w wyniku działania niektórych enzymów na określone substraty
- 3 Toksyczność
- 3.1 Skutki zdrowotne
- 3.2 Pierwsza pomoc
- 3.3 Środki bezpieczeństwa biologicznego
- 4 Odnośniki
Charakterystyka
P-nitrofenol jest syntetyczną substancją chemiczną, co oznacza, że nie jest wytwarzany z naturalnych źródeł.
Charakteryzuje się żółtawo-białym lub jasnożółtym krystalicznym proszkiem. P-nitrofenol ma masę cząsteczkową 139,11 g / mol, temperaturę wrzenia 279 ° C, temperaturę topnienia 110-115 ° C i temperaturę samozapłonu 268 ° C. Ta substancja nie paruje w temperaturze pokojowej.
Rozpuszczalność w wodzie w temperaturze pokojowej wynosi 16 g / l. Jest rozpuszczalny w etanolu, chloroformie i eterze dietylowym.
P-nitrofenol jest związkiem złożonym, ponieważ jego stan stały (kryształy) składa się z mieszaniny dwóch form molekularnych: jednej zwanej alfa, a drugiej beta.
W formie alfa (4-nitrofenol) jest bezbarwny, wykazuje niestabilność w temperaturze pokojowej i nie wykazuje zmian w świetle słonecznym (stabilny).
Podczas gdy forma beta (4-nitrofenolan lub fenoksyd) pojawia się jako żółte kryształy i zachowuje się odwrotnie; to znaczy, że jest stabilny w temperaturze pokojowej, ale pod wpływem światła słonecznego stopniowo zmienia kolor na czerwony..
Substancja ta ma swój punkt izosbesowy przy 348 nm dla form alfa i beta.
Aplikacje
Wskaźnik PH
Chociaż związek ten pełni funkcję wskaźnika pH, nie jest szeroko stosowany w tym celu. W odniesieniu do zmian koloru w zależności od pH wykazuje duże podobieństwo do innych wskaźników pH, takich jak tymoftaleina i fenoloftaleina. Łączy je to, że są bezbarwne przy niskim pH.
Prekursor w syntezie związków
P-nitrofenol to związek stosowany w przemyśle farmaceutycznym do syntezy substancji o korzystnym wpływie na zdrowie..
Na przykład acetaminofen lub paracetamol można zsyntetyzować z p-nitrofenolu, który jest jednym z leków o działaniu przeciwbólowym i przeciwgorączkowym najczęściej stosowanym w społeczności..
Pochodzi z niej również fenetydyna, lek przeciwdrgawkowy stosowany w chorobach ośrodkowego układu nerwowego. Jak również acetofenetydyna o działaniu przeciwbólowym.
Tworzenie p-nitrofenolu w wyniku działania niektórych enzymów na określone substraty
Fosforan 4-nitrofenylu jest syntetycznym substratem używanym do oznaczania fosfatazy alkalicznej. Gdy enzym działa na ten substrat, tworzy p-nitrofenol (bezbarwna substancja).
Później 4-nitrofenol traci protony, tworząc 4-nitrofenolan, który ma kolor żółty. Reakcja musi przebiegać przy alkalicznym pH> 9,0, aby promować konwersję do postaci beta (4-nitrofenolan).
Wytworzony kolor mierzy się spektrofotometrycznie przy 405 nm, dzięki czemu enzym można oznaczyć ilościowo.
To samo dotyczy innych enzymów na innych substratach. Wśród nich można wymienić działanie enzymu anhydrazy węglanowej na octan 4-nitrofenylu oraz glikozydazy na 4-nitrofenylo-β-D-glukopiranozyd.
Toksyczność
Według NFPA (National Fire Protection Association) p-nitrofenol zaliczany jest do substancji o stopniu zagrożenia zdrowia 3. Oznacza to, że szkody zdrowotne, jakie wyrządza, są poważne..
Z drugiej strony stwarza zagrożenie palnością 1, co oznacza, że ryzyko spowodowania pożaru jest niewielkie. Wreszcie, ma 2 stopień reaktywności (umiarkowane ryzyko). Oznacza to, że w określonych warunkach substancja ta może emitować energię.
Efekty zdrowotne
Do najważniejszych efektów zdrowotnych tej substancji należą te, o których wspomnimy poniżej.
Na poziomie skóry wywołuje podrażnienia, stany zapalne i oparzenia. Ponadto kontakt ze skórą stanowi drogę wchłaniania produktu. Przesadna ekspozycja na p-nitrofenol może wpływać na ośrodkowy układ nerwowy (OUN).
Na błonie śluzowej oka może powodować poważne oparzenia, z poważnymi uszkodzeniami oczu. Na poziomie dróg oddechowych, stany zapalne, kaszel i duszenie. W przypadku przypadkowego połknięcia powoduje wymioty z silnym bólem brzucha, dezorientacją, tachykardią, gorączką i osłabieniem..
Jeśli zostanie wchłonięty w dużych ilościach, może wywołać chorobę zwaną methemoglobinemią, charakteryzującą się wzrostem ilości methemoglobiny we krwi..
Choroba ta znacząco wpływa na transport tlenu i dlatego generuje objawy charakteryzujące się bólem głowy, zmęczeniem, zawrotami głowy, sinicą i niewydolnością oddechową. W ciężkich przypadkach może również spowodować śmierć.
Osoby narażone na niewielkie ilości wydalają produkt z moczem. Wreszcie, pomimo wszystkich opisanych szkodliwych skutków, nie udowodniono, że ma działanie rakotwórcze.
Pierwsza pomoc
W przypadku kontaktu z produktem należy zdjąć zanieczyszczoną odzież i przemyć dotknięte miejsce (skórę lub błony śluzowe) dużą ilością wody. W przypadku wdychania zabrać poszkodowanego w dobrze wentylowane miejsce. W przypadku, gdy pacjent nie oddycha, zastosować wspomagane oddychanie.
Następnie konieczne jest jak najszybsze przeniesienie ofiary do ośrodka opieki medycznej.
Środki bezpieczeństwa biologicznego
- Musisz pracować pod wyciągiem lub w inny sposób nosić respiratory. Noś odpowiednią odzież (fartuch, rękawiczki, okulary ochronne, zamknięte buty i czapkę).
- Odzież zanieczyszczoną produktem natychmiast wyprać.
- Nie zabierać do domu zanieczyszczonych narzędzi roboczych.
- Miejsce pracy powinno być wyposażone w płuczkę do oczu i natryski awaryjne.
- Podczas obchodzenia się z tą substancją nie należy nosić soczewek kontaktowych.
- Nie palić, nie jeść ani nie pić wewnątrz obiektów, w których ma miejsce ta substancja.
- Należy pamiętać, że p-nitrofenol jest niekompatybilny z niektórymi substancjami i dlatego należy go przechowywać oddzielnie od silnych zasad, takich jak wodorotlenek sodu lub wodorotlenek potasu. Jest również niekompatybilny z nadtlenkami, nadchloranami, nadmanganianami, chlorem, azotanami, chloranami, bromem i fluorem, między innymi utleniaczami..
- Należy pamiętać, że w przypadku pożaru pojemniki zawierające tę substancję mogą wybuchnąć..
Bibliografia
- Departament Zdrowia i Senior Services stanu New Jersey. Arkusz informacyjny o substancjach niebezpiecznych. 4-nitrofenol. 2004. Dostępne pod adresem: nj.gov/health.
- „4-nitrofenol”. Wikipedia, wolna encyklopedia. 22 lutego 2019 r., 13:58 UTC. 29 maja 2019, 03:59 wikipedia.org.
- Rojas H, Cubillos J, Guerrero D. Uwodornianie p-nitrofenolu przez zastosowanie katalizatorów Ir, Ni i Ir-Ni osadzonych na TiO2. Czasopismo Wydziału Inżynierii UPTC; 2012, 21 (3): 63–72
- Agencje ds. Substancji toksycznych i rejestru chorób. Podsumowania dotyczące zdrowia publicznego. Nitrofenole. Dostępne pod adresem: atsdr.cdc.gov
- Państwowy Zakład Bezpieczeństwa i Higieny Pracy. Międzynarodowe karty bezpieczeństwa chemicznego. 4-nitrofenol. Hiszpania. Dostępne pod adresem: insht.es/InshtWeb



Jeszcze bez komentarzy