
Struktura, właściwości, zastosowanie, produkcja siarczanu sodu (Na2SO4)

Plik siarczan sodu jest nieorganiczną solą, której wzór chemiczny to Nadwapołudniowy zachód4. Składa się z białego ciała stałego występującego w trzech formach: bezwodnej, heptahydratu (mało dostępny) i dekawodzianu (znanego jako sól Glauberta); ta ostatnia jest najbardziej rozpowszechnioną formą siarczanu sodu.
Dekahydrat siarczanu sodu, Nadwapołudniowy zachód410HdwaAlbo została odkryta w 1625 roku przez Glauberta w wodzie ze źródła, który nazwał ją sal mirabilis (cudowna sól) ze względu na jej właściwości lecznicze.

Siarczan sodu ma liczne zastosowania w przemyśle tekstylnym i papierniczym, a także w produkcji szkła. Jego zastosowania są rozszerzone na zastosowania termiczne, które obejmują dostarczanie ciepła z otoczenia i chłodzenie laptopa..
Siarczan sodu jest związkiem o niskiej toksyczności, a jego szkodliwe działanie jest głównie mechaniczne i niechemiczne. Ze względów krystalograficznych sól ta, podobnie jak jej potasowy odpowiednik, Kdwapołudniowy zachód4, posiada struktury kratowe i polimorficzne.
Indeks artykułów
- 1 Struktura
- 1.1 Bezwodna sól
- 1.2 Sól dekahydratowana
- 2 Właściwości
- 2.1 Nazwy
- 2.2 Masa molowa
- 2.3 Wygląd fizyczny
- 2.4 Zapach
- 2.5 Smak
- 2.6 Gęstość
- 2.7 Temperatura topnienia
- 2.8 Temperatura wrzenia
- 2.9 Rozpuszczalność w wodzie
- 2.10 Współczynnik załamania światła
- 2.11 Stabilność
- 2.12 Rozkład
- 2,13 pH
- 2.14 Reaktywność
- 3 Zastosowania
- 3.1 Przemysł papierniczy
- 3.2 Detergenty
- 3.3 Okulary
- 3.4 Przemysł włókienniczy
- 3.5 Medycyna
- 3.6 Środek suszący
- 3.7 Surowiec
- 4 Otrzymywanie
- 4.1 Wydobycie górnicze
- 4.2 Produkcja chemiczna
- 5 Ryzyka
- 6 Odnośniki
Struktura
Sól bezwodna
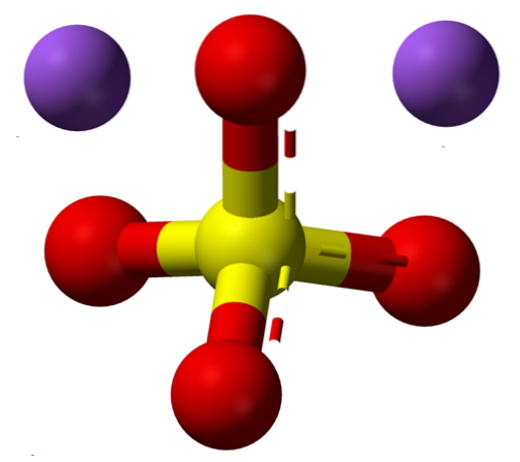
Formuła Nadwapołudniowy zachód4 wskazuje od razu, że jony Na w kryształach soli+ A więc4dwa- są w stosunku 1: 2; to znaczy na każde dwa kationy Na+ jest anion SO4dwa- oddziaływanie z nimi poprzez przyciąganie elektrostatyczne (górne zdjęcie).
Oczywiście dotyczy to Nadwapołudniowy zachód4 bezwodny, brak cząsteczek wody skoordynowanych z sodem w kryształach.
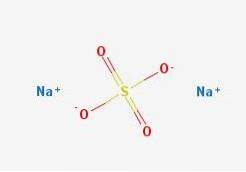
Pomimo pozornie prostej soli, jej opis jest strukturalnie złożony. Następniedwapołudniowy zachód4 charakteryzuje się polimorfizmem, posiadającym do pięciu faz krystalicznych: I, II, III, IV i V, których temperatury przejścia wynoszą odpowiednio 180, 200, 228, 235 i 883 ºC.
Chociaż nie ma żadnych odniesień do poświadczenia tego, Nadwapołudniowy zachód4Muszę być tym, który ma heksagonalną strukturę krystaliczną, gęstszą w porównaniu do ortorombowego Nadwapołudniowy zachód4III, w którego kryształach Na+ tworzą czworościany (NaO4) i ośmiościany (NaO6) koordynacja; to znaczy, może być otoczony przez cztery lub sześć anionów SO4dwa-.
Sól dekahydrowana
Tymczasem jednoskośna struktura krystaliczna jego najważniejszego hydratu, Nadwapołudniowy zachód410HdwaAlbo jest prostsze. W nim praktycznie cząsteczki wody oddziałują lub koordynują z Na+ w ośmiościach Na (H.dwaLUB)6+, z SO4dwa- zapewnienie wystarczającej stabilności kryształowi, tak aby istniał on w fazie stałej.
Jednak jego temperatura topnienia (32,38 ºC) znacznie niższa niż w przypadku bezwodnej soli (884 ºC) pokazuje, jak cząsteczki wody i ich wiązania wodorowe osłabiają silniejsze oddziaływania jonowe w Nadwapołudniowy zachód4.
Nieruchomości
Nazwy
-Siarczan Sodu (IUPAC)
-Sól Glaubera (dziesięciowodzian)
-Cudowna Sól (Dekawodzian)
-Siarczan disodowy.
Masa cząsteczkowa
142,04 g / mol (bezwodna)
322,20 g / mol (dekawodzian)
Wygląd fizyczny
Białe higroskopijne krystaliczne ciało stałe
Zapach
Toaleta
Smak
Gorzkie i słone
Gęstość
2664 g / cm3 (bezwodny)
1464 g / cm3 (dekawodzian)
Zwróć uwagę, jak cząsteczki wody wewnątrz kryształów powodują ich rozszerzanie się, a tym samym zmniejszają ich gęstość..
Temperatura topnienia
884 ºC (bezwodny)
32,38 ºC (dekawodzian)
Temperatura wrzenia
1,429 ºC (bezwodny)
Rozpuszczalność w wodzie
4,76 g / 100 ml (0 ºC)
13,9 g / 100 ml (20 ° C)
42,7 g / 100 ml (100 ° C)
Wszystkie wartości rozpuszczalności odpowiadają bezwodnej soli, która jest dobrze rozpuszczalna w wodzie we wszystkich temperaturach..
Rozpuszczalność wzrasta gwałtownie między 0ºC a 38,34ºC, obserwując, że w tym zakresie temperatur rozpuszczalność wzrasta ponad 10-krotnie. Jednak od 32,38 ° C rozpuszczalność jest niezależna od temperatury..
Zdarza się, że w temperaturze 32,8 ºC dekahydrat siarczanu sodu rozpuszcza się we własnej krystalicznej wodzie. W ten sposób zostaje osiągnięta równowaga między solą dekahydratu, solą bezwodną i nasyconym roztworem siarczanu sodu..
Dopóki utrzymywany jest stan trójfazowy, temperatura pozostanie stała, co pozwala na kalibrację temperatury termometrów.
Z drugiej strony rozpuszczalności heptahydratu soli są następujące:
19,5 g / 100 ml (0 ºC)
44,0 g / 100 ml (20 ° C)
Należy zauważyć, że w 20 ° C sól heptahydratowana jest trzykrotnie bardziej rozpuszczalna niż sól bezwodna..
Współczynnik załamania światła
1,468 (bezwodny)
1,394 (dekawodzian)
Stabilność
Stabilny w zalecanych warunkach przechowywania. Niekompatybilny z mocnymi kwasami i zasadami, aluminium i magnezem.
Rozkład
Po podgrzaniu w celu rozkładu wydziela toksyczny dym tlenku siarki i tlenku sodu..
pH
5% wodny roztwór ma pH 7.
Reaktywność
Siarczan sodu dysocjuje w roztworze wodnym na 2 Na+ A więc4dwa-, co pozwala jonowi siarczanowemu łączyć się z Badwa+ do strącania siarczanu baru. Praktycznie pomaga wypierać jony baru z próbek wody.
Siarczan sodu przekształca się w siarczek sodu w reakcji w podwyższonej temperaturze z węglem:
Nadwapołudniowy zachód4 + 2 C => NadwaS + 2 COdwa
Sól Glauberta, NaSO4.10HdwaLub reaguje z węglanem potasu, tworząc węglan sodu.
Aplikacje
Przemysł papierniczy
Do produkcji masy papierniczej stosuje się siarczan sodu. Wykorzystywany jest do produkcji papieru Kraft, który nie zawiera ligniny lub jest poddawany procesowi wybielania, co nadaje mu dużą odporność. Ponadto jest używany do produkcji tektury.
Detergenty
Używany jako wypełniacz syntetycznych detergentów domowych, dodawany do detergentu w celu zmniejszenia napięcia powierzchniowego.
Okulary
Jest stosowany w produkcji szkła w celu zmniejszenia lub wyeliminowania obecności małych pęcherzyków powietrza w stopionym szkle. Dodatkowo eliminuje tworzenie się żużla podczas rafinacji roztopionego szkła.
Przemysł włókienniczy
Siarczan sodu jest stosowany jako zaprawa, ponieważ ułatwia interakcję barwników z włóknami tkanin. W teście z barwnikiem stosuje się dekahydrat siarczanu sodu.
Ponadto siarczan sodu jest stosowany jako rozcieńczalnik barwnika i środek pomocniczy w drukowaniu barwników; takie jak barwniki bezpośrednie, barwniki siarkowe i inne czynniki sprzyjające barwieniu bawełny. Jest również stosowany jako opóźniacz do bezpośrednich barwników jedwabiu.
Lekarstwo
Dekahydrat siarczanu sodu jest stosowany jako środek przeczyszczający, ponieważ jest słabo wchłaniany w jelicie, a zatem pozostaje w świetle jelita powodując zwiększenie objętości. Stymuluje to wzrost skurczów perystaltycznych, które powodują wydalanie treści jelitowej..
Siarczan sodu jest antidotum do zwalczania zatrucia solą baru i ołowiu. Sól Glauberta jest skuteczna w eliminacji niektórych nadmiernie spożywanych leków; na przykład paracetamol (acetoaminofen).
Ponadto służy do uzupełniania niedoborów elektrolitów obecnych w roztworach izoosmotycznych..
Środek suszący
Siarczan sodu jako odczynnik obojętny służy do usuwania wody z roztworów związków organicznych..
Surowiec
Siarczan sodu jest stosowany jako surowiec do produkcji wielu substancji, w tym: siarczanu sodu, węglanu sodu, siarczanu amonu.
Otrzymywanie
Siarczan sodu otrzymuje się w wyniku wydobycia górniczego i reakcji chemicznych.
Wydobycie górnicze
Istnieją trzy rudy lub minerały, które są eksploatowane komercyjnie: następnieardyt (Nadwapołudniowy zachód4), mirabilit (Nadwapołudniowy zachód410HdwaO) i glaubarite (Nadwapołudniowy zachód4·Walizka4).
W Hiszpanii złoża thenardytu i mirabilitu są eksploatowane przez podziemne wydobycie chodników i filarów. W międzyczasie glauberyt pozyskuje się na otwartej przestrzeni za pomocą dużych tratw, które są umieszczane na złożu mineralnym.
Teren jest przygotowywany za pomocą piaskowania o niskiej intensywności, aby uzyskać porowatość, która umożliwia wypłukiwanie siarczanu sodu. Faza produkcji następuje podczas zraszania wodą słodką glauberytu, którego wypłukiwanie rozprzestrzenia się w dół..
Zbiera się solankę siarczanu sodu, pozostawiając pozostałość siarczanu wapnia jako wypełnienie..
Produkcja chemiczna
Siarczan sodu otrzymywany jest podczas produkcji kwasu solnego dwoma procesami: procesem Mannheim i procesem Hardgreaves.
Proces Mannheim
Odbywa się to w dużych stalowych piecach i 6-metrowej stalowej platformie reakcyjnej. Reakcja zachodzi między chlorkiem sodu i kwasem siarkowym:
2 NaCl + Hdwapołudniowy zachód4 => 2 HCl + Nadwapołudniowy zachód4
Proces Hardgreaves
Polega na reakcji chlorku sodu, tlenku siarki, tlenu i wody:
4 NaCl + 2 SOdwa + LUBdwa + 2 godzdwaO => 4 HCl + Nadwapołudniowy zachód4
Inni
Siarczan sodu powstaje w reakcji neutralizacji między wodorotlenkiem sodu a kwasem siarkowym:
2 NaOH + Hdwapołudniowy zachód4 => Nadwapołudniowy zachód4 + H.dwaLUB
Siarczan sodu jest produktem ubocznym powstawania wielu związków. Jest pozyskiwany z ciekłych odpadów odprowadzanych podczas produkcji wiskozy i celofanu. Również w produkcji dichromianu sodu, fenoli, kwasu borowego i karbaminianu litu.
Ryzyka
Siarczan sodu jest uważany za związek o niskiej toksyczności. Może jednak wyrządzić krzywdę osobie, która używa go niewłaściwie..
Na przykład może powodować podrażnienie oczu, zaczerwienienie i ból w kontakcie. Na skórze u niektórych osób może powodować podrażnienia i alergie. Jego połknięcie może spowodować podrażnienie przewodu pokarmowego z nudnościami, wymiotami i biegunką. I wreszcie jego wdychanie powoduje podrażnienie dróg oddechowych.
Bibliografia
- Shiver & Atkins. (2008). Chemia nieorganiczna. (Czwarta edycja). Mc Graw Hill.
- Wikipedia. (2019). Siarczan sodu. Odzyskane z: en.wikipedia.org
- Narodowe Centrum Informacji Biotechnologicznej. (2019). Siarczan sodu. Baza danych PubChem. CID = 24436. Odzyskany z: pubchem.ncbi.nlm.nih.gov
- B. N. Mehrotra. (1978). Struktura krystaliczna Nadwapołudniowy zachód4III. Odzyskany z: rruff-2.geo.arizona.edu
- Glauberite-Thenardyt (siarczan sodu). [PDF]. Odzyskany z: igme.es
Jeszcze bez komentarzy