
Charakterystyka i przykłady anomerycznego węgla
Plik węgiel anomeryczny jest stereocentrum obecnym w cyklicznych strukturach węglowodanów (mono lub polisacharydach). Będąc stereocentrum, a dokładniej epimerem, pochodzą z niego dwa diastereoizomery, oznaczone literami α i β; to są anomery i są częścią rozległej nomenklatury w świecie cukrów.
Każdy anomer, α lub β, różni się pozycją grupy OH anomerycznego węgla w stosunku do pierścienia; ale w obu anomeryczny węgiel jest taki sam i znajduje się w tym samym miejscu w cząsteczce. Anomery to cykliczne półacetale, produkt reakcji wewnątrzcząsteczkowej w otwartym łańcuchu cukrów; czy aldozy (aldehydy) czy ketozy (ketony).
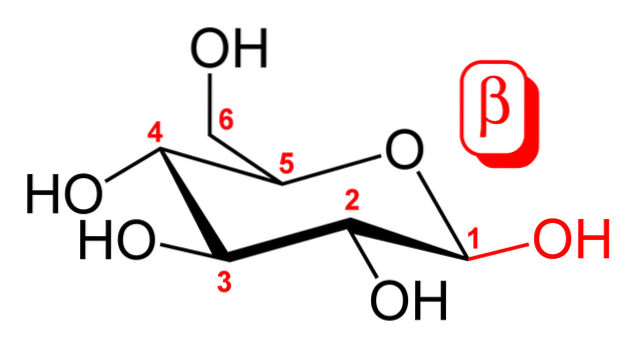
Górny obraz przedstawia konformację fotela dla β-D-glukopiranozy. Jak widać, składa się z sześcioczłonowego pierścienia, zawierającego atom tlenu między atomami węgla 5 i 1; ten ostatni, a raczej pierwszy, to anomeryczny węgiel, który tworzy dwa proste wiązania z dwoma atomami tlenu.
Jeśli przyjrzysz się uważnie, grupa OH przyłączona do węgla 1 jest zorientowana powyżej pierścienia heksagonalnego, podobnie jak grupa CHdwaOH (węgiel 6). To jest anomer β. Z drugiej strony anomer α różniłby się tylko tą grupą OH, która byłaby umiejscowiona w pierścieniu, tak jakby był diastereoizomerem trans..
Indeks artykułów
- 1 Hemiacetale
- 1.1 Cykliczny półacetal
- 2 Charakterystyka węgla anomerycznego i jak go rozpoznać
- 3 przykłady
- 3.1 Przykład 1
- 3.2 Przykład 2
- 3.3 Przykład 3
- 4 Odnośniki
Hemiacetale
Aby lepiej zrozumieć i rozróżnić węgiel anomeryczny, konieczne jest nieco głębsze zapoznanie się z koncepcją półacetali. Hemiacetale są produktem reakcji chemicznej między alkoholem a aldehydem (aldozami) lub ketonem (ketozy).
Tę reakcję można przedstawić za pomocą następującego ogólnego równania chemicznego:
ROH + R'CHO => ROCH (OH) R '
Jak widać, alkohol reaguje z aldehydem, tworząc półacetal. Co by się stało, gdyby oba R i R 'należały do tego samego łańcucha? W takim przypadku miałbyś cykliczny półacetal, a jedynym możliwym sposobem jego utworzenia jest obecność obu grup funkcyjnych, -OH i -CHO, w strukturze molekularnej..
Ponadto struktura musi składać się z elastycznego łańcucha i wiązań zdolnych do ułatwienia nukleofilowego ataku OH w kierunku karbonylowego węgla z grupy CHO. Kiedy tak się dzieje, struktura zamyka się w pięcio- lub sześcioczłonowy pierścień..
Cykliczny półacetal
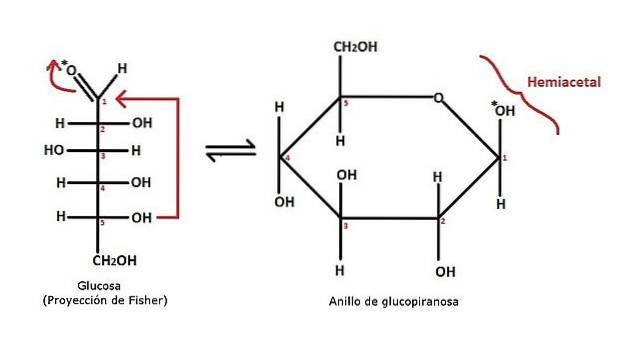
Przykład tworzenia cyklicznego półacetalu dla monosacharydu glukozy pokazano na powyższym obrazku. Można zauważyć, że składa się on z aldozy z grupą aldehydową CHO (węgiel 1). Jest to atakowane przez grupę OH węgla 5, jak wskazuje czerwona strzałka.
Struktura przechodzi od otwartego łańcucha (glukoza) do pierścienia piranowego (glukopiranoza). Na początku może nie być żadnego związku między tą reakcją a tą właśnie wyjaśnioną dla półacetalu; ale jeśli przyjrzysz się uważnie pierścieniowi, szczególnie w sekcji C5-O-C1(OH) -Cdwa, należy zauważyć, że odpowiada to oczekiwanemu szkieletowi półacetalu.
Węgle 5 i 2 reprezentują odpowiednio R i R 'ogólnego równania. Ponieważ są one częścią tej samej struktury, jest to cykliczny półacetal (a pierścień jest wystarczający, aby był widoczny).
Charakterystyka węgla anomerycznego i jak go rozpoznać
Gdzie jest węgiel anomeryczny? W przypadku glukozy jest to grupa CHO, która może ulec nukleofilowemu atakowi przez OH od dołu lub od góry. W zależności od kierunku ataku powstają dwa różne anomery: α i β, jak już wspomniano..
Dlatego pierwszą cechą charakterystyczną, jaką posiada ten węgiel, jest to, że w otwartym łańcuchu cukru to on cierpi na atak nukleofilowy; to znaczy jest to grupa CHO dla aldoz lub grupa R.dwaC = O, dla ketoz. Jednak po utworzeniu cyklicznego półacetalu lub pierścienia może się wydawać, że węgiel ten zniknął..
W tym miejscu istnieją inne, bardziej szczegółowe cechy, które pozwalają zlokalizować go w każdym pierścieniu piranu lub furanozy wszystkich węglowodanów:
-Anomeryczny węgiel znajduje się zawsze po prawej lub lewej stronie atomu tlenu tworzącego pierścień.
-Co ważniejsze, jest powiązany nie tylko z tym atomem tlenu, ale także z grupą OH, pochodzącą z CHO lub R.dwaC = O.
-Jest asymetryczny, to znaczy ma cztery różne podstawniki.
Dzięki tym czterem cechom łatwo jest rozpoznać węgiel anomeryczny, patrząc na jakąkolwiek „słodką strukturę”.
Przykłady
Przykład 1
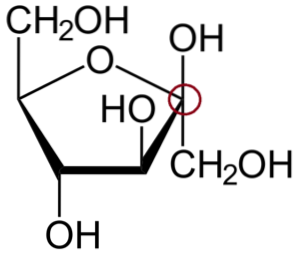
Powyżej znajduje się β-D-fruktofuranoza, cykliczny hemiacetal z pięcioczłonowym pierścieniem..
Aby zidentyfikować węgiel anomeryczny, należy najpierw przyjrzeć się atomom węgla po lewej i prawej stronie atomu tlenu tworzącego pierścień. Następnie ten, który jest połączony z grupą OH, jest atomem węgla; który w tym przypadku jest już zakreślony na czerwono.
Jest to anomer β, ponieważ grupa OH anomerycznego węgla znajduje się powyżej pierścienia, podobnie jak grupa CHdwaO.
Przykład 2
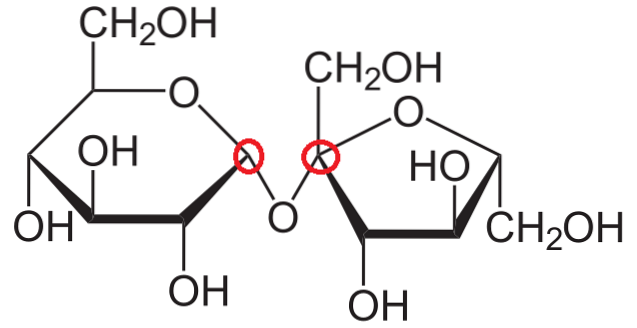
Teraz spróbujemy wyjaśnić, czym są węgle anomeryczne w strukturze sacharozy. Jak widać, składa się z dwóch monosacharydów kowalencyjnie połączonych wiązaniem glikozydowym, -O-.
Pierścień po prawej jest dokładnie taki sam, jak wspomniany przed chwilą: β-D-fruktofuranooza, tyle że jest „odwrócony” w lewo. Węgiel anomeryczny pozostaje taki sam jak w poprzednim przypadku i spełnia wszystkie cechy, których można by się po nim spodziewać.
Z drugiej strony pierścień po lewej stronie to α-D-glukopiranoza.
Powtarzając tę samą procedurę anomerycznego rozpoznawania węgla, patrząc na dwa atomy węgla po lewej i prawej stronie atomu tlenu, okazuje się, że prawy węgiel jest tym, który jest związany z grupą OH; który uczestniczy w wiązaniu glikozydowym.
Dlatego oba anomeryczne atomy węgla są połączone wiązaniem -O- i dlatego są otoczone czerwonymi okręgami..
Przykład 3
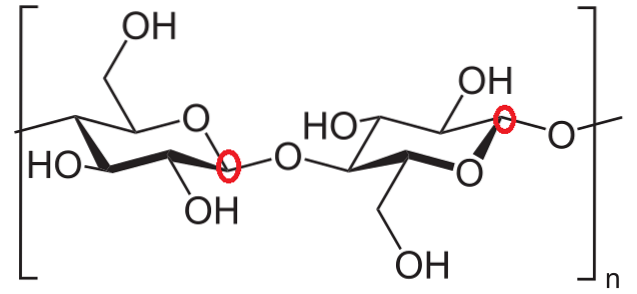
Na koniec proponuje się zidentyfikowanie anomerycznych atomów węgla dwóch jednostek glukozy w celulozie. Ponownie obserwuje się węgle wokół tlenu w pierścieniu i okazuje się, że w pierścieniu glukozy po lewej stronie anomeryczny węgiel uczestniczy w wiązaniu glikozydowym (zamkniętym w czerwonym kółku).
Jednak w pierścieniu glukozy po prawej stronie anomeryczny węgiel znajduje się na prawo od tlenu i można go łatwo zidentyfikować, ponieważ jest połączony z tlenem wiązania glikozydowego. W ten sposób oba anomeryczne atomy węgla są w pełni zidentyfikowane.
Bibliografia
- Morrison, R. T. and Boyd, R, N. (1987). Chemia organiczna. 5ta Wydanie. Od redakcji Addison-Wesley Interamericana.
- Carey F. (2008). Chemia organiczna. (Wydanie szóste). Mc Graw Hill.
- Graham Solomons T.W., Craig B. Fryhle. (2011). Chemia organiczna. Aminy. (10th wydanie.). Wiley plus.
- Rendina G. (1974). Stosowane techniki biochemiczne. Interamericana, Meksyk.
- Chang S. (s.f.). Przewodnik po węglu anomerycznym: Co to jest węgiel anomeryczny? [PDF]. Odzyskany z: chem.ucla.edu
- Gunawardena G. (13 marca 2018). Węgiel anomeryczny. Chemia LibreTexts. Źródło: chem.libretexts.org
- Foist L. (2019). Węgiel anomeryczny: definicja i przegląd. Nauka. Odzyskany z: study.com


Jeszcze bez komentarzy