
Charakterystyczne kinazy, typy, funkcje
Plik kinazy lub kinazySą to białka o aktywności enzymatycznej, które są odpowiedzialne za katalizowanie przenoszenia grup fosforanowych (PO4-3) do różnych typów cząsteczek. W naturze są niezwykle powszechnymi enzymami, w których pełnią transcendentalne funkcje dla organizmów żywych: uczestniczą w metabolizmie, sygnalizowaniu, a także w komunikacji komórkowej..
Dzięki dużej liczbie procesów, w których pełnią wielorakie funkcje, kinazy są jednym z najlepiej poznanych typów białek nie tylko na poziomie biochemicznym, ale także strukturalnym, genetycznym i komórkowym..
Ustalono, że genom człowieka ma co najmniej 500 genów kodujących enzymy należące do grupy kinaz, których „akceptorowymi” substratami grup fosforanowych mogą być węglowodany, lipidy, nukleozydy, białka i inne rodzaje cząsteczek organicznych.
Enzymy te zaliczane są do grupy fosfotransferaz (EC 2.7) i zwykle używają jako „donorowe” cząsteczek grup fosforanowych wysokoenergetycznych związków, takich jak ATP, GTP, CTP i inne pokrewne..
Indeks artykułów
- 1 Funkcje
- 2 rodzaje
- 2.1 EC 2.7.1: enzymy fosfotransferazy z alkoholem jako akceptorem grupy fosforanowej
- 2.2 EC 2.7.2: enzymy fosfotransferazy mające grupę karboksylową jako akceptor grupy fosforanowej
- 2.3 EC 2.7.3: enzymy fosfotransferazy mające atom azotu jako akceptor grupy fosforanowej
- 2.4 EC 2.7.4: enzymy fosfotransferazy mające inną grupę fosforanową jako akceptor grupy fosforanowej
- 2,5 EC 2.7.6: enzymy difosfotransferazy
- 2,6 EC 2.7.7: Enzymy fosfotransferazy specyficzne dla nukleotydów (fosfotransferazy nukleotydylowe)
- 2,7 EC 2.7.8: enzymy przenoszące grupy fosforanowe z substytucjami
- 2.8 EC 2.7.9: Enzymy fosfotransferazy ze sparowanymi akceptorami
- 2.9 Fosfotransferazy fosforylujące reszty aminokwasowe różnych typów białek
- 2.10 Inne formy klasyfikacji
- 3 Funkcje
- 4 Odnośniki
Charakterystyka
Termin „kinaza”, jak już wspomniano, zwykle odnosi się do wszystkich enzymów, które są odpowiedzialne za przeniesienie końcowej grupy fosforanowej ATP na inny receptor lub cząsteczkę „akceptorową” grupy fosforanowej..
Pomimo faktu, że enzymy te katalizują zasadniczo tę samą reakcję przeniesienia grup fosforylowych, istnieje między nimi duża różnorodność, nie tylko pod względem struktury, ale także specyfiki substratów i szlaków komórkowych, w których uczestniczą..
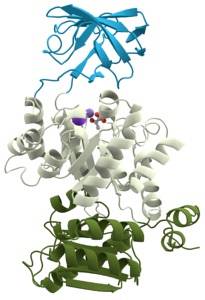
Ogólnie rzecz biorąc, jego struktura składa się z β-pofałdowanych arkuszy i α-helis, które fałdują się specyficznie, tworząc miejsce aktywne, a wspomniane miejsce aktywne zwykle zawiera dodatnio naładowane jony (kationy), które stabilizują ujemne ładunki przenoszonych grup fosforanowych.
Dwa miejsca wiązania substratów znajdują się w miejscu aktywnym lub w jego pobliżu: jedno dla ATP lub cząsteczki będącej donorem grup fosforanowych i jedno dla substratu, który ma być fosforylowany..
Ogólną reakcję tych enzymów (fosforylację) można rozpatrywać w następujący sposób:
ATP + podłoże → ADP + podłoże fosforylowane
Gdzie ATP przekazuje grupę fosforanową, którą zyskuje substrat.
Rodzaje
Zgodnie z klasyfikacją Komitetu Nomenklatury Międzynarodowej Unii Biochemii i Biologii Molekularnej (NC-IUBMB) kinazy znajdują się w grupie fosfotransferaz (EC. 2.7, enzymy przenoszące grupy zawierające fosfor), która jest podzielona na: z kolei w około 14 klasach (EC 2.7.1 - EC 2.7.14).
Podstawowe różnice między tymi 14 klasami fosfotransferaz są związane z chemiczną naturą cząsteczki „akceptorowej” grupy fosforanowej, którą przenoszą (lub naturą części cząsteczki, która otrzymuje grupę fosforanową)..
W tej kategorii (enzymy fosfotransferazy) znajdują się również enzymy przenoszące grupy fosforanowe, ale nie wykorzystujące cząsteczek ATP jako „donora”, lecz nieorganiczne fosforany..
Ogólnie rzecz biorąc, te klasy są opisane w następujący sposób:
EC 2.7.1: enzymy fosfotransferazy z alkoholem jako akceptorem grupy fosforanowej
Jest to jedna z najważniejszych grup dla metabolizmu energetycznego wielu organizmów, ponieważ zawiera enzymy odpowiedzialne za fosforylację węglowodanów i ich pochodnych, takie jak glukoza, galaktoza, fruktoza, mannoza, glukozamina, ryboza i rybuloza, ksyloza, glicerol , pirogronian, mewalonian, arabinoza, inozytol i wiele innych.
Przykładami tych powszechnych enzymów są heksokinaza, glukokinaza, fosfofruktokinaza i kinaza pirogronianowa, które są bezpośrednio zaangażowane w szlak glikolityczny odpowiedzialny za utlenianie glukozy w celu produkcji energii w postaci ATP.
EC 2.7.2: enzymy fosfotransferazy, które mają grupę karboksylową jako akceptor grupy fosforanowej
Do tej klasy enzymów kinaz lub fosfotransferaz należą enzymy przenoszące grupy fosforanowe na części cząsteczek z grupami karboksylowymi, takie jak między innymi octan, karbaminian, asparaginian, fosfoglicerynian..
EC 2.7.3: enzymy fosfotransferazy, które mają atom azotu jako akceptor dla grupy fosforanowej
Z metabolicznego punktu widzenia ta grupa enzymów ma również duże znaczenie, ponieważ są one odpowiedzialne za przenoszenie grup fosforanowych do cząsteczek takich jak kreatynina, arginina, glutamina, octan guanidyny itp..
EC 2.7.4: enzymy fosfotransferazy, które mają inną grupę fosforanową jako akceptor grupy fosforanowej
Duża część enzymów z tej grupy pełni funkcję w regulacji tworzenia lub hydrolizy związków wysokoenergetycznych, takich jak ATP, GTP, CTP i innych, ponieważ odpowiadają one za dodawanie, usuwanie lub wymianę grup fosforanowych między tymi typami cząsteczek.lub jego prekursorów.
Uczestniczą również w przenoszeniu grup fosforanowych do innych wcześniej fosforylowanych cząsteczek, które mogą mieć naturę lipidów, węglowodanów lub ich pochodnych..
Przykładami tych ważnych enzymów są kinaza adenylanowa, kinaza nukleozydowo-fosforanowa, kinaza nukleozydowo-trifosforanowo-adenylanowa, kinaza UMP / CMP i kinaza fosforanu farnezylu itp..
EC 2.7.6: enzymy difosfotransferazy
Difosfotransferazy katalizują przeniesienie dwóch grup fosforanowych jednocześnie na ten sam substrat. Przykładami takich enzymów są difosfokinaza rybozo-fosforanowa, difosfokinaza tiaminy i difosfokinaza GTP, która jest ważnym enzymem w metabolizmie puryn..
EC 2.7.7: enzymy fosfotransferazy specyficzne dla nukleotydów (fosfotransferazy nukleotydów)
Fosfotransferazy nukleotydylowe uczestniczą w wielu procesach komórkowych związanych z aktywacją i dezaktywacją innych białek i enzymów, a także w niektórych mechanizmach naprawy DNA.
Jego funkcją jest przenoszenie nukleotydów, ogólnie nukleotydów monofosforanowych o różnych zasadach azotowych. Do tej klasy enzymów należą między innymi polimerazy DNA i RNA (zależne zarówno od DNA, jak i RNA), urydylotransferaza UDP-glukozo-1-fosforanu..
EC 2.7.8: Enzymy przenoszące grupy fosforanowe z podstawieniami
Ta klasa ma istotne funkcje w szlakach metabolizmu lipidów, zwłaszcza w ich syntezie. Odpowiadają za przenoszenie fosforylowanych cząsteczek (grup fosforanowych z podstawnikami) na inne cząsteczki „akceptorowe”..
Przykładami tej grupy enzymów są fosfotransferaza etanoloaminy, fosfotransferaza diacyloglicerolocholiny, syntaza sfingomieliny itp..
EC 2.7.9: enzymy fosfotransferazy ze sparowanymi akceptorami
Enzymy te wykorzystują pojedynczy donor grup fosforanowych (ATP lub pokrewny) do fosforylacji dwóch różnych cząsteczek akceptorowych. Przykładami takich enzymów są dikinaza pirogronianowo-fosforanowa (PPDK) i fosfoglikanowa dikinaza wodna..
Fosfotransferazy, które fosforylują reszty aminokwasowe różnych typów białek
EC 2.7.10: kinazy białkowo-tyrozynowe
Kinazy białkowo-tyrozynowe to enzymy, które katalizują transfer grup fosforanowych specyficznie do reszt tyrozyny w łańcuchach polipeptydowych różnych typów akceptorów białek..
EC 2.7.11: kinazy białkowo-serynowo / treoninowe
Podobnie jak białkowe kinazy tyrozynowe, ta grupa enzymów katalizuje przeniesienie grup fosforanowych do reszt seryny lub treoniny w innych białkach..
Znanym przykładem tych białek jest rodzina kinaz białkowych C, które uczestniczą w wielu szlakach, ale szczególnie w metabolizmie lipidów..
Do tej grupy zalicza się również wiele cyklicznych AMP i cyklicznych zależnych od GMP kinaz białkowych, które mają ważne implikacje dla różnicowania, wzrostu i komunikacji komórek.
EC 2.7.12: kinazy mają podwójną specyficzność (mogą działać zarówno na reszty seryny / treoniny, jak i tyrozyny)
Kinazy białkowe aktywowane mitogenami (MAPKK) należą do tej grupy enzymów, które są zdolne do wymiennej fosforylacji reszt seryny, treoniny lub tyrozyny innych kinaz białkowych..
Kinazy białkowo-histydynowe (EC 2.7.13) i kinazy białkowo-argininowe (EC 2.7.14)
Istnieją inne kinazy białkowe zdolne do przenoszenia grup fosforanowych na reszty histydyny i argininy w niektórych typach białek i są to kinazy białkowo-histydynowe i kinazy białkowo-argininowe..
Inne formy klasyfikacji
Według różnych autorów kinazy można lepiej sklasyfikować w zależności od rodzaju substratu, którego używają jako akceptora grup fosforanowych..
Inni uważają, że najlepszym sposobem klasyfikacji tych enzymów jest struktura i charakterystyka ich miejsca aktywnego, to znaczy konformacja i obecność w nim jonów lub określonych cząsteczek..
W zależności od rodzaju substratu kinazy można podzielić na kinazy białkowe (które fosforylują inne białka), kinazy lipidowe (które fosforylują lipidy), kinazy węglowodanowe (które fosforylują różne rodzaje węglowodanów), fosforylazy nukleozydowe (które fosforylują nukleozydy) itp..
funkcje
Enzymy z grupy kinaz są z natury wszechobecne, a pojedyncza komórka może być gospodarzem setek różnych typów, katalizujących reakcje na wielu szlakach komórkowych..
Jego funkcje mogą być bardzo zróżnicowane:
-Biorą udział w wielu komórkowych procesach sygnalizacji i komunikacji, zwłaszcza w kinazach białkowych, które katalizują kolejną fosforylację innych kinaz białkowych (kaskady fosforylacji) w odpowiedzi na bodźce wewnętrzne i zewnętrzne..
-Niektóre z tych białek o aktywności enzymatycznej pełnią centralne funkcje w metabolizmie węglowodanów, lipidów, nukleotydów, witamin, kofaktorów i aminokwasów. Na przykład nic innego w glikolizie nie obejmuje co najmniej 4 kinaz: heksokinazy, fosfofruktokinazy, kinazy fosfoglicerynianowej i kinazy pirogronianowej..
-Wśród funkcji sygnalizacyjnych kinazy biorą udział w procesach regulacji ekspresji genów, skurczu mięśni i oporności na antybiotyki u różnych typów organizmów żywych.
-Kinazy białkowo-tyrozynowe odgrywają rolę w regulacji wielu szlaków przekazywania sygnałów, które są związane z rozwojem i komunikacją u wielokomórkowych metazoansów..
-Modyfikacja białek przez fosforylację (w innych kontekstach komórkowych innych niż sygnalizacja komórkowa) jest ważnym elementem regulacji aktywności dużej liczby enzymów uczestniczących w różnych procesach metabolicznych. Taki jest przykład regulacji cyklu komórkowego przez wiele zależnych od kinaz białek cyklinowych..
-Kinazy zdolne do fosforylacji lipidów są niezbędne w procesach przebudowy błon komórkowych, a także w syntezie i tworzeniu nowych błon.
Bibliografia
- Cheek, S., Zhang, H., & Grishin, N. V. (2002). Klasyfikacja sekwencji i struktury kinaz. Journal of Molecular Biology, 2836(02), 855-881.
- Cooper, J. (2018). Encyclopaedia Britannica. Pobrane z britannica.com
- Da Silva, G. (2012). Postępy w kinazach białkowych. Rijeka, Chorwacja: InTech Open.
- Krebs, E. (1983). Historyczne perspektywy fosforylacji białek i system klasyfikacji kinaz białkowych. Phil. Trans. R. Soc. Lond. b, 302, 3-11.
- Krebs, E. (1985). Fosforylacja białek: główny mechanizm regulacji biologicznej. Transakcje Towarzystwa Biochemicznego, 13, 813-820.
- Komitet ds. Nomenklatury Międzynarodowej Unii Biochemii i Biologii Molekularnej (NC-IUBMB). (2019). Odzyskany z qmul.ac.uk



Jeszcze bez komentarzy