
Struktura, zastosowania, właściwości chlorku żelaza (FeCl2)

Plik chlorek żelazawy jest nieorganicznym ciałem stałym utworzonym przez połączenie kationu Fedwa+ i dwa aniony chlorkowe Cl-. Jego wzór chemiczny to FeCldwa. Ma tendencję do wchłaniania wody z otoczenia. Jednym z jego hydratów jest tetrahydrat FeCldwa•4HdwaLub który jest zielonkawym ciałem stałym.
Należy zauważyć, że jest bardzo dobrze rozpuszczalny w wodzie i łatwo utlenia się w obecności powietrza, tworząc chlorek żelazowy FeCl.3. Ponieważ łatwo ulega utlenieniu, a zatem może działać jako środek redukujący, jest szeroko stosowany w laboratoriach chemicznych i biologicznych..

Chlorek żelazowy ma kilka zastosowań, z których najważniejszym jest pomoc innym czynnikom w utlenianiu szlamu pochodzącego ze ścieków lub z oczyszczania ścieków. Jest również stosowany w procesie żelaznego powlekania metali i ma pewne zastosowania w przemyśle farmaceutycznym..
Eksperymentowano również z użyciem FeCldwa w odzyskiwaniu cennych metali ze zużytych katalizatorów znajdujących się w rurach wydechowych pojazdów napędzanych benzyną lub olejem napędowym.
Jest używany w przemyśle tekstylnym do utrwalania kolorów w niektórych rodzajach tkanin.
Indeks artykułów
- 1 Struktura
- 2 Nazewnictwo
- 3 Właściwości
- 3.1 Stan fizyczny
- 3.2 Masa cząsteczkowa
- 3.3 Temperatura topnienia
- 3.4 Temperatura wrzenia
- 3.5 Ciężar właściwy
- 3.6 Rozpuszczalność
- 3.7 Inne właściwości
- 4 Otrzymywanie
- 5 zastosowań
- 5.1 W barwieniu tkanin
- 5.2 W oczyszczaniu ścieków
- 5.3 W badaniach chemicznych
- 5.4 W badaniach biochemicznych
- 6 Odnośniki
Struktura
Chlorek żelazawy składa się z jonu żelazawego Fedwa+ i dwa jony chlorkowe Cl- połączone wiązaniami jonowymi.
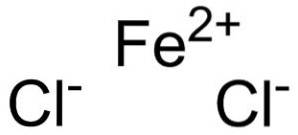
Jon żelazawy Fedwa+ ma następującą strukturę elektroniczną:
1sdwa, 2sdwa 2 P6, 3sdwa 3p6 3d6, 4s0
gdzie widać, że stracił dwa elektrony z powłoki 4s.
Ta konfiguracja nie jest bardzo stabilna iz tego powodu ma tendencję do utleniania, czyli utraty kolejnego elektronu, tym razem z warstwy 3d, tworząc jon Fe.3+.
Ze swojej strony jon chlorkowy Cl- ma następującą strukturę elektroniczną:
1sdwa, 2sdwa 2 P6, 3sdwa 3p6
gdzie widać, że uzyskał dodatkowy elektron w powłoce 3p, uzupełniając go. Ta konfiguracja jest bardzo stabilna, ponieważ wszystkie warstwy elektroniczne są kompletne.
Nomenklatura
- Chlorek żelazawy
- Chlorek żelaza (II)
- Dichlorek żelaza
- Tetrahydrat chlorku żelaza: FeCldwa•4HdwaLUB
Nieruchomości
Stan fizyczny
Bezbarwne lub bladozielone ciało stałe, kryształy.
Waga molekularna
126,75 g / mol
Temperatura topnienia
674 ºC
Temperatura wrzenia
1023 ºC
Dokładna waga
3,16 przy 25 ºC / 4 ºC
Rozpuszczalność
Bardzo dobrze rozpuszczalny w wodzie: 62,5 g / 100 ml w temperaturze 20 ºC. Rozpuszczalny w alkoholu, acetonie. Słabo rozpuszczalny w benzenie. Praktycznie nierozpuszczalny w eterze.
Inne właściwości
FeCldwa bezwodny jest bardzo higroskopijny. Łatwo absorbuje wodę ze środowiska, tworząc różnorodne hydraty, zwłaszcza tetrahydrat, w którym dla każdej cząsteczki FeCldwa istnieją 4 cząsteczki H.dwaLub dołączony do tego (FeCldwa•4HdwaLUB).
W obecności powietrza powoli utlenia się do FeCl3. Oznacza to, że jon Fedwa+ łatwo utlenia się do jonów Fe3+.
Po podgrzaniu w obecności powietrza szybko tworzy chlorek żelazowy FeCl3 i tlenek żelaza FedwaLUB3.
FeCldwa działa korodująco na metale i tkaniny.
Otrzymywanie
Uzyskuje się go przez traktowanie nadmiaru żelaza metalicznego Fe wodnym roztworem kwasu solnego HCl w wysokich temperaturach..
Wiara0 + 2 HCl → FeCldwa + 2 godz+
Jednak dzięki obecności wody tą metodą otrzymuje się tetrahydrat chlorku żelazawego FeCl.dwa•4HdwaLUB.
Aby otrzymać go w postaci bezwodnej (bez wody zawartej w kryształach), niektórzy badacze zdecydowali się przeprowadzić reakcję proszku żelaza z bezwodnym HCl (bez wody) w rozpuszczalniku tetrahydrofuranie (THF) w temperaturze 5 ºC..
W ten sposób otrzymuje się związek FeCldwa•1,5THF, który po podgrzaniu do 80-85 ºC pod próżnią lub w atmosferze azotu (w celu uniknięcia obecności wody) wytwarza FeCldwa bezwodny.
Aplikacje
Chlorek żelazawy ma różne zastosowania, głównie w oparciu o jego zdolność redukcyjną, to znaczy można go łatwo utleniać. Znajduje zastosowanie np. W farbach i powłokach, ponieważ ułatwia ich mocowanie do podłoża.
Żelazo jest niezbędnym mikroelementem dla zdrowia ludzi i niektórych zwierząt. Bierze udział w syntezie białek, oddychaniu i namnażaniu komórek.
Stąd FeCldwa jest stosowany w preparatach farmaceutycznych. Jon Fedwa+ jako taka jest lepiej wchłaniana niż jon Fe3+ w jelitach.
Służy do produkcji FeCl3. Jest stosowany w metalurgii, w kąpielach do powlekania żelaza, w celu uzyskania bardziej plastycznego osadu.
Oto inne polecane zastosowania.
W barwieniu tkanin
FeCldwa Jest stosowany jako zaprawa lub utrwalacz barwników w niektórych rodzajach tkanin. Zaprawa reaguje chemicznie i jednocześnie wiąże się z barwnikiem i tkaniną, tworząc na niej nierozpuszczalny związek..
W ten sposób barwnik pozostaje przytwierdzony do tkaniny, a jej kolor ulega intensyfikacji..
W oczyszczaniu ścieków
FeCldwa stosowany w oczyszczalniach ścieków lub oczyszczalniach ścieków (ścieki).
W tym zastosowaniu chlorek żelazawy uczestniczy w utlenianiu szlamu w procesie zwanym utlenianiem Fentona. To utlenianie powoduje rozpad kłaczków szlamu i umożliwia uwolnienie wody, która jest z nim silnie związana..

Następnie osad można wysuszyć i zutylizować w sposób przyjazny dla środowiska. Zastosowanie chlorku żelazawego pomaga obniżyć koszty procesu.
Ostatnio zaproponowano również użycie go do zmniejszenia tworzenia się siarkowodoru lub siarkowodoru w tych wodach ściekowych..
W ten sposób zmniejszyłaby się korozja wytwarzana przez ten gaz, a także nieprzyjemne zapachy..
W badaniach chemicznych
Ze względu na swoje właściwości redukujące (przeciwieństwo utleniacza) FeCldwa Jest szeroko stosowany w różnych badaniach w laboratoriach chemicznych, fizycznych i inżynieryjnych.
Niektórzy naukowcy używali oparów chlorku żelazawego do ekstrakcji cennych metali, takich jak platyna, pallad i rod, ze zużytych katalizatorów w pojazdach z silnikami benzynowymi lub wysokoprężnymi..
Te katalizatory służą do usuwania gazów szkodliwych dla ludzi i środowiska. Znajdują się w rurze wydechowej samochodów osobowych i ciężarowych zasilanych benzyną lub olejem napędowym.

Po pewnym czasie katalizator pojazdu zużywa się i traci skuteczność i należy go wymienić. Zużyty katalizator jest odrzucany i podejmowane są wysiłki mające na celu odzyskanie zawartych w nim cennych metali..

Zdaniem naukowców metale te tworzyły stopy magnetyczne z żelazem zawartym w chlorku żelazawym..
Stopy można było ekstrahować za pomocą magnesów, a następnie cenne metale odzyskiwać dobrze znanymi metodami..
W badaniach biochemicznych
Za posiadanie kationu Fedwa+, który jest ważnym mikroelementem u ludzi i niektórych zwierząt, FeCldwa stosowany w badaniach biochemicznych i medycznych.
Niektóre badania wykazały, że chlorek żelazawy poprawia skuteczność grzybobójczą zimnej plazmy argonowej..
Zimna plazma to technologia stosowana do sterylizacji powierzchni medycznych i instrumentów. Opiera się na tworzeniu rodników hydroksylowych OH · z wilgoci otoczenia. Rodniki te reagują ze ścianą komórkową mikroorganizmu i powodują jego śmierć.
W tym badaniu FeCldwa poprawiło działanie zimnej plazmy i przyspieszyło eliminację grzyba odpornego na inne metody dezynfekcji.
Niektórzy naukowcy odkryli, że stosowanie FeCldwa pozwala na zwiększenie wydajności reakcji otrzymywania glukozy wychodząc z wytłoków z trzciny cukrowej.
W tym przypadku, będąc Fedwa+ niezbędny mikroelement dla zdrowia ludzkiego, jego obecność w śladowych ilościach w produkcie nie wpłynie na ludzi.
Bibliografia
- Fukuda, S. i in. (2019). Chlorek żelazawy i siarczan żelazawy poprawiają skuteczność grzybobójczą zimnej atmosferycznej plazmy argonowej na melanizowane Aureobasidium pullulans. J Biosci Bioeng, 2019, 128 (1): 28–32. Odzyskany z ncbi.clm.nih.gov.
- Ismal, O.E. i Yildirim, L. (2019). Metalowe mordanty i biomordanty. Wpływ i perspektywy zielonej chemii dla technologii włókienniczych. Rozdział 3, s. 57-82. Odzyskany z sciencedirect.com.
- Zhang, W. i in. (2019). Współkataliza chlorku magnezu i chlorku żelazawego do produkcji ksylo-oligosacharydów i glukozy z wytłoków z trzciny cukrowej. Bioresour Technol 2019, 291: 121839. Odzyskany z ncbi.nlm.nih.gov.
- Zhou, X. i in. (2015). Rola rodzimego żelaza w poprawie odwadniania osadu poprzez peroksydację. Raporty naukowe 5: 7516. Odzyskany z ncbi.nlm.nih.gov.
- Rathnayake, D. i in. (2019). Kontrola siarkowodoru w kanalizacji poprzez katalizowanie reakcji z tlenem. Nauka o całkowitym środowisku 689 (2019) 1192-1200. Odzyskany z ncbi.nlm.nih.gov.
- Taninouchi, Y. i Okabe, T.H. (2018). Odzysk metali z grupy platynowców ze zużytych katalizatorów za pomocą obróbki parą chlorku żelaza. Metall and Materi Trans B (2018) 49: 1781. Odzyskany z link.springer.com.
- NAS. National Library of Medicine. (2019). Chlorek żelaza. Odzyskany z: pubchem.ncbi.nlm.nih.gov.
- Aresta, M. i in. (1977). Utlenianie żelaza (0) chlorowodorem w tetrahydrofuranie: prosta droga do bezwodnego chlorku żelaza (II). Inorganic Chemistry, tom 16, nr 7, 1977. Źródło: pubs.acs.org.
- Cotton, F. Albert i Wilkinson, Geoffrey. (1980). Zaawansowana chemia nieorganiczna. Czwarta edycja. John Wiley & Sons.



Jeszcze bez komentarzy