
Struktura dichlorometanu, właściwości, zastosowania, toksyczność
Plik dichlorometan, znany również jako chlorek metylenu, jest związkiem organicznym, którego wzór chemiczny to CHdwaCldwa. W szczególności jest to halogenek alkilu pochodzący z gazowego metanu. W przeciwieństwie do metanu, związek ten jest bezbarwną, polarną cieczą.
Początkowo został zsyntetyzowany w 1839 roku przez francuskiego chemika i fizyka Henri Victora Regnaulta (1810-1878), któremu udało się wyodrębnić go z mieszaniny chloru i chlorometanu wystawionej na działanie promieni słonecznych..

Dichlorometan jest produkowany przemysłowo poprzez traktowanie metanu lub chlorometanu gazowym chlorem w podwyższonych temperaturach (400-500 ° C). Wraz z dichlorometanem w procesie powstają chloroform i czterochlorek węgla, które są rozdzielane na drodze destylacji..
Dichlorometan jest stosowany jako rozpuszczalnik umożliwiający spawanie tworzyw sztucznych i odtłuszczanie metali. Znajduje również zastosowanie w odkażaniu kawy i herbaty, a także jako ekstraktor chmielu i rozcieńczalnik do barwników i tuszów do znakowania owoców.
Dichlorometan jest związkiem toksycznym, który może powodować podrażnienie dróg nosowych i gardła przez drogi oddechowe. Zgłaszano uszkodzenie wątroby u pracowników narażonych na wysokie stężenia dichlorometanu. Ponadto jest to czynnik mutagenny, co do którego istnieje podejrzenie, że jest rakotwórczy.
Indeks artykułów
- 1 Struktura
- 2 Właściwości
- 2.1 Wygląd
- 2.2 Masa molowa
- 2.3 Zapach
- 2.4 Próg zapachu
- 2.5 Gęstość
- 2.6 Temperatura topnienia
- 2.7 Temperatura wrzenia
- 2.8 Rozpuszczalność w wodzie
- 2.9 Rozpuszczalność w innych rozpuszczalnikach
- 2.10 Współczynnik podziału oktanol / woda
- 2.11 Prężność par
- 2.12 Gęstość par
- 2.13 Współczynnik załamania światła (πD)
- 2.14 Lepkość
- 2.15 Temperatura zapłonu
- 2.16 Temperatura samozapłonu
- 2.17 Stabilność
- 2.18 Rozkład
- 2.19 Korozja
- 2.20 Ciepło parowania
- 2.21 Napięcie powierzchniowe
- 2.22 Reaktywność
- 3 Zastosowania
- 3.1 Przetwórstwo spożywcze
- 3.2 Przemysł farmaceutyczny
- 3.3 Fotografia
- 3.4 Przemysł elektroniczny
- 3.5 Obrazy
- 3.6 Transport
- 3.7 Inne zastosowania
- 4 Toksyczność
- 4.1 Ostre skutki
- 4.2 Przewlekłe skutki
- 5 Referencje
Struktura
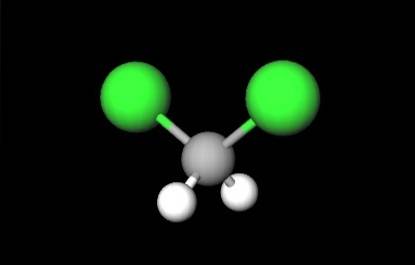
Pierwsze zdjęcie pokazało wzór strukturalny CHdwaCldwa, w którym wyróżniają się ich wiązania kowalencyjne C-H i C-Cl. Powyżej ma również swoją strukturę reprezentowaną przez model kul i prętów. Zauważ gołym okiem, że wiązania C-H (białe kule) są krótkie, podczas gdy wiązania C-Cl (zielone kule) są długie.
Geometria CHdwaCldwa jest czworościenny; ale zniekształcone przez większe atomy chloru. Jeden koniec czworościanu jest określony przez dwa atomy chloru, bardziej elektroujemne niż atom wodoru i węgla. Stąd w cząsteczce CHdwaCldwa ustala się stały moment dipolowy (1,6D).
Pozwala to cząsteczkom dichlorometanu na interakcję ze sobą poprzez siły dipol-dipol. Podobnie te interakcje międzycząsteczkowe są odpowiedzialne za fakt, że związek ten istnieje w postaci cieczy pomimo swojej małej masy cząsteczkowej; ciecz, która jest jednak dość lotna.
Nieruchomości
Wygląd
Bezbarwna ciecz.
Masa cząsteczkowa
84,93 g / mol.
Zapach
Słodki, podobny do chloroformu.
Próg zapachu
205-307 ppm.
Gęstość
1,3266 g / cm3 (20 ºC).
Temperatura topnienia
- 97,6 ° C.
Temperatura wrzenia
39,6 ° C.
Rozpuszczalność w wodzie
25,6 g / l przy 15 ° C i 5,2 g / l przy 60 ° C.
Dichlorometan jest słabo rozpuszczalny w wodzie. Podczas gdy obie cząsteczki, CHdwaCldwa i HdwaLub, są polarne, ich interakcje są nieefektywne, prawdopodobnie z powodu odpychania między atomami chloru i tlenu.
Rozpuszczalność w innych rozpuszczalnikach
Mieszalny z octanem etylu, alkoholem, heksanem, benzenem, czterochlorkiem węgla, eterem dietylowym, chloroformem i dimetyloformamidem.
Współczynnik podziału oktanol / woda
Log P = 1,19.
Ciśnienie pary
57,3 kPa (25 ° C). To ciśnienie odpowiada około 5,66 atm, co odzwierciedla wysokie ciśnienie pary..
Gęstość pary
2,93 w stosunku do powietrza przyjętego jako 1.
Współczynnik załamania (πD)
1,4244 (20 ºC).
Lepkość
0,413 cP (25 ° C).
punkt zapłonu
Dichlorometan nie jest łatwopalny, ale zmieszany z powietrzem tworzy palne opary powyżej 100ºC..
Temperatura samozapłonu
556 ºC.
Stabilność
Jest stabilny w temperaturze otoczenia przy braku wilgoci, wykazując względną stabilność w porównaniu do swoich kongenerów: chloroformu i czterochlorku węgla..
Ma skłonność do zwęglenia w wysokich temperaturach (300-450 ºC), kiedy jego opary wchodzą w kontakt ze stalą i chlorkami metali.
Rozkład
Może rozkładać się w kontakcie z gorącymi powierzchniami lub płomieniem, wydzielając toksyczne i drażniące opary fosgenu i chlorowodoru..
Korozja
Dichlorometan atakuje niektóre formy tworzyw sztucznych, gumy i powłoki.
Ciepło parowania
28,82 kJ / mol w 25 ° C.
Napięcie powierzchniowe
28,20 dyn / cm przy 25 ° C.
Reaktywność
Dichlorometan silnie reaguje z aktywnymi metalami, takimi jak potas, sód i lit. Reaguje z mocnymi zasadami, np. Tert-butanolanem potasu. Jest niekompatybilny z substancjami żrącymi, utleniaczami i metalami chemicznie czynnymi.
Dodatkowo reaguje z ciekłym tlenem zawartym w stopach sodu i potasu oraz czterotlenkiem azotu. W kontakcie z wodą może powodować korozję niektórych stali nierdzewnych, niklu, miedzi, a także żelaza.
Aplikacje
Większość zastosowań i zastosowań dichlorometanu opiera się na jego właściwościach jako rozpuszczalnika. Ze względu na tę właściwość dichlorometan znajduje zastosowanie w przemyśle spożywczym, transportowym, medycznym itp..
Przetwórstwo spożywcze
Dichlorometan jest stosowany do odkofeinowania ziaren kawy i liści herbaty. Służy również do ekstrakcji chmielu do piwa, napojów i innych aromatów spożywczych, a także do przetwarzania przypraw..
Przemysł farmaceutyczny
Dichlorometan służy do przygotowania cefalosporyny i ampicyliny, oprócz produkcji antybiotyków, sterydów i witamin.
Fotografia
Znajduje również zastosowanie jako rozpuszczalnik przy produkcji trioctanu celulozy (CTA), wykorzystywanego przy tworzeniu folii zabezpieczających.
Przemysł elektroniczny
Jest idealnym związkiem do produkcji obwodów drukowanych, służy do odtłuszczania powierzchni aluminium przed nałożeniem warstwy fotorezystu na płytkę..
Malatura
Dichlorometan to rozpuszczalnik występujący w lakierach i separatorach farb, stosowany do usuwania lakierów lub powłok malarskich z różnego rodzaju powierzchni..
Transport
Służy do odtłuszczania części i powierzchni metalowych występujących w sprzęcie kolejowym, a także w podzespołach samolotów.
Inne zastosowania
Stosowany jest jako propelent do rozpylania (aerozole) oraz jako porofor do pianki poliuretanowej. Jest również stosowany jako płyn w niektórych typach lampek choinkowych.
Toksyczność
Ostre efekty
Wdychanie dichlorometanu może powodować podrażnienie górnych dróg oddechowych, kaszel, świszczący oddech lub duszność..
Może powodować zaczerwienienie skóry, a jeśli związek utrzyma się na niej przez długi czas, spowodować oparzenia chemiczne. W kontakcie z oczami dichlorometan powoduje silne podrażnienie, które może prowadzić do oparzenia.
Ponadto działa jako neurotoksyna powodująca zaburzenia widzenia, słuchu i psychomotoryczne; ale efekty te są odwracalne po zatrzymaniu wdychania dichlorometanu.
Przewlekłe skutki
Dichlorometan może wpływać na ośrodkowy układ nerwowy, powodując bóle głowy, dezorientację, nudności, wymioty i utratę pamięci..
U zwierząt działa szkodliwie na wątrobę, nerki, ośrodkowy układ nerwowy i układ sercowo-naczyniowy.
Jeśli chodzi o karcynogenezę, nie odnotowano znaczącego wzrostu liczby zgonów z powodu raka u pracowników narażonych na dichlorometan. Jednak badania na zwierzętach wykazały wzrost częstości występowania raka wątroby i płuc, a także łagodnych guzów gruczołów sutkowych, który można przypisać dichlorometanowi..
Bibliografia
- Morrison, R. T. i Boyd, R, N. (1987). Chemia organiczna. 5ta Wydanie. Od redakcji Addison-Wesley Interamericana.
- Carey F. (2008). Chemia organiczna. (Wydanie szóste). Mc Graw Hill.
- Graham Solomons T.W., Craig B. Fryhle. (2011). Chemia organiczna. (10th wydanie.). Wiley plus.
- Narodowe Centrum Informacji Biotechnologicznej. (2020). Dichlorometan. Baza danych PubChem., CID = 6344. Odzyskany z: pubchem.ncbi.nlm.nih.gov
- Wikipedia. (2020). Dichlorometan. Odzyskane z: en.wikipedia.org
- Brumer. (14 lipca 2018). Dichlorometan. Odzyskany z: brumer.com
- MSDS Online. (2019). Dichlorometan (chlorek metylenu) Zagrożenia i informacje dotyczące bezpieczeństwa. Odzyskany z: msdsonline.com
- EPA. (2000). Chlorek metylenu (dichlorometan). [PDF]. Odzyskany z: epa.gov


Jeszcze bez komentarzy