
Właściwości skali mikroskopowej, liczenie cząstek, przykłady
Plik mikroskopijna skala Jest to taki, który służy do pomiaru rozmiarów i długości, których nie można zobaczyć gołym okiem i które są poniżej milimetra długości. Od najwyższej do najniższej, mikroskopijne skale w systemie metrycznym to:
- Milimetr (1 mm), czyli jedna dziesiąta centymetra lub jedna tysięczna metra. W takiej skali mamy jedną z największych komórek ciała, jaką jest komórka jajowa, której rozmiar wynosi 1,5 mm.
- Dziesiąta część milimetra (0,1 mm). To jest skala grubości lub średnicy ludzkiego włosa.
- Mikrometr lub mikron (1 μm = 0,001 mm). W tej skali są komórki roślinne i zwierzęce oraz bakterie.
Komórki roślinne są rzędu 100 μm. Komórki zwierzęce są dziesięciokrotnie mniejsze, są rzędu 10 μm; podczas gdy bakterie są 10 razy mniejsze od komórek zwierzęcych i są rzędu 1 μm.
Indeks artykułów
- 1 nanoskala
- 2 Przyrządy do obserwacji mikroskopowych
- 3 Właściwości mikroskopowe
- 3.1-Materia to ogromna pustka
- 4 Jak liczyć cząstki w skali mikroskopowej?
- 4.1 - Przykład 1
- 4.2 - Przykład 2
- 5 Referencje
Skala nano
Istnieją pomiary nawet mniejsze niż skala mikroskopowa, ale nie są one powszechnie używane, z wyjątkiem niektórych specjalnych kontekstów. Oto niektóre z najważniejszych pomiarów nanometrycznych:
- Nanometr (1 ηm = 0,001 μm = 0,000001 mm) to jedna milionowa milimetra. W tej skali są niektóre wirusy i cząsteczki. Wirusy są rzędu 10 ηm, a cząsteczki rzędu 1 ηm.
- Angstrem (1Å = 0,1ηm = 0,0001μm = 10-7mm). Ten pomiar określa skalę lub rozmiar atomu.
- Fantomometr (1fm = 0,00001Å = 0,000001ηm = 10-12mm). Jest to skala jąder atomowych, które są od 10 000 do 100 000 razy mniejsze od atomu. Jednak pomimo niewielkich rozmiarów jądro skupia 99,99% masy atomowej.
- Jądro atomowe ma mniejsze łuski, ponieważ składają się one z cząstek, takich jak protony i neutrony. Ale jest więcej: te cząstki składają się z kolei z bardziej podstawowych cząstek, takich jak kwarki..
Przyrządy do obserwacji mikroskopowych
Gdy obiekty znajdują się między podziałką milimetrową a mikrometryczną (1 mm - 0,001 mm), można je obserwować za pomocą mikroskopu optycznego.
Jeśli jednak obiekty lub struktury znajdują się między nanometrami a angstremami, wymagane będą mikroskopy elektronowe lub nanoskop..
W mikroskopii elektronowej zamiast światła stosuje się elektrony o wysokiej energii, które mają znacznie krótszą długość fali niż światło. Wadą mikroskopu elektronowego jest to, że nie można w nim umieścić żywych próbek, ponieważ działa w próżni..
Zamiast tego nanoskop wykorzystuje światło laserowe i ma przewagę nad mikroskopią elektronową, że struktury i cząsteczki w żywej komórce mogą być oglądane i rejestrowane..
Nanotechnologia to technologia, za pomocą której obwody, struktury, części, a nawet silniki są wytwarzane w skali od nanometra do skali atomowej.
Właściwości mikroskopowe
W fizyce w pierwszym przybliżeniu zachowanie materii i układów jest badane z makroskopowego punktu widzenia. Z tego paradygmatu materia jest nieskończenie podzielnym kontinuum; i ten punkt widzenia jest ważny i odpowiedni w wielu sytuacjach życia codziennego.
Jednak niektóre zjawiska w świecie makroskopowym można wyjaśnić tylko wtedy, gdy weźmie się pod uwagę mikroskopowe właściwości materii..
Z mikroskopowego punktu widzenia brana jest pod uwagę molekularna i atomowa struktura materii. W przeciwieństwie do podejścia makroskopowego, w tej skali występuje struktura ziarnista z lukami i przestrzeniami między cząsteczkami, atomami, a nawet wewnątrz nich..
Inną cechą fizyczną z mikroskopijnego punktu widzenia jest to, że kawałek materii, nieważne jak mały, składa się z ogromnej liczby cząstek oddzielonych od siebie i będących w ciągłym ruchu..
-Materia jest ogromną pustką
W małym kawałku materii odległość między atomami jest ogromna w porównaniu z ich rozmiarami, ale z kolei atomy są ogromne w porównaniu z ich własnymi jądrami, w których skoncentrowane jest 99,99% masy..
Oznacza to, że kawałek materii w skali mikroskopowej to ogromna próżnia ze stężeniami atomów i jąder, które zajmują niewielki ułamek całkowitej objętości. W tym sensie skala mikroskopowa jest podobna do skali astronomicznej..
Od obiektów makroskopowych po odkrycie atomu
Pierwsi chemicy, którzy byli alchemikami, zdali sobie sprawę, że materiały mogą być dwojakiego rodzaju: czyste lub złożone. W ten sposób powstała idea pierwiastków chemicznych.
Pierwszymi odkrytymi pierwiastkami chemicznymi było siedem starożytnych metali: srebro, złoto, żelazo, ołów, cyna, miedź i rtęć. Z biegiem czasu odkryto więcej, do tego stopnia, że znaleziono substancje, których nie można było rozłożyć na inne.
Następnie pierwiastki zostały sklasyfikowane według ich właściwości i właściwości w metalach i niemetalach. Wszystkie te, które miały podobne właściwości i powinowactwo chemiczne, zostały zgrupowane w tej samej kolumnie, a tym samym powstał układ okresowy pierwiastków..
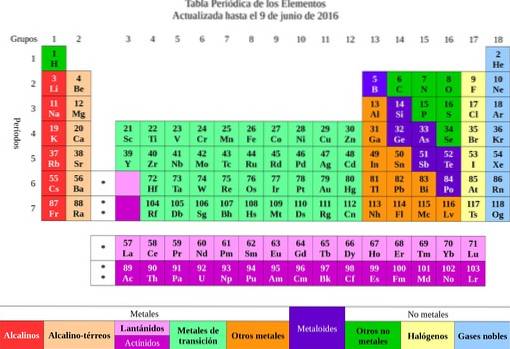
Z elementów przekazano ideę atomów, słowo oznaczające niepodzielność. Niedługo później naukowcy zdali sobie sprawę, że atomy mają strukturę. Ponadto atomy miały dwa rodzaje ładunku elektrycznego (dodatni i ujemny).
Cząstki elementarne
W eksperymentach Rutherforda, w których bombardował atomy cienkiej złotej płytki cząstkami alfa, ujawniono strukturę atomu: małe dodatnie jądro otoczone elektronami.
Atomy były nadal bombardowane coraz większą ilością cząstek energii i nadal jest to robione, aby odkryć tajemnice i właściwości mikroskopijnego świata na coraz mniejszą skalę..
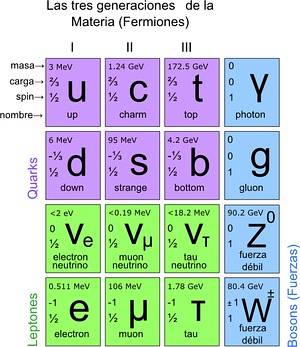
W ten sposób uzyskano model standardowy, w którym ustalono, że prawdziwymi cząstkami elementarnymi są te, z których zbudowane są atomy. Z kolei z atomów powstają pierwiastki, te związki i wszystkie znane interakcje (z wyjątkiem grawitacji). W sumie jest 12 cząstek.
Te podstawowe cząstki mają również swój układ okresowy. Istnieją dwie grupy: fermionowe cząstki o spinie ½ i bozonowe. Bozony są odpowiedzialne za interakcje. Fermioniki to 12 i to te, z których powstają protony, neutrony i atomy.
Jak liczyć cząstki w skali mikroskopowej?
Z biegiem czasu chemicy odkrywali względne masy pierwiastków na podstawie precyzyjnych pomiarów w reakcjach chemicznych. Można więc na przykład ustalić, że węgiel jest 12 razy cięższy od wodoru..
Wodór również uznano za najlżejszy pierwiastek, więc temu elementowi przypisano względną masę 1.
Z drugiej strony chemicy musieli znać liczbę cząsteczek biorących udział w reakcji, aby żaden odczynnik nie został wyczerpany ani nie brakuje go. Na przykład cząsteczka wody wymaga dwóch atomów wodoru i jednego atomu tlenu..
Z tych poprzedników rodzi się pojęcie mola. Mol dowolnej substancji to ustalona liczba cząstek równoważna jej masie cząsteczkowej lub atomowej w gramach. W ten sposób ustalono, że 12 gramów węgla ma taką samą liczbę cząstek jak 1 gram wodoru. Ta liczba jest znana jako liczba Avogadro: 6,02 x 10 ^ 23 cząstek.
-Przykład 1
Oblicz, ile atomów złota znajduje się w 1 gramie złota.
Rozwiązanie
Wiadomo, że złoto ma masę atomową 197. Dane te można znaleźć w układzie okresowym pierwiastków i wskazują, że atom złota jest 197 razy cięższy od atomu wodoru i 197/12 = 16 416 razy cięższy od węgla..
Mol złota ma 6,02 × 10 ^ 23 atomów i ma masę atomową wyrażoną w gramach, czyli 197 gramów.
W jednym gramie złota znajduje się 1/197 mola złota, czyli 6,02 × 10 ^ 23 atomy / 197 = 3,06 x10 ^ 23 atomy złota.
-Przykład 2
Określ liczbę cząsteczek węglanu wapnia (CaCO3), które znajdują się w 150 gramach tej substancji. Powiedz także, ile atomów wapnia, ile węgla i ile tlenu jest w tym związku.
Rozwiązanie
Pierwszą rzeczą jest określenie masy cząsteczkowej węglanu wapnia. Układ okresowy wskazuje, że wapń ma masę cząsteczkową 40 g / mol, węgiel 12 g / mol i tlen 16 g / mol..
Następnie masa cząsteczkowa (CaCO3) będzie :
40 g / mol + 12 g / mol + 3 x 16 g / mol = 100 g / mol
Każde 100 gramów węglanu wapnia to 1 mol. Tak więc w 150 gramach odpowiadają one 1,5 mola.
Każdy mol węglanu ma 6,02 x 10 ^ 23 cząsteczek węglanu, więc w 1,5 mola węglanu znajduje się 9,03 x 10 ^ 23 cząsteczek.
Krótko mówiąc, w 150 gramach węglanu wapnia znajduje się:
- 9,03 x 10 ^ 23 cząsteczek węglanu wapnia.
- Atomy wapnia: 9,03 x 10 ^ 23 .
- Również 9,03 x 10 ^ 23 atomów węgla
- Wreszcie 3 x 9,03 x 10 ^ 23 atomów tlenu = 27,09 x 10 ^ 23 atomów tlenu.
Bibliografia
- Biologia stosowana. Jakie są pomiary mikroskopowe? Odzyskany z: youtube.com
- Edukacja chemiczna. Makroskopowe, submikroskopowe i symboliczne przedstawienia materii. Odzyskany z: scielo.org.mx.
- García A. Interaktywny kurs fizyki. Makrostany, mikropaństwa. Temperatura, entropia. Odzyskany z: sc.ehu.es
- Mikroskopijna budowa materii. Odzyskany z: alipso.com
- Wikipedia. Poziom mikroskopowy. Odzyskane z: wikipedia.com



Jeszcze bez komentarzy