
Charakterystyka, budowa i funkcje Helicasa
Plik helikaza odnosi się do grupy enzymów typu hydrolitycznego białek, które są bardzo ważne dla wszystkich organizmów żywych; nazywane są również białkami motorycznymi. Przemieszczają się one przez cytoplazmę komórki, przekształcając energię chemiczną w pracę mechaniczną poprzez hydrolizę ATP..
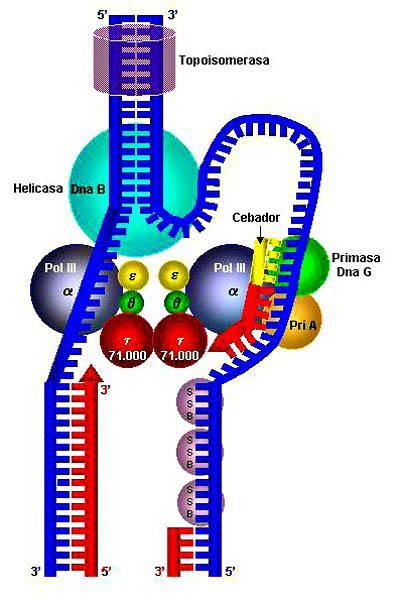
Jego najważniejszą funkcją jest rozrywanie wiązań wodorowych między zasadami azotowymi kwasów nukleinowych, umożliwiając w ten sposób ich replikację. Należy podkreślić, że helikazy są praktycznie wszechobecne, ponieważ są obecne w wirusach, bakteriach i organizmach eukariotycznych..
Pierwsze z tych białek lub enzymów odkryto w 1976 roku u bakterii Escherichia coli; dwa lata później pierwszą helikazę odkryto w organizmie eukariotycznym, w roślinach lilii.
Obecnie białka helikazy zostały scharakteryzowane we wszystkich królestwach przyrody, w tym wirusach, co oznacza, że uzyskano ogromną wiedzę na temat tych enzymów hydrolitycznych, ich funkcji w organizmach i ich mechanistycznej roli..
Indeks artykułów
- 1 Funkcje
- 1.1 helikaza DNA
- 1.2 helikaza RNA
- 2 Taksonomia
- 2.1 SF1
- 2.2 SF2
- 2,3 SF3
- 2,4 SF4
- 2,5 SF5
- 2,6 SF6
- 3 Struktura
- 4 Funkcje
- 4.1 helikaza DNA
- 4.2 Helikaza RNA
- 5 Znaczenie medyczne
- 5.1 Zespół Wernera
- 5.2 Zespół Blooma
- 5.3 Zespół Rothmunda-Thomsona
- 6 Odnośniki
Charakterystyka
Helikazy to biologiczne lub naturalne makrocząsteczki, które przyspieszają reakcje chemiczne (enzymy). Charakteryzują się głównie oddzielaniem kompleksów chemicznych trifosforanu adenozyny (ATP) poprzez hydrolizę.
Enzymy te wykorzystują ATP do wiązania i przebudowy kompleksów kwasów dezoksyrybonukleinowych (DNA) i rybonukleinowych (RNA)..
Istnieją co najmniej 2 rodzaje helikaz: DNA i RNA.
Helikaza DNA
Helikazy DNA działają w procesie replikacji DNA i charakteryzują się rozdzielaniem dwuniciowego DNA na pojedyncze nici.
Helikaza RNA
Enzymy te działają w procesach metabolicznych kwasu rybonukleinowego (RNA) oraz w namnażaniu, rozmnażaniu lub biogenezie rybosomów.
Helikaza RNA jest również kluczowa w procesie pre-splicingu informacyjnego RNA (mRNA) i inicjacji syntezy białek po transkrypcji DNA na RNA w jądrze komórkowym..
Taksonomia
Enzymy te można różnicować zgodnie z ich homologią sekwencjonowania aminokwasów z domeną ATPazy aminokwasu rdzeniowego lub według wspólnych motywów sekwencjonowania. Zgodnie z klasyfikacją są one pogrupowane w 6 nadrodzin (SF 1-6):
SF1
Enzymy z tej nadrodziny mają biegunowość translokacji 3'-5 'lub 5'-3' i nie tworzą struktur pierścieniowych..
SF2
Jest znany jako największa grupa helikaz i składa się głównie z helikaz RNA. Mają one ogólnie polaryzację translokacji 3'-5 'z nielicznymi wyjątkami.
Mają dziewięć motywów (z angielskiego motywy, co jest tłumaczone jako „powtarzające się elementy”) wysoce konserwatywnych sekwencji aminokwasowych i, podobnie jak SF1, nie tworzą struktur pierścieniowych.
SF3
Są charakterystycznymi helikazami wirusów i mają unikalną biegunowość translokacji 3'-5 '. Posiadają tylko cztery wysoce konserwatywne motywy sekwencji i tworzą struktury pierścieniowe lub pierścienie.
SF4
Po raz pierwszy opisano je u bakterii i bakteriofagów. Są grupą replikujących się lub replikujących helikaz.
Mają unikalną polaryzację translokacji 5'-3 'i mają pięć wysoce konserwatywnych motywów sekwencji. Te helikazy charakteryzują się tworzeniem pierścieni.
SF5
Są to białka typu czynnika Rho. Helikazy z nadrodziny SF5 są charakterystyczne dla organizmów prokariotycznych i są heksameryczne zależne od ATP. Uważa się, że są blisko spokrewnione z SF4; ponadto mają pierścieniowe i nie-pierścieniowe kształty.
SF6
Są to białka najwyraźniej spokrewnione z nadrodziną SF3; jednak SF6 prezentują domenę białek ATPazy związanych z różnymi czynnościami komórkowymi (białka AAA), które nie są obecne w SF3.
Struktura
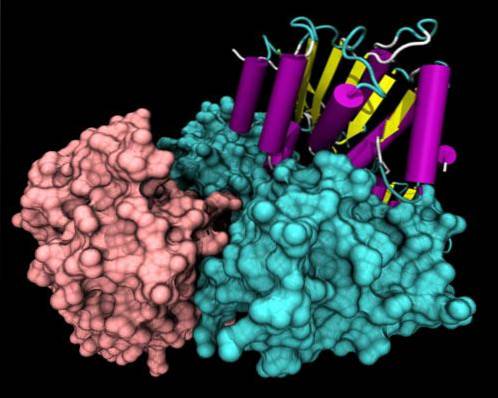
Strukturalnie wszystkie helikazy mają wysoce konserwatywne motywy sekwencji w przedniej części ich pierwotnej struktury. Część cząsteczki ma określony układ aminokwasów, który zależy od specyficznej funkcji każdej helikazy..
Najbardziej zbadane strukturalnie helikazy to helikazy z nadrodziny SF1. Wiadomo, że te białka są pogrupowane w 2 domeny bardzo podobne do wielofunkcyjnych białek RecA, a domeny te tworzą między nimi kieszeń wiążącą ATP..
Niekonserwowane regiony mogą przedstawiać specyficzne domeny typu rozpoznawanego przez DNA, domenę lokalizacji komórki i białko-białko..
funkcje
Helikaza DNA
Funkcje tych białek zależą od wielu różnych czynników, w tym stresu środowiskowego, linii komórkowej, podłoża genetycznego i etapów cyklu komórkowego..
Wiadomo, że helikazy DNA SF1 pełnią określone funkcje w naprawie, replikacji, transferze i rekombinacji DNA..
Oddzielają nici podwójnej helisy DNA i uczestniczą w utrzymaniu telomerów, naprawie pęknięć dwuniciowych i usuwaniu białek związanych z kwasami nukleinowymi.
Helikaza RNA
Jak już wspomniano, helikazy RNA są niezbędne w większości procesów metabolicznych RNA i wiadomo również, że białka te uczestniczą w wykrywaniu wirusowego RNA..
Ponadto działają w przeciwwirusowej odpowiedzi immunologicznej, ponieważ wykrywają obce RNA lub obce dla organizmu (u kręgowców).
Znaczenie medyczne
Helikazy pomagają komórkom przezwyciężyć stres endogenny i egzogenny, unikając niestabilności chromosomów i utrzymując równowagę komórkową.
Niepowodzenie tego systemu lub równowagi homeostatycznej jest związane z mutacjami genetycznymi, które obejmują geny kodujące białka typu helikazy; z tego powodu są przedmiotem badań biomedycznych i genetycznych.
Poniżej wymienimy niektóre z chorób związanych z mutacjami w genach kodujących DNA jako białka typu helikazy:
Zespół Wernera
Jest to choroba genetyczna spowodowana mutacją genu WRN, który koduje helikazę. Zmutowana helikaza nie działa prawidłowo i powoduje szereg chorób, które razem składają się na zespół Wernera.
Główną cechą osób cierpiących na tę patologię jest ich przedwczesne starzenie. Aby choroba się ujawniła, zmutowany gen musi być odziedziczony po obojgu rodzicach; częstość występowania jest bardzo niska i nie ma lekarstwa na jego wyleczenie.
Zespół Blooma
Zespół Blooma to choroba genetyczna wynikająca z mutacji autosomalnego genu zwanego BLM, który koduje białko helikazy. Występuje tylko dla osób homozygotycznych pod względem tego charakteru (recesywny).
Główną cechą tej rzadkiej choroby jest nadwrażliwość na światło słoneczne, które powoduje zmiany skórne w postaci rumieniowatej wysypki. Nie ma jeszcze lekarstwa.
Zespół Rothmunda-Thomsona
Jest również znany jako wrodzona zanikowa poikiloderma. Jest to patologia o bardzo rzadkim pochodzeniu genetycznym: do tej pory na całym świecie opisano mniej niż 300 przypadków.
Jest spowodowana mutacją w genie RECQ4, autosomalnym i recesywnym genie, który znajduje się na chromosomie 8.
Objawy lub stany tego zespołu obejmują młodzieńczą zaćmę, nieprawidłowości w układzie kostnym, depigmentację, rozszerzenie naczyń włosowatych i atrofię skóry (poikiloderma). W niektórych przypadkach może wystąpić nadczynność tarczycy i niedobór produkcji testosteronu..
Bibliografia
- R.M. Brosh (2013). Helikazy DNA zaangażowane w naprawę DNA i ich rola w nowotworach. Nature Reviews Cancer.
- Helicase. Odzyskany z nature.com.
- Helicase. Odzyskany z en.wikipedia.org.
- A. Juárez, L.P. Islas, A.M. Rivera, S.E. Tellez, M.A. Duran (2011). Zespół Rothmunda-Thompsona (wrodzona zanikowa poikiloderma) u kobiety w ciąży. Klinika i badania w ginekologii i położnictwie.
- K.D. Raney, A.K. Byrd, S. Aarattuthodiyil (2013). Struktura i mechanizmy helikaz DNA SF1. Postępy w medycynie eksperymentalnej i biologii.
- Zespół Blooma. Odzyskany z Medicina.ufm.edu.
- M. Singleton, M.S. Dillingham, D.B. Wigley (2007). Struktura i mechanizm helikaz i translokaz kwasów nukleinowych. Roczny przegląd biochemii.



Jeszcze bez komentarzy