
Charakterystyka, rodzaje i mechanizm uwodornienia katalitycznego
Plik uwodornienie katalityczne Jest to reakcja, w której wodór cząsteczkowy jest dodawany do związku z większą szybkością. Cząsteczka H.dwa Nie tylko musi najpierw zerwać wiązanie kowalencyjne, ale także, ponieważ jest tak małe, wydajne kolizje między nim a związkiem, do którego zostanie dodany, są mniej prawdopodobne..
Związek będący receptorem wodoru może być organiczny lub nieorganiczny. W związkach organicznych znajduje się większość przykładów uwodornienia katalitycznego; zwłaszcza te, które mają aktywność farmakologiczną lub które mają metale wbudowane w swoje struktury (związki metaloorganiczne).
Co się dzieje, gdy dodaje się H.dwa do struktury wypełnionej węglem? Zmniejsza się jego nienasycenie, to znaczy węgiel osiąga maksymalny stopień prostych wiązań, jakie może utworzyć.
Dlatego Hdwa jest dodawany do wiązań podwójnych (C = C) i potrójnych (C≡C); chociaż można go również dodać do grup karbonylowych (C = O).
Tak więc dodane alkeny i alkiny reagują przez katalityczne uwodornienie. Na podstawie powierzchownej analizy dowolnej struktury można przewidzieć, czy doda ona H.dwa po prostu wykrywając wiązania podwójne i potrójne.
Indeks artykułów
- 1 Charakterystyka uwodornienia katalitycznego
- 1.1 Zrywa się wiązanie wodorowe
- 1.2 Eksperymentalne
- 2 rodzaje
- 2.1 Jednorodne
- 2.2 Heterogeniczne
- 3 Mechanizm
- 4 Odnośniki
Charakterystyka uwodornienia katalitycznego
Na zdjęciu mechanizm tej reakcji. Jednak przed jego opisem konieczne jest odniesienie się do pewnych aspektów teoretycznych.
Powierzchnie szarawych kul reprezentują atomy metalu, które, jak widać, są katalizatorami uwodornienia par excellence..
Wiązanie wodorowe pęka
Po pierwsze uwodornienie jest reakcją egzotermiczną, to znaczy uwalnia ciepło w wyniku tworzenia się związków o niższej energii..
Wyjaśnia to stabilność utworzonych wiązań C-H, które wymagają więcej energii do ich późniejszego zerwania niż wymagana przez wiązanie H-H wodoru cząsteczkowego..
Z drugiej strony uwodornienie zawsze obejmuje najpierw zerwanie wiązania H-H. To pęknięcie może być homolityczne, jak to ma miejsce w wielu przypadkach:
H-H => H ∙ + ∙ H
Lub heterolityczny, który może wystąpić, na przykład, gdy tlenek cynku, ZnO, jest uwodorniony:
H-H => H+ + H.-
Zauważ, że różnica między dwoma przerwami polega na tym, jak rozmieszczone są elektrony w wiązaniu. Jeśli są rozłożone równomiernie (kowalencyjnie), każdy H kończy się na zachowaniu jednego elektronu; podczas gdy jeśli podział jest jonowy, kończy się bez elektronów, H.+, a druga wygrywa je całkowicie, H.-.
Oba pęknięcia są możliwe podczas katalitycznego uwodornienia, chociaż homolityczny pozwala ustąpić miejsca opracowaniu logicznego mechanizmu tego procesu..
Eksperymentalny
Wodór jest gazem, dlatego należy go barbotować i upewnić się, że tylko on dominuje na powierzchni cieczy..
Z drugiej strony uwodorniony związek musi być rozpuszczony w środowisku, czy to w wodzie, alkoholu, eterze, estrach lub ciekłej aminie; w przeciwnym razie uwodornianie przebiegałoby bardzo wolno.
Rozpuszczony związek, który ma być uwodorniony, musi być również katalizatorem w środowisku reakcji. Będzie to odpowiedzialne za przyspieszenie reakcji.
W uwodornieniu katalitycznym często stosuje się drobno rozdrobnione metale niklu, palladu, platyny lub rodu, które są nierozpuszczalne w prawie wszystkich rozpuszczalnikach organicznych. Dlatego będą dwie fazy: ciekła z rozpuszczonym związkiem i wodorem oraz stała, z katalizatorem..
Metale te zapewniają swoją powierzchnię do reakcji wodoru i związku, w taki sposób, że przyśpiesza się zrywanie wiązań..
Podobnie zmniejszają przestrzeń dyfuzyjną gatunku, zwiększając liczbę skutecznych zderzeń molekularnych. Nie tylko to, ale nawet reakcja zachodzi w porach metalu..
Rodzaje
Jednorodny
O homogenicznym uwodornieniu katalitycznym mówimy, gdy medium reakcyjne składa się z jednej fazy. Tutaj nie ma miejsca na stosowanie metali w ich czystym stanie, ponieważ są one nierozpuszczalne.
Zamiast tego stosuje się związki metaloorganiczne tych metali, które są rozpuszczalne i jak wykazano, mają wysokie wydajności..
Jednym z tych związków metaloorganicznych jest katalizator Wilkinsona: chlorek tris (trifenylofosfiny) rodu, [(C6H.5)3P]3RhCl. Związki te tworzą kompleks z Hdwa, aktywowanie go do późniejszej reakcji addycji do alkenu lub alkinu.
Homogeniczne uwodornianie ma znacznie więcej alternatyw niż heterogeniczne. Dlaczego? Ponieważ chemia jest związkami metaloorganicznymi jest obficie: wystarczy zmienić metal (Pt, Pd, Rh, Ni) i ligandy (cząsteczki organiczne lub nieorganiczne połączone z centrum metalu), aby uzyskać nowy katalizator.
Heterogeniczny
Heterogeniczne uwodornianie katalityczne, jak już wspomniano, ma dwie fazy: jedną ciecz i drugą stałą..
Oprócz katalizatorów metalicznych istnieją inne, które składają się ze stałej mieszaniny; na przykład katalizator Lindlara, który składa się z platyny, węglanu wapnia, octanu ołowiu i chinoliny.
Szczególną cechą katalizatora Lindlara jest to, że brakuje mu uwodornienia alkenów; Jest jednak bardzo przydatny do częściowego uwodornienia, to znaczy doskonale działa na alkinach:
RC≡CR + Hdwa => RHC = CHR
Mechanizm
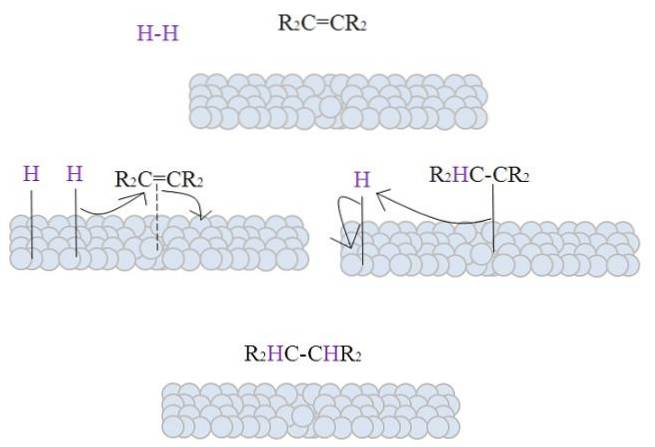
Zdjęcie przedstawia mechanizm katalitycznego uwodornienia przy użyciu sproszkowanego metalu jako katalizatora.
Szarawe kule odpowiadają metalicznej powierzchni, powiedzmy, platyny. Cząsteczka H.dwa (kolor fioletowy) zbliża się do powierzchni metalu, podobnie jak czteropodstawiony alken, R.dwaC = CRdwa.
Hdwa oddziałuje z elektronami, które podróżują przez atomy metalu i następuje zerwanie i utworzenie tymczasowego wiązania H-M, gdzie M jest metalem. Ten proces jest znany jako chemisorpcja; to znaczy adsorpcja przez siły chemiczne.
Alken oddziałuje w podobny sposób, ale wiązanie tworzy podwójne wiązanie (linia przerywana). Wiązanie H-H już się rozpadło i każdy atom wodoru pozostaje związany z metalem; w ten sam sposób robi to z centrami metalicznymi w katalizatorach metaloorganicznych, tworząc pośredni kompleks H-M-H.
Następnie następuje migracja H w kierunku wiązania podwójnego, która otwiera się tworząc wiązanie z metalem. Pozostały H wiąże się następnie z drugim węglem pierwotnego wiązania podwójnego, a wytworzony alkan, R, jest ostatecznie uwalniany.dwaHC-CHRdwa.
Mechanizm ten będzie powtarzany tyle razy, ile będzie to konieczne, aż wszystkie H.dwa w pełni zareagowały.
Bibliografia
- Graham Solomons T.W., Craig B. Fryhle. (2011). Chemia organiczna. Aminy. (10th wydanie.). Wiley plus.
- Carey F. (2008). Chemia organiczna. (Wydanie szóste). Mc Graw Hill.
- Shiver & Atkins. (2008). Chemia nieorganiczna. (Czwarta edycja). Mc Graw Hill.
- Lew J. (s.f.). Katalityczne uwodornianie alkenów. Chemia LibreTexts. Źródło: chem.libretexts.org
- Jones D. (2018). Co to jest uwodornienie katalityczne? - Mechanizm i reakcja. Nauka. Odzyskany z: study.com



Jeszcze bez komentarzy