
Charakterystyka, budowa, rodzaje, funkcje lipazy
Plik lipazy stanowią dużą rodzinę enzymów zdolnych do katalizowania hydrolizy wiązań estrowych obecnych w substratach, takich jak trójglicerydy, fosfolipidy, estry cholesterolu i niektóre witaminy.
Występują praktycznie we wszystkich królestwach życia, zarówno w mikroorganizmach, takich jak bakterie i drożdże, jak iu roślin i zwierząt; w każdym typie organizmu enzymy te mają szczególne właściwości i cechy, które odróżniają je od siebie.
W zależności od rodzaju klasyfikacji można dokonać rozróżnienia między „prawdziwymi” lipazami, znanymi również jako lipazy triacyloglicerolowe, a innymi enzymami o podobnej aktywności lipolitycznej, takimi jak fosfolipazy, esterazy sterolowe i esterazy palmitynianowe retinylu..
Pierwszym opublikowanym raportem o sekwencji enzymu lipazy był De Caro i wsp. W 1981 roku, który badał trzustkową lipazę triacyloglicerolową pochodzącą od świń. Późniejsze badania wykazały istnienie wielu innych ustrojowych lipaz w organizmach żywych..
Najważniejszymi lipazami u zwierząt są lipazy trawienne wytwarzane przez trzustkę i wątrobę, które uczestniczą w metabolizmie regularnie spożywanych w pożywieniu tłuszczów, a zatem mają ważne implikacje fizjologiczne z różnych punktów widzenia..
Obecnie enzymy te są badane nie tylko do celów klinicznych i / lub metabolicznych, ale są również produkowane przemysłowo do celów handlowych do przetwarzania żywności i innych produktów i można je uzyskać z hodowli specjalnych mikroorganizmów..
Indeks artykułów
- 1 Funkcje
- 1.1 Mechanizm katalityczny
- 1.2 Specyfika podłoża
- 2 Struktura
- 2.1 Ludzka lipaza trzustkowa
- 3 Funkcje
- 3.1 Funkcje przemysłowe
- 4 Odnośniki
Charakterystyka
Lipazy są białkami rozpuszczalnymi w wodzie i katalizują reakcje hydrolityczne na nierozpuszczalnych substratach. Występują w naturze w równowadze między ich aktywną i nieaktywną formą, a aktywacja lub inaktywacja zależy od różnych wewnętrznych czynników komórkowych..
Należą do nadrodziny enzymów hydrolaz z fałdami α / β, w której klasyfikowane są również esterazy, tioesterazy, niektóre proteazy i peroksydazy, dehalogenazy i inne hydrolazy wewnątrzkomórkowe..
Lipazy są kodowane przez geny należące do rodziny, która obejmuje geny kodujące lipazę trzustkową, lipazę wątrobową, lipazę lipoproteinową, lipazę śródbłonkową i fosfolipazę fosfatydyloseryny A1..
Mechanizm katalityczny
Niektórzy autorzy sugerują, że forma katalizy, którą mają te enzymy, jest analogiczna do tej, jaką mają proteazy serynowe, co jest związane z obecnością trzech specjalnych reszt aminokwasowych w miejscu aktywnym.
Mechanizm hydrolizy obejmuje tworzenie kompleksu enzym-substrat (lipaza: trójgliceryd), następnie tworzenie półacetalowego związku pośredniego, a następnie uwalnianie diacyloglicerydu i kwasu tłuszczowego..
Ostatni etap hydrolizy, uwolnienie kwasu tłuszczowego z miejsca aktywnego, zachodzi w modelu znanym jako model „katapulty”, co oznacza, że po rozszczepieniu lub rozpadzie wiązania estrowego kwas tłuszczowy jest szybko wyrzucany z strona katalityczna.
Specyfika podłoża
Lipazy mogą być specyficzne i rozróżniać substraty, takie jak triglicerydy, diacyloglicerydy, monoglicerydy i fosfolipidy. Niektóre są specyficzne pod względem kwasów tłuszczowych, to znaczy pod względem długości, stopnia nasycenia itp..
Mogą być również selektywne pod względem regionu, w którym katalizują hydrolizę, co oznacza, że mogą mieć specyficzność pozycyjną w odniesieniu do miejsca, w którym cząsteczki kwasu tłuszczowego wiążą się ze szkieletem glicerolu (na którymkolwiek z trzech atomów węgla)..
Struktura
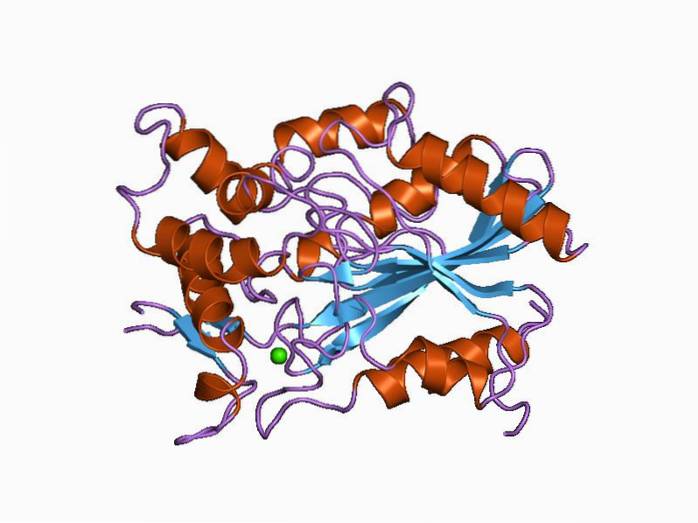
Podobnie jak inni członkowie rodziny enzymów, do której należą, lipazy charakteryzują się topologią złożoną z α-helis i β-fałdowanych arkuszy. Miejsce katalityczne tych enzymów na ogół składa się z triady aminokwasów: seryny, kwasu asparaginowego lub glutaminowego i histydyny..
Większość lipaz to glikoproteiny, które w zależności od wielkości części węglowodanowej mają masę cząsteczkową od 50 do 70 kDa..
Ludzka lipaza trzustkowa
Ma 449 reszt aminokwasowych i dwie oddzielne domeny: jedną N-końcową, w której znajduje się miejsce katalityczne i charakterystyczny fałd hydrolaz (α / β), oraz drugą C-końcową, mniejszą i uważaną za „pomocniczą”, z struktura zwana „kanapką β”.
Jego masa cząsteczkowa wynosi od 45 do 53 kDa, a aktywność katalityczna jest wyższa w temperaturach bliskich 37 ° C i przy pH między 6 a 10.
funkcje
W zależności od narządu, w którym znajdują się na przykład u ssaków, lipazy pełnią nieco inne funkcje fizjologiczne.
Jak wspomniano, specyficzne lipazy występują w trzustce, wątrobie, jajnikach i nadnerczach (w nerkach) oraz w tkankach śródbłonka..
Lipazy wątrobowe są odpowiedzialne za metabolizm cząstek lipoprotein, które są kompleksami tworzonymi przez lipidy i białka, które pełnią funkcję głównie w transporcie trójglicerydów i cholesterolu pomiędzy narządami i tkankami..
W szczególności lipazy uczestniczą w hydrolizie lub uwalnianiu kwasów tłuszczowych z cząsteczek triglicerydów zawartych w lipoproteinach. Jest to konieczne, aby wydobyć energię z tych cząsteczek lub poddać je recyklingowi, wykorzystując je jako prekursory w syntezie innych związków..
Lipazy śródbłonkowe są obecne w wątrobie, płucach, tarczycy i narządach rozrodczych, a ekspresja ich genów jest regulowana przez różne cytokiny. Enzymy te są również zaangażowane w metabolizm lipoprotein..
Funkcje przemysłowe
W mleczarskim przemyśle spożywczym powszechnie stosuje się lipazy do hydrolizy tłuszczów obecnych w mleku, co ma bezpośredni wpływ na „wzmocnienie” smaku serów, kremów i innych produktów mlecznych..
Są również wykorzystywane do produkcji innych produktów spożywczych, zwłaszcza podczas fermentacji, w celu polepszenia smaku i „strawności” niektórych potraw przygotowywanych przemysłowo..
Z dala od przemysłu spożywczego popularne jest stosowanie lipaz pochodzenia drobnoustrojowego w formułowaniu detergentów i ogólnych środków czyszczących, które zmniejszają szkodliwy wpływ na środowisko spowodowany ogromnym obciążeniem chemicznym obecnym w konwencjonalnych środkach czyszczących..
Bibliografia
- Lowe, M. E. (2002). Lipazy trójglicerydowe trzustki. Journal of Lipid Research, 43, 2007-2016.
- Mead, J. R., Irvine, S. A., & Ramji, D. P. (2002). Lipaza lipoproteinowa: budowa, funkcja, regulacja i rola w chorobie. J. Mol. Med., 80, 753-769.
- Perret, B., Mabile, L., Martinez, L., Tercé, F., Barbaras, R., & Collet, X. (2002). Lipaza wątrobowa: związek struktura / funkcja, synteza i regulacja. Journal of Lipid Research, 43, 1163-1169.
- Santamarina-fojo, S., González-navarro, H., Freeman, L., Wagner, E., Santamarina-fojo, S., Gonza, H.,… Nong, Z. (2004). Lipaza wątrobowa, metabolizm lipoprotein i miażdżyca. Arterioskleroza, zakrzepica i biologia naczyniowa, 24, 1750-1754.
- Taylor, P., Kurtovic, I., Marshall, S. N., Zhao, X., Simpson, B. K., Kurtovic, I.,… Zhao, X. I. N. (2012). Lipazy od ssaków i ryb. Recenzje w Fisheries Science, 29, 37-41.



Jeszcze bez komentarzy