
Budowa, funkcja i tworzenie miceli
Plik micele Są stabilnymi strukturami kulistymi złożonymi z setek cząsteczek amfipatycznych, to znaczy cząsteczek charakteryzujących się regionem polarnym (hydrofilowym) i niepolarnym (hydrofobowym). Podobnie jak cząsteczki, które je tworzą, micele mają silnie hydrofobowy środek, a ich powierzchnia jest „wyłożona” hydrofilowymi grupami polarnymi..
Wynikają one w większości przypadków z mieszaniny grupy cząsteczek amfipatycznych z wodą, więc jest to sposób na „stabilizację” hydrofobowych regionów wielu cząsteczek razem, co jest spowodowane efektem hydrofobowym i zorganizowanym przez van der Siły Waalsa.
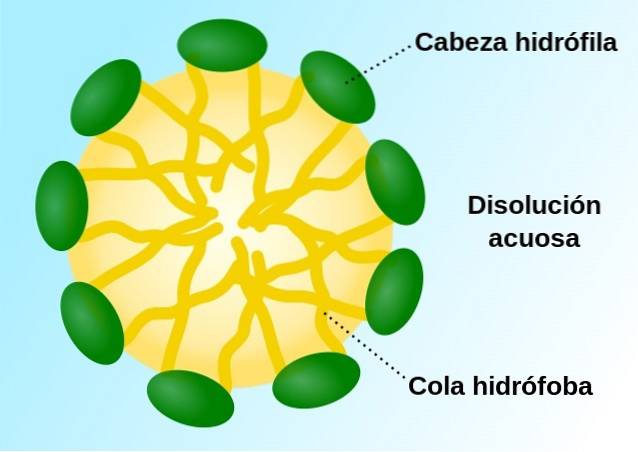
Zarówno detergenty, jak i mydła, a także niektóre lipidy komórkowe mogą tworzyć micele, które mają znaczenie funkcjonalne, przynajmniej u zwierząt, z punktu widzenia wchłaniania tłuszczu i transportu substancji rozpuszczalnych w tłuszczach..
Fosfolipidy, jedna z najliczniejszych i najważniejszych klas lipidów dla żywych komórek, w pewnych warunkach mogą tworzyć, oprócz liposomów i dwuwarstw, struktury micelarne.
Micele mogą również powstawać w ośrodku niepolarnym iw tym przypadku nazywane są „odwróconymi micelami”, ponieważ obszary polarne tworzących je cząsteczek amfipatycznych są „ukryte” w centrum hydrofilowym, podczas gdy części niepolarne są w bezpośrednim kontakcie z medium, które je zawiera.
Indeks artykułów
- 1 Struktura
- 1.1 Organizacja
- 2 Funkcja
- 3 Szkolenie
- 4 Odnośniki
Struktura
Micele składają się z cząsteczek amfipatycznych lub, innymi słowy, cząsteczek, które mają region hydrofilowy (podobny do wody, polarny) i inny region hydrofobowy (hydrofobowy, niepolarny).
Te cząsteczki obejmują na przykład kwasy tłuszczowe, cząsteczki dowolnego detergentu i fosfolipidy błon komórkowych.
W kontekście komórkowym micela jest zwykle zbudowana z kwasów tłuszczowych (o zmiennej długości), których polarne grupy karboksylowe są wystawione na powierzchnię agregatu, podczas gdy łańcuchy węglowodorowe są „ukryte” w hydrofobowym centrum, przyjmując w ten sposób bardziej lub mniej kulista struktura.
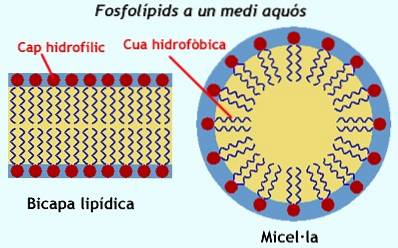
Fosfolipidy, które są innymi amfipatycznymi cząsteczkami o wielkim znaczeniu dla komórek, są na ogół niezdolne do tworzenia miceli, ponieważ dwa łańcuchy kwasów tłuszczowych, które tworzą ich „hydrofobowe ogony”, zajmują duże rozmiary i utrudniają pakowanie dowolnego kształtu..
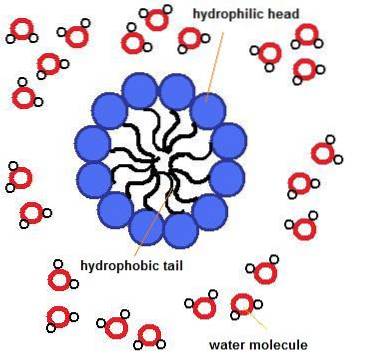
Zamiast tego, gdy te cząsteczki znajdują się w środowisku wodnym, „zagnieżdżają się” w dwuwarstwach (podobnie jak kanapka); to znaczy w bardziej płaskich strukturach, gdzie każda z „powierzchni” wystawionych na działanie ośrodka składa się z polarnych głów grup przyłączonych do glicerolu, a „wypełnienie” kanapki składa się z hydrofobowych ogonów (kwasy tłuszczowe zestryfikowane do pozostałe dwa węgle szkieletu glicerolowego).
Jedynym sposobem, w jaki fosfolipid może uczestniczyć w tworzeniu miceli, jest usunięcie jednego z jego dwóch łańcuchów kwasów tłuszczowych przez hydrolizę..
Organizacja
W miceli, jak wspomniano, „centrum” oddziela niepolarne części cząsteczek, z których się składają, i izoluje je od wody..
Centralny region miceli składa się zatem z wysoce nieuporządkowanego środowiska o właściwościach przypominających płyn, w którym pomiar promienia jest od 10 do 30% mniejszy niż w przypadku w pełni rozciągniętych łańcuchów cząsteczek nieamfipatycznych. Związanych z kompleksem molekularnym.
Podobnie powierzchnia miceli nie jest jednorodna, ale raczej „szorstka” i niejednorodna, z czego niektóre badania magnetycznego rezonansu jądrowego wskazują, że tylko jedna trzecia jest pokryta polarnymi częściami składowych monomerów..
Funkcjonować
Micele pełnią bardzo ważne funkcje, zarówno w przyrodzie, jak iw przemyśle i badaniach.
Jeśli chodzi o ich funkcje w przyrodzie, te agregaty molekularne są szczególnie ważne dla wchłaniania tłuszczów (monoglicerydów i kwasów tłuszczowych) z jelit, ponieważ micele o różnej wielkości i składzie mogą powstawać z cząsteczek tłuszczowych wchłanianych z pożywieniem i transportować je do wnętrza komórek błony śluzowej jelit, umożliwiając ich wchłanianie.
Micele działają również w transporcie cholesterolu (inna klasa lipidów komórkowych) nabytego z pożywieniem oraz niektórych witamin zwanych „rozpuszczalnymi w tłuszczach”, dlatego też są wykorzystywane farmakologicznie do transportu i podawania leków o właściwościach niepolarnych..
Detergenty i mydła używane codziennie do higieny osobistej lub do czyszczenia różnego rodzaju powierzchni składają się z cząsteczek lipidów zdolnych do tworzenia miceli, gdy znajdują się w roztworze wodnym..
Te micele zachowują się jak małe kulki w łożysku, nadając roztworom mydła ich śliską konsystencję i właściwości smarne. Działanie większości detergentów w dużym stopniu zależy od ich zdolności do wytwarzania miceli..
W badaniach i badaniach białek błonowych, na przykład, detergenty są używane do „oczyszczania” lizatów komórkowych z lipidów, które tworzą charakterystyczne dwuwarstwy błon, a także do oddzielania integralnych białek błonowych od hydrofobowych składników..
Trening
Aby zrozumieć tworzenie się struktur micelarnych, zwłaszcza w detergentach, należy wziąć pod uwagę nieco abstrakcyjną koncepcję: krytyczne stężenie micelarne lub CMC..
Krytyczne stężenie micelarne to takie stężenie amfipatycznych cząsteczek, przy którym micele zaczynają się tworzyć. Jest to wartość odniesienia, powyżej której wzrost stężenia tych cząsteczek zakończy się jedynie wzrostem liczby miceli, poniżej której są one preferencyjnie zorganizowane w warstwach na powierzchni zawierającego je środowiska wodnego..
Zatem tworzenie miceli jest bezpośrednią konsekwencją „amfifilowości” środków powierzchniowo czynnych i jest silnie zależne od ich właściwości strukturalnych, zwłaszcza od zależności kształtu i wielkości między grupami polarnymi i niepolarnymi..
W tym sensie tworzenie miceli jest korzystne, gdy pole przekroju poprzecznego grupy polarnej jest znacznie większe niż grupy niepolarnej, jak ma to miejsce w przypadku wolnych kwasów tłuszczowych, lizofosfolipidów i detergentów, takich jak dodecylosiarczan sodu ( SDS).
Dwa inne parametry, od których zależy tworzenie miceli, to:
- Temperatura: Zdefiniowano również krytyczną temperaturę micelarną (CMT). krytyczna temperatura micelarna), która jest temperaturą, powyżej której korzystne jest tworzenie się miceli
- Siła jonowa: dotyczy przede wszystkim detergentów typu jonowego lub środków powierzchniowo czynnych (których grupa polarna ma ładunek)
Bibliografia
- Hassan, P. A., Verma, G. i Ganguly, R. (2011). 1 Miękkie materiały - Właściwości i zastosowania. Materiały funkcjonalne: przygotowanie, przetwarzanie i zastosowania, 1.
- Lodish, H., Berk, A., Kaiser, C. A., Krieger, M., Scott, M. P., Bretscher, A.,… & Matsudaira, P. (2008). Biologia komórki molekularnej. Macmillan.
- Luckey, M. (2014). Biologia strukturalna błony: na podstawach biochemicznych i biofizycznych. Cambridge University Press.
- Nelson, D. L. i Cox, M. M. (2009). Zasady Lehningera biochemii (str. 71–85). Nowy Jork: WH Freeman.
- Tanford, C. (1972). Kształt i rozmiar miceli. The Journal of Physical Chemistry, 76 (21), 3020-3024.
- Zhang, Y., Cao, Y., Luo, S., Mukerabigwi, J. F. i Liu, M. (2016). Nanocząsteczki jako systemy dostarczania leków w terapii skojarzonej raka. W Nanobiomaterials in Cancer Therapy (str. 253-280). Wydawnictwo William Andrew.


Jeszcze bez komentarzy