
Struktura, właściwości, zastosowania, zagrożenia azotynem sodu (NaNO2)

Plik azotan sodu jest krystaliczną nieorganiczną substancją stałą utworzoną przez jon sodu Na+ i jon azotynowy NOdwa-. Jego wzór chemiczny to NaNOdwa. Jest to biała krystaliczna substancja stała, która ma tendencję do pochłaniania wody z otoczenia, czyli jest higroskopijna.
W obecności powietrza powoli utlenia się do azotanu sodu NaNO3. Posiada właściwości utleniające (utlenia inne związki), a także redukujące (utlenia się innymi związkami).

Występuje naturalnie w organizmie człowieka i jest stosowany jako środek konserwujący wędliny i ryby wędzone, ponieważ zapobiega rozwojowi szkodliwych mikroorganizmów.
Ma ważne zastosowanie w doraźnym leczeniu zatrucia cyjankami, ponieważ zmniejsza toksyczne i śmiertelne działanie tego związku. Jednak należy go podawać z dużą ostrożnością i nie we wszystkich przypadkach działa.
Stwierdzono, że może zapobiegać infekcjom oczu spowodowanym zanieczyszczeniem soczewek kontaktowych przez mikroorganizmy. Niektóre badania wskazują, że jego spożycie z pożywieniem może powodować raka, ale szacuje się, że można tego uniknąć, spożywając witaminę C z takimi pokarmami.
Indeks artykułów
- 1 Struktura
- 2 Nazewnictwo
- 3 Właściwości
- 3.1 Stan fizyczny
- 3.2 Masa cząsteczkowa
- 3.3 Temperatura topnienia
- 3.4 Temperatura wrzenia
- 3.5 Gęstość
- 3.6 Rozpuszczalność
- 3,7 pH
- 3.8 Inne właściwości
- 4 Otrzymywanie
- 4.1 Obecność w ciele
- 5 zastosowań
- 5.1 W przemyśle spożywczym
- 5.2 Jako pomoc doraźna w przypadku zatrucia cyjankami
- 5.3 Do rozszerzania naczyń krwionośnych
- 5.4 Przeciw niektórym pasożytom
- 5.5 Aby uniknąć uszkodzenia narządów
- 5.6 Unikanie infekcji spowodowanych noszeniem soczewek kontaktowych
- 5.7 Do różnych zastosowań
- 6 Zagrożenia lub niedogodności
- 7 Referencje
Struktura
Azotyn sodu składa się z kationu sodu Na+ i anion azotynowy NOdwa-.
W anionie azotynowym NOdwa- azot ma wartościowość +3, a tlen -2, z tego powodu anion ma jeden globalny ładunek ujemny.
Anion azotynowy NIEdwa- ma strukturę kątową, to znaczy wiązania azotu (N) z atomami tlenu (O) tworzą kąt.
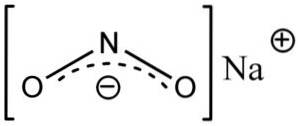
Nomenklatura
- Azotan sodu
- Azotan sodu
- Sól sodowa kwasu azotowego.
Nieruchomości
Stan fizyczny
Żółtawo-białe krystaliczne ciało stałe. Kryształy rombowe.
Waga molekularna
68,995 g / mol
Temperatura topnienia
271 ºC
Temperatura wrzenia
Nie gotuje się. Rozkłada się powyżej 320 ºC
Gęstość
2,17 g / cm3 przy 20 ºC
Rozpuszczalność
Rozpuszczalny w wodzie: 84,8 g / 100 g wody o temperaturze 25 ºC. Słabo rozpuszczalny w etanolu. Umiarkowanie rozpuszczalny w metanolu. Trudno rozpuszczalny w eterze dietylowym.
pH
Jego wodne roztwory są alkaliczne, o pH około 9. Dzieje się tak, ponieważ kwas azotawy jest słabym kwasem, który nie dysocjuje, więc jon NOdwa- spróbuj wziąć proton H.+ wody do utworzenia HNOdwa, co prowadzi do powstania jonów OH- które wytwarzają zasadowość.
NIEdwa- + H.dwaO → HNOdwa + O-
Inne właściwości
Azotyn sodu NaNOdwa w obecności powietrza powoli utlenia się do azotanu sodu NaNO3. Jest higroskopijnym ciałem stałym, gdyż pochłania wodę z otoczenia.
Posiada właściwości utleniające (może utleniać inne związki), a także właściwości redukujące (może być utleniany przez inne związki).
Jeśli wejdzie w kontakt z materiałami, takimi jak drewno, papier lub tekstylia, może spowodować ich niebezpieczne zapalenie..
W przypadku kwasów następuje jego rozkład, w wyniku czego powstaje mieszanina brązowych toksycznych gazów tlenków azotu (NOx).
Otrzymywanie
Można go uzyskać przez ogrzewanie azotanu sodu NaNO3 z ołowiem Pb:
Starszy brat3 + Pb → NaNOdwa + PbO
Obecność w ciele
Anion azotynowy występuje naturalnie we krwi i tkankach, ponieważ powstaje w wyniku utleniania NO..
Aplikacje
W przemyśle spożywczym
Służy do marynowania mięs, ponieważ działa jako środek utrwalający kolor i smak oraz jako środek konserwujący, ponieważ kontroluje rozwój mikroorganizmów, w szczególności zapobiegając rozwojowi Clostridium botulinum wywołując zatrucie jadem kiełbasianym.
Azotyn sodu w mięsie reaguje z hemoglobiną zawartą w krwinkach czerwonych lub krwinkach czerwonych w tym pożywieniu. Stosowany również do peklowanych wędzonych ryb.

Jako pomoc w nagłych przypadkach zatrucia cyjankiem
Azotyn sodu jest stosowany w leczeniu ostrego zatrucia cyjankiem. To antidotum na ten poważny problem.
Jego działanie wynika z faktu, że sprzyja tworzeniu się we krwi methemoglobiny (rodzaj hemoglobiny), która zatrzymuje jony cyjanku i nie uwalnia ich, a tym samym zapobiega ich uwalnianiu do komórek, czyniąc je mniej toksycznymi.
W przypadku zatrucia cyjankiem dożylnie podaje się azotyn sodu, w ciągu około 12 minut wytworzy się methemoglobina. Pomimo tego opóźnienia zapewnia również ochronę ze względu na działanie rozszerzające naczynia krwionośne..
Do rozszerzania naczyń krwionośnych
Jest stosowany w leczeniu tętniczego nadciśnienia płucnego, ponieważ działa rozszerzając naczynia krwionośne, obniżając w ten sposób ciśnienie krwi. Szacuje się, że efekt ten wynika z faktu, że przekształca się on w tlenek azotu NO, który działa rozluźniająco na mięśnie miękkie.
Jednak przyczyny jego skuteczności są nadal badane..
Przeciw niektórym pasożytom
Niektórzy badacze odkryli, że azotyn sodu hamuje wzrost i namnażanie się pasożyta jelitowego Blastocystis hominis nawet jeśli jest oporny na inne leki.
Znaleziono NaNOdwa generuje śmierć tego pasożyta przez apoptozę, która jest rodzajem samobójstwa komórki pasożyta. Azotyn sodu powoduje, że komórki jelitowe wytwarzają NO, co wydaje się być ważne w tym procesie.
Aby uniknąć uszkodzenia narządów
Według niektórych badań azotyn jest silnym inhibitorem uszkodzeń serca i wątroby w procesach niedokrwiennych (zmniejszony przepływ krwi w części ciała). Uważa się, że jest to spowodowane faktem, że jest to biologiczna rezerwa NO.
Stwierdzono, że można go stosować do zapobiegania uszkodzeniom narządów po przywróceniu przepływu krwi, który został przerwany przez zawał serca, operację brzucha wysokiego ryzyka lub przeszczep narządu..
Aby uniknąć infekcji spowodowanych noszeniem soczewek kontaktowych
Znaleziono NaNOdwa zapobiega tworzeniu się warstw mikroorganizmów chorobotwórczych Staphylococcus aureus Y Pseudomonas aeruginosa o soczewkach kontaktowych.

W różnych zastosowaniach
Azotyn sodu jest używany do produkcji barwników, leków i różnych związków organicznych.
Służy również jako inhibitor korozji w smarach uniwersalnych.
Ryzyko lub niedogodności
Jednym z problemów związanych ze stosowaniem azotynu sodu do zatruć cyjankami jest to, że powoduje on poważne zaburzenia sercowo-naczyniowe u dzieci..
Niezalecany dla ofiar pożaru, gdzie występuje jednoczesna ekspozycja na cyjanek i tlenek węgla (CO). CO zmniejsza zdolność krwi do przenoszenia tlenu, więc podawanie NaNOdwa pogorszy stan niskiego poziomu tlenu we krwi pacjenta.
Wziewny azotyn sodu jest drażniący i toksyczny, może uszkodzić układ sercowo-naczyniowy i ośrodkowy układ nerwowy. Ponadto jest szkodliwy dla środowiska.
Azotyn sodu spożywany z pożywieniem może być szkodliwy. Azotyn po dotarciu do żołądka reaguje z określonymi związkami tworząc nitrozoaminy, które mogą powodować raka.
Reakcji tych można uniknąć w obecności witaminy C..
Według niektórych konsultowanych źródeł ryzyko spożycia azotynów z wędlinami lub rybami jest minimalne, ponieważ azotyn jest naturalnie obecny w ślinie.
Źródła wskazują, że to ryzyko jest również minimalne w porównaniu z ogromnymi korzyściami płynącymi ze spożywania żywności wolnej od szkodliwych mikroorganizmów.
Bibliografia
- Bhattacharya, R. i Flora, S.J.S. (2015). Toksyczność cyjankowa i jej leczenie. W Handbook of Toxicology of Chemical Warfare Agents (wydanie drugie). Odzyskany z sciencedirect.com.
- NAS. National Library of Medicine. (2019). Azotan sodu. Odzyskany z: pubchem.ncbi.nlm.nih.gov.
- Kim, D.J. et al. (2017). Skuteczność antybiofilmu tlenku azotu na miękkich soczewkach kontaktowych. BMC Ophthalmol 17, 206 (2017). Odzyskany z bmcophthalmol.biomedcentral.com.
- Ramis-Ramos, G. (2003). Przeciwutleniacze. Syntetyczne przeciwutleniacze. W Encyklopedii Nauk o Żywności i Żywieniu (drugie wydanie). Odzyskany z sciencedirect.
- Barozzi Seabra, A. i Durán, N. (2017). Dawcy tlenku azotu do leczenia chorób zaniedbanych. W przypadku dawców tlenku azotu. Odzyskany z sciencedirect.com.
- Duranski, M.R. et al. (2005). Cytoprotekcyjne działanie azotynów podczas niedokrwienia - reperfuzji serca i wątroby in vivo. J Clin Invest 2005; 115 (5): 1232-1240. Odzyskany z ncbi.nlm.nih.gov.
- Cotton, F. Albert i Wilkinson, Geoffrey. (1980). Zaawansowana chemia nieorganiczna. Czwarta edycja. John Wiley & Sons.



Jeszcze bez komentarzy