
Charakterystyka, budowa i krzywa wiązania oksyhemoglobiny
LUBksihemoglobina Jest to nazwa, którą otrzymuje hemoglobina, gdy wiąże się z tlenem. Hemoglobina to białko występujące w krwinkach czerwonych, którego główną funkcją jest transport tlenu z płuc do tkanek..
Pierwsze żywe istoty były jednokomórkowe i żyły w płynnym środowisku, z którego były odżywiane iz którego eliminowały swoje odchody, podobnie jak niektóre organizmy istniejące dzisiaj. W tych warunkach procesy te zachodzą dzięki prostym mechanizmom dyfuzji, ponieważ ściana komórkowa jest w bliskim kontakcie z dostarczającym ją medium..
Rozwój coraz bardziej złożonych organizmów wielokomórkowych oznaczał, że komórki wewnętrzne znacznie odsunęły się od środowiska, przez co mechanizmy dyfuzji jako jedyne źródło zaopatrzenia stały się niewystarczające..
W związku z tym opracowano wyspecjalizowane systemy do pozyskiwania składników odżywczych i gazów, takich jak układ pokarmowy i układ oddechowy, a także mechanizmy transportu, które doprowadzają te składniki odżywcze i gazy bliżej komórki: układ sercowo-naczyniowy.
Do produkcji energii w postaci cząsteczek ATP komórki potrzebują tlenu. Ponieważ ATP nie może być magazynowany, musi być stale syntetyzowany, co oznacza stałe zapotrzebowanie komórek na tlen..
Hemoglobina wyłoniła się, mówiąc ewolucyjnie, jako transporter gazu, który „rozwiązał” problem transportu tlenu ze środowiska do komórki..
Indeks artykułów
- 1 Charakterystyka i struktura
- 1.1 Do czego służy hemoglobina?
- 1.2 Jak wygląda cząsteczka hemoglobiny?
- 1.3 Jak jest grupa hemu?
- 1.4 Jak powstaje oksyhemoglobina?
- 1.5 Jaka jest maksymalna ilość tlenu, jaką może przenosić hemoglobina?
- 2 Krzywa wiązania oksyhemoglobiny
- 3 Odnośniki
Charakterystyka i struktura
Aby mówić o właściwościach i budowie oksyhemoglobiny, konieczne jest odniesienie się do hemoglobiny, ponieważ oksyhemoglobina to nic innego jak hemoglobina związana z tlenem. Dlatego od teraz łączne właściwości cząsteczki będą opisywane w obecności danego gazu lub bez..
Do czego służy hemoglobina?
Hemoglobina jest niezbędna do transportu tlenu do tkanek w ilości i szybkości, jaką gwarantują, biorąc pod uwagę, że tlen ma tak małą rozpuszczalność we krwi, że jego transport przez dyfuzję byłby niewystarczający do zaspokojenia potrzeb tkanek.
Jaka jest cząsteczka hemoglobiny?
Hemoglobina jest białkiem tetramerycznym (które ma cztery podjednostki), ma kulisty kształt i masę cząsteczkową 64 kDa.
Jego cztery podjednostki stanowią pojedynczą jednostkę funkcjonalną, w której każda z nich wpływa na siebie wzajemnie. Każda podjednostka składa się z łańcucha polipeptydowego, globiny i grupy prostetycznej, grupy hemu lub „hemu”, która działa jako kofaktor i nie jest zbudowana z aminokwasów; to znaczy, że nie ma natury białkowej.
Globina występuje w dwóch formach: alfa-globina i beta-globina. Tetramer hemoglobiny składa się z pary łańcuchów alfa globiny (ze 141 aminokwasów) i pary łańcuchów beta globiny (ze 146 aminokwasów).
Każdy z czterech łańcuchów polipeptydowych jest przyłączony do grupy hemu, która ma atom żelaza w środku w stanie żelazawym (Fe2 +).
Jak tam grupa hemu?
Grupa hemowa to pierścień porfirynowy, który składa się z czterech pierścieni pirolowych (heterocyklicznych związków aromatycznych o wzorze C4H5N) połączonych mostkami metylowymi. Żelazo w stanie żelaznym, które znajduje się w środku, jest połączone ze strukturą za pomocą skoordynowanych wiązań azotowych.
Każda grupa hemu może wiązać się z jedną cząsteczką tlenu, więc każda cząsteczka hemoglobiny może wiązać tylko 4 cząsteczki gazu.
Ciało ludzkie zawiera około 2,5 x 1013 erytrocytów, które są komórkami krwi, które wytwarzają i transportują hemoglobinę. Każdy erytrocyt ma około 280 milionów cząsteczek hemoglobiny, a następnie może przenosić ponad 1 miliard cząsteczek tlenu.
Jak powstaje oksyhemoglobina?
Oksyhemoglobina powstaje po połączeniu atomu tlenu z każdym atomem żelaza w stanie żelazawym znajdującym się w każdej grupie hemowej cząsteczki hemoglobiny.
Termin oksyhemoglobina odnosi się zatem do utlenionej, a nie utlenionej chemicznie hemoglobiny, ponieważ nie traci ona elektronu, gdy łączy się z tlenem, a żelazo pozostaje w stanie żelazawym..
Natlenianie powoduje zmianę czwartorzędowej struktury cząsteczki, to znaczy zmianę konformacji, która może być przenoszona z łańcuchów globiny do grupy hemu i odwrotnie..
Jaka jest maksymalna ilość tlenu, jaką może przenosić hemoglobina?
Hemoglobina może co najwyżej związać w swojej strukturze cztery cząsteczki tlenu. Jeśli objętość molowa gazów doskonałych wynosi 22,4 l / mol, jeden mol hemoglobiny (64 500 g) wiąże się z 89,6 litrami tlenu (4 mole O2 x 22,4 l / mol).
Tak więc każdy gram hemoglobiny musi wiązać 1,39 ml O2, aby był w 100% nasycony (89,6 l / 64500 g x (1000 ml / l)).
W praktyce badania krwi dają nieco niższe wyniki, ponieważ istnieją niewielkie ilości methemoglobiny (utlenionej hemoglobiny) i karboksyhemoglobiny (hemoglobina + tlenek węgla (CO)), które nie mogą wiązać tlenu.
Biorąc to pod uwagę, reguła „Hüfnera” określa, że 1g hemoglobiny we krwi ma maksymalną zdolność wiązania tlenu wynoszącą 1,34 ml..
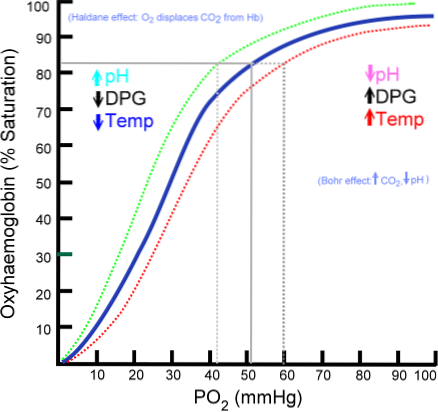
Krzywa wiązania oksyhemoglobiny
Liczba cząsteczek tlenu, które mogą związać się z cząsteczką hemoglobiny, zależy od ciśnienia parcjalnego tlenu lub PO2. W przypadku braku tlenu hemoglobina jest odtleniona, ale wraz ze wzrostem PO2 wzrasta liczba tlenów, które wiążą się z hemoglobiną..
Proces wiązania tlenu z hemoglobiną zależny od ciśnienia parcjalnego tlenu. Na wykresie wynik nazywany jest „krzywą oksyhemoglobiny” i ma charakterystyczny kształt „S” lub esicy..
W zależności od PO2, hemoglobina będzie mniej lub bardziej zdolna do „uwalniania” lub „dostarczania” tlenu, który niesie, jak również do bycia nim obciążonym..
Na przykład w obszarze między 10 a 60 mmHg ciśnienia uzyskuje się najbardziej stromą część krzywej. W tym stanie hemoglobina może łatwo oddać duże ilości O2. To jest stan, który osiąga się w tkankach.
Kiedy PO2 wynosi od 90 do 100 mmHg (12 do 13 kPa), hemoglobina jest prawie w 100% nasycona O2; a gdy tętnicze PO2 wynosi 60 mmHg (8 kPa), nasycenie O2 jest nadal tak wysokie, jak 90%.
W płucach panują takie warunki (ciśnienie między 60 a 100 mmHg) i to właśnie one pozwalają na naładowanie tlenem cząsteczek hemoglobiny obecnych w erytrocytach..
Ten esowaty kształt, który rysuje krzywą oksyhemoglobiny, zapewnia, że białko to zachowuje się jak doskonały ładowacz płuc, bardzo wydajny transporter w krwi tętniczej i doskonały dawca O2 w tkankach, proporcjonalnie do lokalnego tempa metabolizmu, czyli na żądanie.
Bibliografia
- Fox, S. I. (2006). Human Physiology 9th Edition (str. 501-502). McGraw-Hill Press, Nowy Jork, USA.
- Murray, R. K., Granner, D. K., Mayes, P. A. i Rodwell, V. W. (2014). Ilustrowana biochemia Harpera. McGraw-Hill.
- Rawn, J. D. (1998). Biochemia (1989). Burlington, Karolina Północna: Neil Patterson Publishers (c) N. Lalioti, CP Raptopoulou, A. Terzis, A. Panagiotopoulos, SP Perlepes, E. Manessi-Zoupa, J. Chem. Soc. Dalton Trans, 1327.
- Robert M. Berne, Matthew N. Levy. (2001) Fizjologia. (Wydanie 3) Ediciones Harcourt, S.A.
- Zachód, J. B. (1991). Fizjologiczne podstawy praktyki lekarskiej. Williams & Wilkins


Jeszcze bez komentarzy