
Struktura, właściwości, synteza i zastosowania glikolu propylenowego

Plik glikol propylenowy jest alkoholem, którego wzór chemiczny to C3H.8LUBdwa lub CH3CHOHCHdwaO. Składa się z bezbarwnej, bezwonnej, bez smaku, lepkiej cieczy, podobnej do syropu. Posiada świetną rozpuszczalność w wodzie, dzięki czemu ma właściwości higroskopijne i nawilżające.
Ponadto glikol propylenowy jest związkiem stosunkowo stabilnym i obojętnym chemicznie, co pozwoliło na jego stosowanie jako rozcieńczalnika przy dożylnym podawaniu wielu leków oraz w miejscowym i doustnym leczeniu różnych chorób, np. Rybiej łuski..

Jego wzór strukturalny pokazano powyżej, co pozwala na jasny obraz tego, jaka powinna być jego cząsteczka. Należy zauważyć, że ma dwie grupy hydroksylowe na sąsiednich atomach węgla i że jego szkielet węglowy pochodzi z propanu węglowodorowego; to znaczy ma trzy atomy węgla.
Inne nazwy tego alkoholu to 1,2-propanodiol (zalecany przez IUPAC) i 1,2-dihydroksypropan, poza niektórymi niezbyt powszechnymi.
Glikol propylenowy jest stosowany przemysłowo do produkcji różnych potraw i napojów, pełniąc funkcje środka utrzymującego wilgoć, stabilizatora, przeciwutleniacza, przeciwbakteryjnego, wzmacniającego działanie innych dodatków itp..
W przemyśle znajduje szerokie zastosowanie m.in .: przeciw zamarzaniu, rozpuszczalnik, produkcja żywic i tworzyw sztucznych, tkanin poliestrowych, barwników i barwników.
Chociaż jest uważany za bezpieczny związek, w pewnych warunkach może być toksyczny i szkodliwy dla zdrowia, co może prowadzić do zatrzymania akcji serca. Jest jednak bardziej przyjazny dla środowiska w porównaniu z glikolem etylenowym, zastępując ten ostatni jako płyn przeciw zamarzaniu samochodu..
Indeks artykułów
- 1 Struktura glikolu propylenowego
- 1.1 Stereoizomery
- 2 Właściwości
- 2.1 Nazwy chemiczne
- 2.2 Masa cząsteczkowa
- 2.3 Temperatura topnienia
- 2.4 Temperatura wrzenia
- 2.5 Temperatura zapłonu
- 2.6 Rozpuszczalność w wodzie
- 2.7 Rozpuszczalność w cieczach organicznych
- 2.8 Gęstość
- 2.9 Gęstość par
- 2.10 Prężność par
- 2.11 Stabilność
- 2.12 Lepkość
- 2.13 Ciepło spalania
- 2.14 Ciepło parowania
- 2.15 Ciepło właściwe
- 2.16 Ciepło formowania
- 2.17 Współczynnik załamania światła
- 2,18 pKa
- 3 Synteza
- 3.1 Z tlenku propylenu
- 3.2 Z glicerolu
- 4 Ryzyka
- 5 zastosowań
- 5.1 -Lekarze
- 5.2 -Przemysłowe
- 5.3 - Dodatkowe zastosowania
- 6 Odnośniki
Struktura glikolu propylenowego
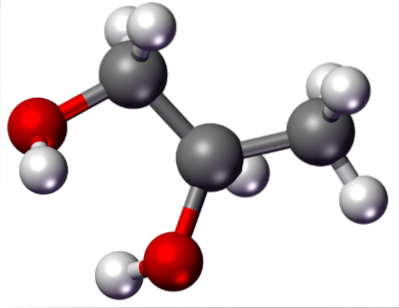
Na pierwszym zdjęciu pokazano wzór strukturalny glikolu propylenowego; Powyżej, zamiast tego, masz jego strukturę molekularną reprezentowaną przez model sfer i prętów. Czerwone kule odpowiadają atomom tlenu dwóch grup OH.
Wszystkie wiązania, które można zaobserwować w strukturze mają zdolność obracania się wokół własnej osi, co nadaje cząsteczce elastyczność; z kolei wpływa na ich tryby wibracyjne.
Z punktu widzenia ich oddziaływań międzycząsteczkowych, dzięki dwóm OH znajdującym się tak blisko siebie, pozwalają glikolowi propylenowemu na utworzenie kilku wiązań wodorowych. Konsekwencją tych mostków jest to, że alkohol ten ma wyższą temperaturę wrzenia niż woda (187,6 ° C), mimo że jest cięższy..
Stereoizomery

W strukturze molekularnej atom węgla w środku (Cdwa) jest asymetryczny, ponieważ ma cztery różne podstawniki: OH, H, CH3 i CHdwaO.
Na powyższym obrazku widać również wyżej wymienione. Po lewej stronie znajduje się wzór strukturalny, a po prawej dwa stereoizomery glikolu propylenowego:
Należy zauważyć, że wspomniana para stereoizomerów jest odbiciem lustrzanym, to znaczy nie można ich nakładać; i dlatego są enancjomerami.
Jeśli stereoizomer skrajnie prawy (o konfiguracji R) jest „odwrócony”, będzie miał taki sam wzór jak jego partner (o konfiguracji S); z tą różnicą, że twój atom H będzie wskazywał z płaszczyzny, w kierunku czytelnika, a nie za płaszczyzną.
Nieruchomości
Nazwy chemiczne
-Glikol propylenowy lub glikol α-propylenowy
-1,2-propanodiol (preferowany przez IUPAC)
-1,2-dihydroksypropan
-Glikol metyloetylowy.
Waga molekularna
76,095 g / mol
Temperatura topnienia
-60 ºC.
Temperatura wrzenia
187,6 ° C.
punkt zapłonu
-104 ºC.
-99 ºC (zamknięty tygiel).
Rozpuszczalność w wodzie
106 mg / l w 20 ° C; to znaczy, praktycznie mieszalny w każdej proporcji.
Rozpuszczalność w cieczach organicznych
Rozpuszczalny w etanolu, acetonie i acetonie. Oprócz wody miesza się również z acetonem i chloroformem. Rozpuszczalny w eterze.
Gęstość
1,0361 g / cm3 przy 20 ºC.
Gęstość pary
2,62 (w odniesieniu do powietrza przyjętego jako 1).
Ciśnienie pary
0,13 mmHg w 25 ° C.
Stabilność
W niskich temperaturach jest stabilny w szczelnie zamkniętych pojemnikach. Ale w otwartych pojemnikach iw wysokich temperaturach ma tendencję do utleniania, wytwarzając aldehyd propionowy, kwas mlekowy, kwas pirogronowy i kwas octowy..
Glikol propylenowy jest stabilny chemicznie po zmieszaniu z 95% etanolem, glicyną lub wodą.
Lepkość
0,581 cPuazy w 20 ° C.
Ciepło spalania
431 kcal / mol.
Ciepło parowania
168,6 cal / g (w temperaturze wrzenia).
Ciepło właściwe
0,590 cal / g przy 20 ºC.
Ciepło formowania
-116,1 kcal / mol w 25 ºC.
Współczynnik załamania światła
1,431 - 1,433 w 20 ° C.
pKa
14,9 w 25 ° C.
Synteza
Z tlenku propylenu
W przemyśle glikol propylenowy jest wytwarzany z tlenku propylenu (który jest epoksydem). Niektórzy producenci nie stosują katalizatorów tą metodą, a reakcję przeprowadzają w wysokich temperaturach od 200 do 220 ºC.
Z drugiej strony, inni producenci używają metali jako katalizatorów, a stosowane temperatury są nieco niższe niż poprzednie, między 150ºC a 180ºC, przy obecności żywicy jonowymiennej i niewielkich ilości kwasu siarkowego lub zasady..
Reakcję przedstawiono w następującym równaniu chemicznym, w którym praktycznie węgiel w górnym wierzchołku trójkąta jest uwodniony w środowisku kwaśnym:

Końcowy produkt zawiera 20% glikolu propylenowego, który dodatkowo oczyszcza do 99,5%.
Z glicerolu
Syntezę glikolu propylenowego można również przeprowadzić z glicerolu przy użyciu katalizatorów; takie jak katalizator Ni Raneya.
Glicerol ma trzy grupy OH, więc musi się pozbyć jednej, jednocześnie potrzebny jest wodór, aby umożliwić tę przemianę, a woda jest uwalniana w reakcji hydrogenolizy.
Ryzyka
Chociaż stosowanie glikolu propylenowego w żywności jest uważane przez Amerykańską Agencję ds.Żywności i Leków (1982) za bezpieczne, istnieją doniesienia o niekorzystnych skutkach. Wśród nich wystąpiła hiperosmolalność, hemoliza, arytmia serca i kwasica mleczanowa..
15-miesięczny chłopiec, który otrzymał duże dawki witaminy C zawieszonej w glikolu propylenowym, miał epizody braku reakcji na stymulację, przyspieszenie oddechu, tachykardię, pocenie się i hipoglikemię..
Donoszono o występowaniu ataków związanych z przyjmowaniem witaminy D przy użyciu glikolu propylenowego jako nośnika do podawania. Podobnie, stan hiperosmolalności odnotowano u małych dzieci, które przyjmowały multiwitaminy zawierające glikol propylenowy..
U dorosłych dożylne podanie dużych dawek glikolu propylenowego może spowodować niewydolność nerek i zaburzenia czynności wątroby. Ponadto skutki toksyczne obejmują hiperosmolalność, kwasicę metaboliczną (kwasicę mleczanową) i zespół septyczny..
Szybkie dożylne wstrzyknięcie leków zawierających glikol propylenowy wiąże się z depresją nerwową, niedociśnieniem, udarem, arytmią, utratą przytomności i ostatecznie zatrzymaniem akcji serca..
WHO (1974) zaleciła maksymalną dawkę glikolu propylenowego 25 m / kg / dzień w pożywieniu. Niektóre badania wykazały toksyczne działanie glikolu propylenowego, gdy jego stężenie w surowicy przekracza 25 mg / dl.
Aplikacje
-Lekarze
Rozcieńczalnik w lekach
Niektóre preparaty do sztucznych łez, takie jak Systane, zawierają glikol propylenowy jako składnik.
Jest stosowany jako rozcieńczalnik do dożylnego podawania wielu leków, w tym: diazepamu, digoksyny, lorazepamu, ferrytyny, etomidatu, nitrogliceryny, fenobarbitalu sodu itp..
Glikol propylenowy został użyty w środkach do dezynfekcji rąk na bazie alkoholu, które mają działanie nawilżające, aby zapobiec wysuszeniu dłoni..
Środek higroskopijny
Glikol propylenowy jest dodawany do inhalatorów oddechowych w celu zmniejszenia lepkości wydzieliny oskrzelowej, jak ma to miejsce w przypadku choroby astmatycznej..
Antyseptyczny
Jest stosowany jako środek antyseptyczny o działaniu podobnym do etanolu; ale jest trochę mniej skuteczny niż etanol. Miejscowe stosowanie glikolu propylenowego w wodnym rozcieńczeniu 40-60%.
Leczenie rybiej łuski
Był stosowany w leczeniu pacjentów z rybią łuską sprzężoną z chromosomem X i rybią łuską pospolitą. Choroby te charakteryzują się procesem powstawania plam i łusek na skórze.
Glikol propylenowy i inne żele bezalkoholowe powodują nasilenie keratolitycznego działania kwasu salicylowego. Ta kombinacja związków chemicznych może być przydatna w leczeniu rybiej łuski..
Inni
Maść w której składzie zawiera 70% glikolu propylenowego, z dobrymi efektami stosowana jest w leczeniu obrzęku rogówki.
-Przemysłowy
W jedzeniu
.Glikol propylenowy jest bardzo przydatną substancją utrzymującą wilgoć w żywności. Ponadto działa jako środek konserwujący, który może działać na patogeny. Dodatkowo jest związkiem mało reaktywnym, dzięki czemu nie reaguje z innymi składnikami żywności..
-Jego higroskopijność zapewnia wchłanianie wody i innych substancji w optymalnych warunkach. W ten sposób utrzymuje się kontrolę wilgotności potrawy, aby uniknąć jej wysuszenia i przyspieszenia jej psucia się..
-Jest przeciwutleniaczem, który wydłuża okres półtrwania żywności, chroniąc ją przed uszkodzeniami, jakie może wywołać tlen..
-Działa poprzez rozpuszczanie innych dodatków, które mogą występować w przetwórstwie żywności, takich jak: barwniki, aromaty i przeciwutleniacze.
-Służy do przygotowania płynnych słodzików, kremowych lodów, bitego mleka itp..
Płyn przeciw zamarzaniu
Pełni funkcję podobną do glikolu etylenowego. Jednak preferowano stosowanie glikolu propylenowego ze względu na jego niską toksyczność. Glikol etylenowy może powodować kryształy szczawianu wapnia, które mogą uszkodzić serce, płuca i nerki..
Glikol propylenowy jest w stanie blokować tworzenie się kryształków lodu, zapobiegając zamarzaniu. Dodatkowo obniża temperaturę zamarzania wody, utrudniając jej występowanie. Znajduje również zastosowanie w odladzaniu skrzydeł samolotów..
Kosmetyki i produkty do pielęgnacji ciała
Służy do utrzymania nawilżenia włosów. Ponadto pomaga zmiękczyć skórę i włosy oraz kontroluje rozwój bakterii..
Glikol propylenowy jest używany do produkcji wielu produktów higieny osobistej, takich jak: dezodoranty, filtry przeciwsłoneczne, kremy do twarzy, balsamy do ciała oraz substancja pomocnicza stabilizująca pianę w kremie do golenia.
Jest również stosowany jako środek nawilżający, zapobiegający wysuszaniu skóry i dłoni..
Inni
Glikol propylenowy jest używany do produkcji środków klejących, uszczelniaczy i powłok.
Stosowany jest w płynach do przenoszenia ciepła oraz w płynach hydraulicznych i hamulcowych. Dodatkowo służy do tłumienia kurzu; w barwnikach i barwnikach: smary, odwadnianie gazu ziemnego, plastyfikatory, środki powierzchniowo czynne i woski.
Znajduje zastosowanie w przemyśle tekstylnym do produkcji włókien poliestrowych. Stosowany jest w farbach i powłokach do ochrony elementów; jako rozpuszczalnik w farbach drukarskich i do produkcji zgodnych z normami tworzyw sztucznych.
-Dodatkowe zastosowania
Armia USA używa go do produkcji dymu, który służy jako zasłona lub zasłona, aby ukryć ruch żołnierzy na polu bitwy..
Jest również stosowany w modelach pociągów i statków do symulacji emisji dymu za pomocą małych grzejników..
Glikol propylenowy wraz z gliceryną jest stosowany w płynnych wkładach do papierosów elektronicznych, co zmniejsza toksyczne skutki używania konwencjonalnych papierosów.
Bibliografia
- Wikipedia. (2019). Glikol propylenowy. Odzyskane z: en.wikipedia.org
- PubChem. (2019). Glikol propylenowy. Odzyskany z: pubchem.ncbi.nlm.nih.gov
- The Dow Chemical Company. (2019). Glikole propylenowe do zastosowań przemysłowych. Odzyskany z: dow.com
- Graham Solomons T.W., Craig B. Fryhle. (2011). Chemia organiczna. Aminy. (10th wydanie.). Wiley plus.
- Lim, T. Y., Poole, R. L. and Pagelen, N. M. (2014). Toksyczność glikolu propylenowego u dzieci. J. Pediatr. Pharmacol Ther. 19 (4): 277-282.
- Mandl Elise. (02 marca 2018). Glikol propylenowy w żywności: czy ten dodatek jest bezpieczny? Odzyskany z: heatline.com
- Green Carolyn. (26 września 2017). Zastosowania glikolu propylenowego w życiu codziennym. Odzyskany z: bizfluent.com



Jeszcze bez komentarzy