
Kierunek i zastosowania chemii środowiska
Plik chemia środowiska bada procesy chemiczne zachodzące na poziomie środowiskowym. Jest to nauka, która stosuje zasady chemiczne do badania efektów działalności środowiskowej i wpływu wywieranego przez działalność człowieka..
Ponadto chemia środowiska projektuje techniki zapobiegania, łagodzenia i naprawiania istniejących szkód w środowisku..
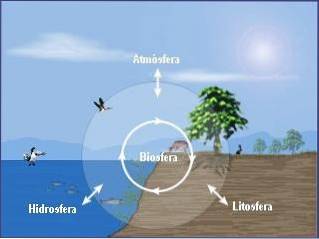
Chemię środowiska można podzielić na trzy podstawowe dyscypliny, którymi są:
- Chemia środowiska atmosfery.
- Chemia środowiska hydrosfery.
- Chemia środowiska gleby.
Integralne podejście do chemii środowiska wymaga dodatkowo zbadania wzajemnych zależności między procesami chemicznymi zachodzącymi w tych trzech przedziałach (atmosfera, hydrosfera, gleba) a ich związkami z biosferą..
Indeks artykułów
- 1 Chemia środowiska atmosfery
- 1.1 -Stratosfera
- 1.2 -Troposfera
- 2 Chemia środowiska hydrosfery
- 2.1 -Świeża woda
- 2.2 -Cykl wodny
- 2.3 - Oddziaływania antropologiczne na obieg wody
- 3 Chemia środowiska gleby
- 3.1 Gleba
- 3.2 Oddziaływania antropologiczne na glebę
- 4 Relacja chemiczna-środowisko
- 4.1 -Model Garrels i Lerman
- 5 Zastosowania chemii środowiska
- 6 Odnośniki
Chemia środowiska atmosfery
Atmosfera to warstwa gazów otaczająca Ziemię; stanowi bardzo złożony system, w którym temperatura, ciśnienie i skład chemiczny zmieniają się wraz z wysokością w bardzo szerokich zakresach.
Słońce bombarduje atmosferę promieniowaniem i wysokoenergetycznymi cząsteczkami; fakt ten ma bardzo znaczące skutki chemiczne we wszystkich warstwach atmosfery, ale w szczególności w warstwie górnej i zewnętrznej.
-Stratosfera
Reakcje fotodysocjacji i fotojonizacji zachodzą w zewnętrznych obszarach atmosfery. W rejonie między 30 a 90 km wysokości mierzonej od powierzchni Ziemi, w stratosferze, znajduje się warstwa zawierająca głównie ozon (O3), zwany warstwą ozonową.
Warstwa ozonowa
Ozon pochłania wysokoenergetyczne promieniowanie ultrafioletowe pochodzące ze słońca i gdyby nie istnienie tej warstwy, żadna znana forma życia na planecie nie mogłaby przetrwać..
W 1995 roku chemicy atmosferyczni Mario J. Molina (Meksyk), Frank S. Rowland (Amerykanin) i Paul Crutzen (Holender) otrzymali Nagrodę Nobla w dziedzinie chemii za swoje badania nad niszczeniem i zubożeniem ozonu w stratosferze..
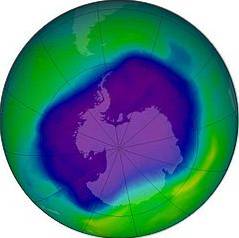
W 1970 Crutzen wykazał, że tlenki azotu niszczą ozon poprzez katalityczne reakcje chemiczne. Później Molina i Rowland w 1974 roku wykazali, że chlor w związkach chlorofluorowęglowodorowych (CFC) jest również zdolny do niszczenia warstwy ozonowej.
-Troposfera
Bezpośrednia warstwa atmosfery na powierzchni Ziemi, o wysokości od 0 do 12 km, zwana troposferą, składa się głównie z azotu (Ndwa) i tlen (Odwa).
Gazy toksyczne
W wyniku działalności człowieka troposfera zawiera wiele dodatkowych chemikaliów uznawanych za zanieczyszczenia powietrza, takich jak:
- Dwutlenek i tlenek węgla (COdwa i CO).
- Metan (CH4).
- Tlenek azotu (NO).
- Dwutlenek siarki (SOdwa).
- Ozon O3 (uważany za zanieczyszczający w troposferze)
- Lotne związki organiczne (LZO), proszki lub cząstki stałe.
Wśród wielu innych substancji, które mają wpływ na zdrowie ludzi, roślin i zwierząt.
Kwaśny deszcz
Tlenki siarki (SOdwa A więc3) i azotowych, takich jak podtlenek azotu (NOdwa), powodują inny problem środowiskowy zwany kwaśnym deszczem.
Tlenki te, obecne w troposferze głównie jako produkty spalania paliw kopalnych w działalności przemysłowej i transporcie, reagują z wodą deszczową, wytwarzając kwas siarkowy i azotowy, co prowadzi do wytrącania się kwasów..
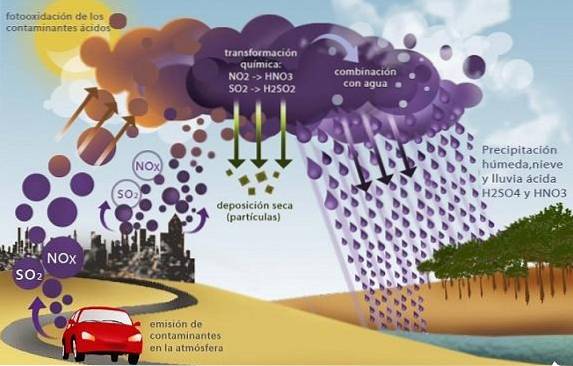
Wytrącając ten deszcz, który zawiera silne kwasy, wywołuje szereg problemów środowiskowych, takich jak zakwaszenie mórz i słodkich wód. To powoduje śmierć organizmów wodnych; zakwaszenie gleb powodujące obumieranie upraw i niszczenie przez korozyjne działanie chemiczne budynków, mostów i pomników.
Inne problemy związane ze środowiskiem atmosferycznym to smog fotochemiczny, wywoływany głównie przez tlenki azotu i ozon troposferyczny.
Globalne ocieplenie
Globalne ocieplenie jest spowodowane wysokimi stężeniami COdwa atmosferyczne i inne gazy cieplarniane (GHG), które pochłaniają większość promieniowania podczerwonego emitowanego przez powierzchnię Ziemi i zatrzymują ciepło w troposferze. To powoduje zmianę klimatu na naszej planecie.
Chemia środowiska hydrosfery
Hydrosfera składa się ze wszystkich zbiorników wodnych na Ziemi: powierzchniowych lub podmokłych - oceanów, jezior, rzek, źródeł - oraz podziemnych lub warstw wodonośnych..
-Świeża woda
Woda jest najpowszechniejszą substancją płynną na naszej planecie, pokrywa 75% powierzchni Ziemi i jest absolutnie niezbędna do życia..
Wszystkie formy życia zależą od słodkiej wody (definiowanej jako woda o zawartości soli poniżej 0,01%). 97% wody na naszej planecie to woda słona.
Z pozostałych 3% świeżej wody 87% znajduje się w:
- Bieguny Ziemi (które topią się i wlewają do mórz w wyniku globalnego ocieplenia).
- Lodowce (również zanikające).
- Wody gruntowe.
- Woda w postaci pary występującej w atmosferze.
Tylko 0,4% całkowitej słodkiej wody na naszej planecie jest dostępne do spożycia. Odparowywanie wody z oceanów i opady nieustannie zapewniają ten niewielki procent..
Chemia środowiskowa wody bada procesy chemiczne zachodzące w cyklu wodnym lub hydrologicznym, a także opracowuje technologie oczyszczania wody przeznaczonej do spożycia przez ludzi, oczyszczania ścieków przemysłowych i miejskich, odsalania wody morskiej, recyklingu i oszczędzania tego zasobu, pośród innych.
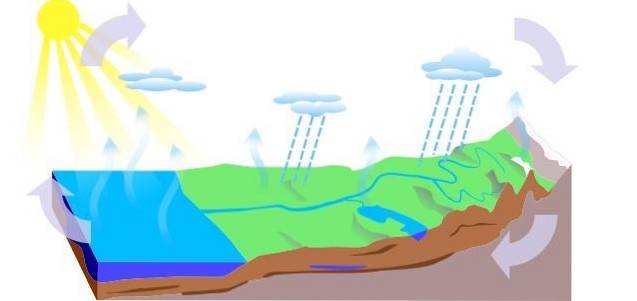
-Obieg wody
Cykl wodny na Ziemi składa się z trzech głównych procesów: parowania, kondensacji i opadów, z których pochodzą trzy obiegi:
- Spływ powierzchniowy
- Ewapotranspiracja roślin
- Infiltracja, podczas której woda przedostaje się do poziomów podziemnych (freatic), krąży kanałami wodonośnymi i wychodzi przez źródła, fontanny lub studnie.
-Oddziaływania antropologiczne na obieg wody
Działalność człowieka ma wpływ na obieg wody; niektóre przyczyny i skutki działań antropologicznych są następujące:
Modyfikacja powierzchni ziemi
Powstaje w wyniku niszczenia lasów i pól z wylesieniem. Wpływa to na obieg wody poprzez eliminację ewapotranspiracji (pobór wody przez rośliny i powrót do środowiska w wyniku transpiracji i parowania) oraz zwiększenie odpływu..
Wzrost spływu powierzchniowego powoduje wzrost przepływu rzek i powodzi.
Urbanizacja modyfikuje również powierzchnię terenu i wpływa na obieg wody, ponieważ porowatą glebę zastępuje nieprzepuszczalny cement i asfalt, co uniemożliwia infiltrację..
Zanieczyszczenie obiegu wody
Cykl wodny obejmuje całą biosferę, w związku z czym odpady wytwarzane przez człowieka są włączane do tego cyklu za pomocą różnych procesów..
Zanieczyszczenia chemiczne w powietrzu przedostają się do deszczu. Substancje agrochemiczne stosowane do gleby, ulegają wymywaniu i infiltracji do warstw wodonośnych lub spływają do rzek, jezior i mórz.
Również odpady tłuszczów i olejów oraz odcieki ze składowisk sanitarnych są wciągane przez infiltrację do wód gruntowych.
Wydobywanie zasobów wodnych z debetem w zasobach wodnych
Te praktyki w zakresie przekroczenia stanu konta powodują wyczerpywanie się zasobów wód gruntowych i powierzchniowych, wpływają na ekosystemy i powodują lokalne osiadanie gleby..
Chemia środowiska gleby
Gleby są jednym z najważniejszych czynników wpływających na równowagę biosfery. Zapewniają kotwiczenie, wodę i składniki odżywcze roślinom, które są producentami ziemskich łańcuchów troficznych.
Gleba
Glebę można zdefiniować jako złożony i dynamiczny ekosystem składający się z trzech faz: fazy stałej z podłożem mineralnym i organicznym, wodnej fazy ciekłej i fazy gazowej; charakteryzuje się posiadaniem określonej fauny i flory (bakterie, grzyby, wirusy, rośliny, owady, nicienie, pierwotniaki).
Właściwości gleby są stale modyfikowane przez warunki środowiskowe i zachodzącą w niej aktywność biologiczną..
Oddziaływania antropologiczne na glebę
Degradacja gleby to proces, który zmniejsza produktywność gleby i może spowodować głęboką i negatywną zmianę w ekosystemie..
Czynniki powodujące degradację gleby to: klimat, fizjografia, litologia, roślinność i działalność człowieka.

Ludzkie działanie może spowodować:
- Fizyczna degradacja gleby (na przykład zagęszczenie spowodowane niewłaściwymi praktykami rolniczymi i ranczerskimi).
- Chemiczna degradacja gleby (m.in. zakwaszenie, alkalizacja, zasolenie, zanieczyszczenie agrochemikaliami, ściekami z działalności przemysłowej i miejskiej, wycieki ropy).
- Biologiczna degradacja gleby (m.in. zmniejszenie zawartości materii organicznej, degradacja szaty roślinnej, utrata mikroorganizmów wiążących azot).
Relacja chemiczno-środowiskowa
Chemia środowiska bada różne procesy chemiczne zachodzące w trzech częściach środowiska: atmosferze, hydrosferze i glebie. Interesujący jest przegląd dodatkowego podejścia do prostego modelu chemicznego, który próbuje wyjaśnić globalne transfery materii zachodzące w środowisku..
-Model Garrels i Lerman
Garrels i Lerman (1981) opracowali uproszczony model biogeochemii powierzchni Ziemi, który bada interakcje między przedziałami: atmosferą, hydrosferą, skorupą ziemską i zawartą w niej biosferą..
Model Garrelsa i Lermana uwzględnia siedem głównych minerałów składowych planety:
- Gips (CaSO4)
- Piryt (FeSdwa)
- Węglan wapnia (CaCO3)
- Węglan magnezu (MgCO3)
- Krzemian magnezu (MgSiO3)
- Tlenek żelaza (FedwaLUB3)
- Dwutlenek krzemu (SiOdwa)
Materia organiczna tworząca biosferę (zarówno żywa, jak i martwa) jest reprezentowana jako CHdwaLub, który jest przybliżonym składem stechiometrycznym żywych tkanek.
W modelu Garrelsa i Lermana zmiany geologiczne są badane jako transfery netto materii między tymi ośmioma składnikami planety, poprzez reakcje chemiczne i równowagę zachowania masy netto..
Nagromadzenie COdwa w atmosferze
Na przykład problem akumulacji COdwa w atmosferze jest badany w tym modelu, mówiąc, że: obecnie spalamy węgiel organiczny zmagazynowany w biosferze w postaci węgla, ropy i gazu ziemnego osadzonych w podłożu w przeszłości geologicznej.
Konsekwencją tego intensywnego spalania paliw kopalnych jest stężenie COdwa atmosferyczne rośnie.
Zwiększone stężenie COdwa w atmosferze ziemskiej wynika z faktu, że tempo spalania węgla kopalnego przewyższa szybkość jego pochłaniania przez inne składniki ziemskiego układu biogeochemicznego (takie jak na przykład organizmy fotosyntetyzujące i hydrosfera).
W ten sposób emisja COdwa do atmosfery w wyniku działalności człowieka, omija system regulacyjny, który moduluje zmiany na Ziemi.
Wielkość biosfery
Model opracowany przez Garrelsa i Lermana uwzględnia również, że rozmiar biosfery zwiększa się i zmniejsza w wyniku równowagi między fotosyntezą a oddychaniem..
W historii życia na Ziemi masa biosfery zwiększała się etapami z wysokim współczynnikiem fotosyntezy. Spowodowało to magazynowanie netto węgla organicznego i emisję tlenu:
WSPÓŁdwa + H.dwaO → CHdwaO + Odwa
Oddychanie jako aktywność metaboliczna mikroorganizmów i wyższych zwierząt przekształca węgiel organiczny z powrotem w dwutlenek węgla (COdwa) i wodę (H.dwaO), czyli odwraca poprzednią reakcję chemiczną.
Obecność wody, magazynowanie węgla organicznego i wytwarzanie tlenu cząsteczkowego mają fundamentalne znaczenie dla istnienia życia..
Zastosowania chemii środowiska
Chemia środowiska oferuje rozwiązania w zakresie zapobiegania, łagodzenia i naprawiania szkód w środowisku spowodowanych działalnością człowieka. Wśród niektórych z tych rozwiązań możemy wymienić:
- Projekt nowych materiałów zwanych MOF (od angielskiego akronimu: Metalowe ramy organiczne). Są bardzo porowate i mają zdolność: pochłaniania i zatrzymywania COdwa, dostać HdwaLub z pustynnych oparów powietrza i przechowuj H.dwa w małych pojemnikach.
- Przekształcanie odpadów w surowce. Na przykład wykorzystanie zużytych opon do produkcji sztucznej trawy lub podeszew do butów. Również wykorzystanie odpadów z przycinania roślin do produkcji biogazu lub bioetanolu.
- Chemiczne syntezy substytutów CFC.
- Rozwój alternatywnych źródeł energii, takich jak ogniwa wodorowe, do wytwarzania niezanieczyszczającej energii elektrycznej.
- Kontrola zanieczyszczenia atmosfery za pomocą filtrów obojętnych i filtrów reaktywnych.
- Odsalanie wody morskiej metodą odwróconej osmozy.
- Opracowanie nowych materiałów do flokulacji zawieszonych w wodzie substancji koloidalnych (proces oczyszczania).
- Odwrócenie eutrofizacji jezior.
- Rozwój „zielonej chemii”, trendu proponującego zastępowanie toksycznych związków chemicznych mniej toksycznymi, oraz „przyjaznych dla środowiska” procedur chemicznych. Przykładowo znajduje zastosowanie przy stosowaniu mniej toksycznych rozpuszczalników i surowców, w przemyśle m.in. w pralniach na sucho..
Bibliografia
- Calvert, J. G., Lazrus, A., Kok, G. L., Heikes, B. G., Walega, J. G., Lind, J., and Cantrell, C. A. (1985). Mechanizmy chemiczne powstawania kwasów w troposferze. Naturę, 317 (6032), 27-35. doi: 10.1038 / 317027a0.
- Crutzen, P.J. (1970). Wpływ tlenków azotu na zawartość atmosfery. Q.J.R. Metheorol. Soc. Wiley-Blackwell. 96: 320-325.
- Garrels, R.M. i Lerman, A. (1981). Cykle fanerozoiczne węgla osadowego i siarki. Materiały z Akademii Nauk Przyrodniczych. ZASTOSOWANIA. 78: 4,652-4,656.
- Hester, R. E. i Harrison, R. M. (2002). Globalna zmiana środowiska. Królewskie Towarzystwo Chemii. pp 205.
- Hites, R. A. (2007). Elementy chemii środowiska. Wiley-Interscience. pp 215.
- Manahan, S. E. (2000). Chemia środowiska. Wydanie siódme. CRC. pp 876
- Molina, M.J. i Rowland, F.S. (1974). Stratosferyczny pochłaniacz chlorofluorometanów: katalizowane atomem chloru niszczenie ozonu. Natura. 249: 810-812.
- Morel, F.M. i Hering, J.M. (2000). Zasady i zastosowania chemii wodnej. Nowy Jork: John Wiley.
- Stockwell, W. R., Lawson, C. V., Saunders, E. i Goliff, W. S. (2011). Przegląd troposferycznej chemii atmosfery i mechanizmów chemicznych fazy gazowej do modelowania jakości powietrza. Atmosfera, 3 (1), 1-32. doi: 10.3390 / atm3010001


Jeszcze bez komentarzy