
Reakcja endotermiczna i egzotermiczna

ZA reakcja endotermiczna wymaga mocy, gdy a reakcja egzotermiczna uwalnia energię. Ta klasyfikacja reakcji chemicznych uwzględnia udział energii jako substratu lub produktu..
Energia to zdolność do wykonywania pracy lub wytwarzania ciepła. Pamiętaj, że reakcje chemiczne obejmują reorganizację atomów między substancjami z przerwaniem lub utworzeniem wiązań chemicznych. Ogólnie rzecz biorąc, temu tworzeniu się lub zrywaniu wiązań chemicznych towarzyszą zmiany energii układu..
| Reakcja endotermiczna | Reakcja egzotermiczna | |
|---|---|---|
| Definicja | Reakcja chemiczna, w której pochłaniana jest energia. | Reakcja chemiczna, w której energia jest uwalniana w postaci ciepła. |
| Pochodzenie energii | Środowiska | Systemu |
| Energia potencjalna | Mniejsza zawartość reagentów niż produktów. | Większe w reagentach niż w produktach. |
| Produkcja | Nie spontaniczne | Spontaniczny |
| Zmiana energii wewnętrznej | ΔE> 0; wewnętrzna zmiana energii większa niż zero. | ΔE<0; cambio de energía interna menor que cero. |
| Temperatura | Zmniejsza się | Zwiększa |
| Przykłady | Reakcje w fotosyntezie i syntezie w ogóle. | Płonąca zapałka, reakcje spalania. |
Co to jest reakcja endotermiczna?
Reakcja chemiczna jest endotermiczna, gdy pochłania energię z otoczenia. W tym przypadku ciepło jest przenoszone z zewnątrz do wnętrza systemu. Kiedy umieszczamy termometr w czasie reakcji endotermicznej, temperatura spada.
Słowo „endotermiczny” pochodzi z języka greckiego endon co oznacza „wewnątrz” i term co oznacza „ciepło”. Reakcje endotermiczne nie zachodzą spontanicznie.
Skąd pochodzi energia w reakcjach endotermicznych?
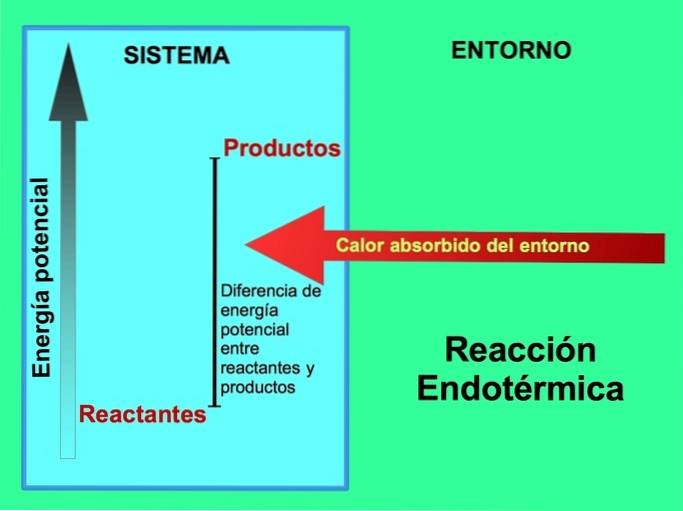
W reakcjach endotermicznych energia pochodzi ze środowiska znajdującego się poza systemem. Ilość energii potencjalnej produktów jest większa niż energia potencjalna reagentów. Dlatego konieczne jest dodanie energii do reagentów, aby reakcja przebiegła. Ta energia pochodzi z ciepła otoczenia.
Na przykład, fotosynteza jest procesem endotermicznym, gdzie rośliny wychwytują energię słoneczną do produkcji glukozy z dwutlenku węgla i tlenu:

Produkty reakcji fotosyntezy, glukoza i tlen, mają większą ilość energii potencjalnej w stosunku do reagentów, dwutlenku węgla i wody. Inne przykłady endotermicznych reakcji chemicznych z ilością zużytej energii:

Przykłady reakcji endotermicznych
Reakcje zachodzą nie tylko w laboratorium chemicznym. Na co dzień spotykamy się również z sytuacjami, w których zachodzą reakcje endotermiczne.
Gotowanie jedzenia
Chociaż może się na to nie wydawać, proces gotowania potraw jest endotermiczny. Aby móc spożywać określone pokarmy, musimy zapewnić ciepło.
Natychmiastowa zimna torba
Zimne okłady stosowane w leczeniu guzków lub skręceń są wypełnione wodą, ale po potrząśnięciu lub uderzeniu kapsułka zawierająca azotan amonu pęka w środku. Zmieszanie saletry amonowej z wodą jest reakcją endotermiczną powodującą ochłodzenie worka.
Co to jest reakcja egzotermiczna?
ZA reakcja egzotermiczna to taka, w której energia wypływa z układu. Energia ta jest uwalniana w postaci ciepła, więc umieszczenie termometru w układzie reakcyjnym podwyższa temperaturę.
Słowo „egzotermiczny” jest utworzone przez egzo co oznacza „na zewnątrz” i termy, co oznacza „ciepło”. Reakcje egzotermiczne mogą zachodzić spontanicznie, aw niektórych przypadkach mogą być wybuchowe, jak na przykład połączenie metali alkalicznych i wody.
Skąd pochodzi energia w reakcjach egzotermicznych?
W reakcji chemicznej reagentami są związki, które przekształcają się i tworzą produkty. Na przykład, gdy sodu Na reaguje z chlorem Cl, są to reagenty, a produktem jest chlorek sodu NaCl:
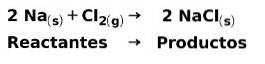
Zarówno reagenty, jak i produkty zgromadziły energię potencjalną. Wiemy z loszczędność energii ey energia ta nie jest ani tracona, ani uzyskiwana, więc energia reagentów musi być równa energii produktów.
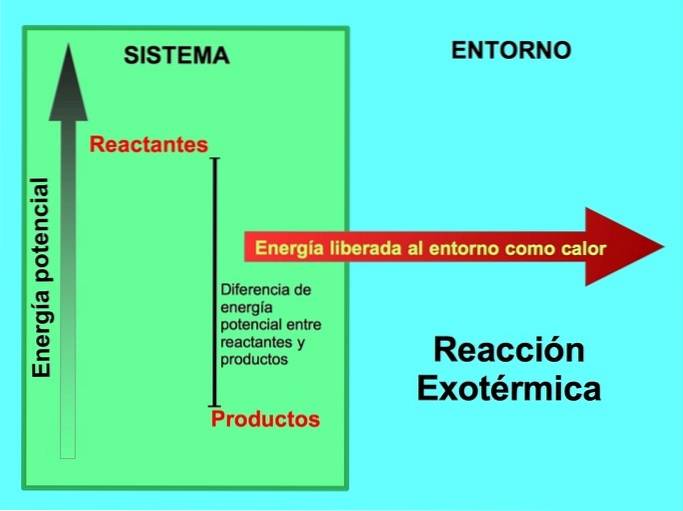
W reakcji egzotermicznej lreagenty mają więcej energii potencjalnej w porównaniu z produktami, więc nadmiar energii jest uwalniany w postaci ciepła. W tym przypadku energia jest również uważana za część produktów:

W każdym procesie egzotermicznym część energii potencjalnej zmagazynowanej w wiązaniach chemicznych jest zamieniana na energię cieplną poprzez ciepło..
Przykłady reakcji egzotermicznych
Proszek do prania
Kiedy rozpuścimy w dłoniach odrobinę proszku do prania z wodą, możemy poczuć lekkie rozgrzanie.
Domowe spalanie gazu
Spalanie gazów do użytku domowego, takich jak metan czy butan, obejmuje reakcję chemiczną z tlenem z wytworzeniem dwutlenku węgla i wody oraz uwolnienie energii. To typowa egzotermiczna reakcja w codziennym użytkowaniu:
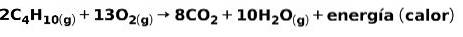
Energia uwalniana w procesie spalania wykorzystywana jest do gotowania potraw.
Możesz również chcieć dowiedzieć się, czym jest system otwarty, system zamknięty i system izolowany.



Jeszcze bez komentarzy