
Struktura, właściwości, zastosowania, synteza siarczanu potasu (K2SO4)

Plik siarczan potasu jest białą lub bezbarwną solą nieorganiczną o wzorze chemicznym Kdwapołudniowy zachód4. Znany był już w XIV wieku, nazywany w XVII wieku solą duplicatum, gdyż jest połączeniem soli kwaśnej i alkalicznej..
Siarczan potasu występuje w postaci mineralnej w arkanicie, ale jego postać występuje częściej w tzw. Solach Stassfurtu. Są to ko-krystalizacje siarczanów potasu, magnezu, wapnia i sodu, które można zaobserwować w minerałach takich jak leonit i polihalit..

Siarczan potasu jest solą o niskiej toksyczności i powoduje podrażnienie jedynie w kontakcie z oczami, drogami oddechowymi lub przewodem pokarmowym. Nie ma dowodów na działanie rakotwórcze lub mutagenne.
Siarczan potasu jest stosowany jako nawóz, zwłaszcza w uprawach podatnych na chlorki; tak jest w przypadku tytoniu i ziemniaków. Związek dostarcza potasu, jednego z trzech głównych składników odżywczych roślin oraz siarki, która jest obecna w ich białkach..
Indeks artykułów
- 1 Struktura
- 1.1 Fazy krystaliczne
- 1.2 Plątanina jonowa
- 2 Właściwości fizyczne i chemiczne
- 2.1 Nazwy
- 2.2 Masa molowa
- 2.3 Wygląd fizyczny
- 2.4 Gęstość
- 2.5 Temperatura topnienia
- 2.6 Temperatura wrzenia
- 2.7 Rozpuszczalność w wodzie
- 2.8 Rozpuszczalność w rozpuszczalnikach organicznych
- 2.9 Współczynnik załamania światła (nD)
- 2.10 Reaktywność
- 3 Synteza
- 3.1 Pierwsza metoda
- 3.2 Druga metoda
- 3.3 Trzecia metoda
- 3.4 Czwarta metoda
- 4 Zastosowania
- 4.1 Nawóz
- 4.2 Zastosowanie przemysłowe i jako surowiec
- 4.3 Medycyna
- 4.4 Weterynaria
- 4.5 Aromaty spożywcze
- 4.6 Inne zastosowania
- 5 Ryzyka
- 6 Odnośniki
Struktura
Fazy krystaliczne
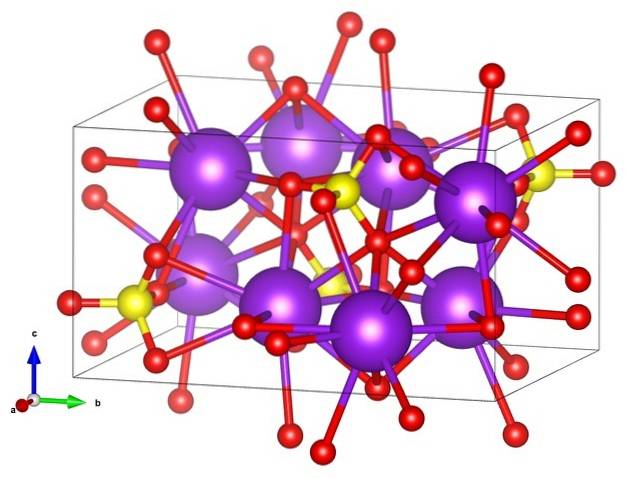
Na pierwszym zdjęciu pokazano wzór strukturalny siarczanu potasu. Dla każdego anionu SO4dwa-, o geometrii czworościennej występują dwa kationy K.+, które mogą być reprezentowane przez fioletowe kule (górne zdjęcie).
Tak więc powyżej mamy rombową strukturę krystaliczną Kdwapołudniowy zachód4, z anionami SO4dwa- reprezentowane przez żółte i czerwone kule; podczas gdy kationy K.+, już powiedziałem, że są to fioletowe kule (trochę bardziej wytrzymałe).
Ta reprezentacja może powodować zamieszanie, jeśli myślisz, że słupki naprawdę odpowiadają połączeniom koordynacyjnym. Wskazują raczej, który jon oddziałuje bezpośrednio lub blisko z innym wokół niego. Dlatego każdy tlen „łączy się” z pięcioma K.+ (LUB3południowy zachóddwa-- K.+), a te z kolei z dziesięcioma tlenami z innych otaczających anionów siarczanowych.
Istnieje zatem „rzadka” sfera koordynacyjna potasu w K.dwapołudniowy zachód4:
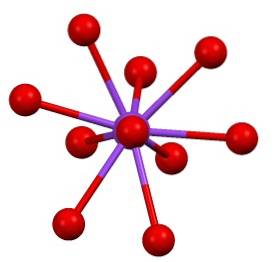
Ta krystaliczna struktura odpowiada polimorfowi β-Kdwapołudniowy zachód4. Po podgrzaniu do 583 ºC następuje przejście do fazy α-Kdwapołudniowy zachód4, który jest sześciokątny.
Plątanina jonów
Z pewnością struktura K.dwapołudniowy zachód4 jest to niezwykle skomplikowane w przypadku soli nieorganicznej. Jego jony są ułożone, tworząc rodzaj bezsensownej plątaniny i, jak widać gołym okiem, pozbawionej okresowości.
Ci, którzy poświęcają się krystalografii, mogą podejść do tego splotu w bardziej odpowiedni i opisowy sposób, obserwując go z trzech osi przestrzennych.
Zauważ, że jego splątana struktura może wyjaśnić, dlaczego Kdwapołudniowy zachód4 nie tworzy hydratów: cząsteczek H.dwaLub nie mają możliwości penetracji sieci krystalicznej w celu uwodnienia kationów potasu.
Ponadto, przy tak wielu oddziaływaniach obejmujących plątaninę jonów, należy się spodziewać, że ta sieć krystaliczna będzie miała dość dużą odporność na ciepło; i faktycznie tak jest, ponieważ temperatura topnienia Kdwapołudniowy zachód4 wynosi 1069 ºC, co pokazuje, że jego jony są silnie kohezyjne.
Fizyczne i chemiczne właściwości

Nazwy
-Siarczan potasu
-Siarczan potażu
-Arcanite
-Potaż siarkowy
Masa cząsteczkowa
174,259 g / mol
Wygląd fizyczny
Białe, bezwonne, gorzkie krystaliczne ciało stałe, granulki lub proszek.
Gęstość
2,66 g / cm3
Temperatura topnienia
1069 ºC
Temperatura wrzenia
1,689 ºC
Rozpuszczalność w wodzie
111 g / L przy 20 ºC
120 g / L przy 25 ºC
240 g / L przy 100 ºC
Rozpuszczalność w wodzie spada z powodu obecności chlorku potasu, KCl lub siarczanu amonu (NH4)dwapołudniowy zachód4, ze względu na efekt wspólnego jonu.
Rozpuszczalność w rozpuszczalnikach organicznych
Słabo rozpuszczalny w glicerolu, ale nierozpuszczalny w acetonie i siarczku węgla.
Współczynnik załamania (nD)
1,495
Reaktywność
Siarczan potasu może reagować z kwasem siarkowym, zakwaszając, tworząc wodorosiarczan potasu (KHSO4). W wysokich temperaturach można go zredukować do siarczku potasu (KdwaS).
Synteza
Pierwsza metoda
Siarczan potasu jest syntetyzowany w reakcji chlorku potasu z kwasem siarkowym. Synteza siarczanu potasu przebiega dwuetapowo. Pierwszy etap polega na utworzeniu wodorosiarczanu potasu.
Jest to reakcja egzotermiczna, ponieważ uwalnia ciepło i dlatego nie wymaga zewnętrznego źródła ciepła. Reakcję prowadzi się w temperaturze pokojowej.
KCl + Hdwapołudniowy zachód4 => HCl + KHSO4
Drugi etap reakcji jest endotermiczny, to znaczy wymaga dostarczenia ciepła, aby mogło nastąpić.
KCl + KHSO4 => HCl + Kdwapołudniowy zachód4
Druga metoda
Siarczan potasu można syntetyzować w reakcji zobojętniania kwasu siarkowego zasadą, wodorotlenkiem potasu:
H.dwapołudniowy zachód4 + 2 KOH => Kdwapołudniowy zachód4 + 2 godzdwaLUB
Trzecia metoda
Siarczan potasu powstaje w wyniku reakcji dwutlenku siarki, tlenu, chlorku potasu i wody.
Czwarta metoda
Siarczan potasu jest wytwarzany poprzez ekstrakcję siarczanu potasu obecnego w solance z dorzecza Loop Nur w Chinach. Siarczan potasu oddziela się od nierozpuszczalnych składników solanki przez dodanie związku zakwaszającego tripolifosforan sodu / fosforan mocznika.
Związek ten zwiększa różnicę między rozpuszczalnością siarczanu potasu a rozpuszczalnością innych mniej rozpuszczalnych związków, uzyskując, zdaniem twórców metody, 100% czysty siarczan potasu. W ścisłym sensie nie jest to metoda syntezy, ale nowatorska metoda ekstrakcji.
Aplikacje
Nawóz

Głównym zastosowaniem jako nawozu jest siarczan potasu. 90% jego całkowitej produkcji jest wykorzystywane do tego celu. Jego stosowanie jest preferowane niż chlorku potasu w uprawach wrażliwych na obecność chlorków w glebie; na przykład tytoń.
Siarczan potasu zawiera 40-44% potasu, a zawartość siarki 17-18%. Potas jest niezbędny do pełnienia wielu podstawowych funkcji dla roślin, ponieważ aktywuje reakcje enzymatyczne, syntezę białek, tworzenie skrobi itp..
Ponadto potas bierze udział w regulacji przepływu wody w liściach. Siarka jest niezbędna do syntezy białek, ponieważ występuje w aminokwasach, które ją posiadają; tak jest w przypadku metioniny, cysteiny i cystyny, a także interweniuje w reakcjach enzymatycznych.
Nawet siarczan potasu jest używany przez opryskiwanie liści cząstkami siarczanu potasu mniejszymi niż 0,015 mm.
Zastosowanie przemysłowe i jako surowiec
Surowy siarczan potasu jest używany do produkcji szkła oraz do produkcji ałunu i węglanu potasu. Jest używany jako odczynnik w produkcji kosmetyków. Jest używany do produkcji piwa jako środek korygujący wodę.
Lekarstwo
Stosowany jest w celu skorygowania ciężkiego spadku stężenia potasu w osoczu (hipokaliemii), spowodowanego nadmiernym stosowaniem leków moczopędnych, które zwiększają wydalanie potasu z moczem..
Potas jest głównym wewnątrzkomórkowym jonem komórek pobudliwych, w tym komórek serca. Dlatego znaczny spadek stężenia potasu w osoczu upośledza czynność serca i należy go natychmiast skorygować..
Siarczan potasu ma działanie przeczyszczające, to znaczy sprzyja wydalaniu stolca z okrężnicy. Z tego powodu mieszanina siarczanów potasu, magnezu i sodu służy do oczyszczenia okrężnicy ze stolca przed wykonaniem kolonoskopii, co pozwala lekarzowi na lepszą wizualizację okrężnicy..
weterynarz
Siarczan potasu został użyty w celu zmniejszenia zapotrzebowania na metioninę w paszy dla drobiu. Obecność 0,1% siarczanu potasu w paszy dla kur niosek wiąże się z 5% wzrostem produkcji jaj.
Aromaty spożywcze
Jest to środek aromatyzujący, który nadaje potrawom gorzki i słony smak, który jest pożądany w niektórych z nich. Ponadto należy zauważyć, że siarczan potasu jest obdarzony czterema podstawowymi smakami: słodyczą, goryczką, kwasowością i zasoleniem..
Wraz ze stężeniem siarczanu potasu wzrasta zasolenie, kwasowość i gorycz, natomiast spada słodycz.
Inne zastosowania
Siarczan potasu jest używany jako materiał pirotechniczny, w połączeniu z azotanem potasu, w celu wytworzenia fioletowego płomienia. Używany jako reduktor płomienia w ładunkach sterów strumieniowych artylerii.
Ponadto jest stosowany jako środek zwiększający lepkość w produktach kosmetycznych, takich jak kremy do twarzy..
Ryzyka
Siarczan potasu jest związkiem o niskiej toksyczności i bardzo niskiej śmiertelności. LD50 dla dawki doustnej dla myszy wynosi 6600 mg / kg masy ciała zwierzęcia, co wskazuje, że do spowodowania śmierci myszy wymagana jest wysoka dawka. Ta sama wartość LD50 występuje u szczurów.
W kontakcie z oczami siarczan potasu może powodować mechaniczne podrażnienie. Na skórze siarczan potasu powoduje niewielkie uszkodzenia przy obróbce przemysłowej..
W przypadku połknięcia siarczan potasu może powodować podrażnienie przewodu pokarmowego z nudnościami, wymiotami i biegunką. I wreszcie wdychanie pyłu siarczanu potasu powoduje podrażnienie dróg oddechowych..
Bibliografia
- Shiver & Atkins. (2008). Chemia nieorganiczna. (Czwarta edycja). Mc Graw Hill.
- Wikipedia. (2019). Siarczan potasu. Odzyskane z: en.wikipedia.org
- Narodowe Centrum Informacji Biotechnologicznej. (2019). Siarczan potasu. Baza danych PubChem. CID = 24507. Odzyskany z: pubchem.ncbi.nlm.nih.gov
- Brian Clegg. (5 lipca 2018). Siarczan potasu. Królewskie Towarzystwo Chemii. Źródło: chemistryworld.com
- Marie T. Averbuch-Pouchot, A. Durif. (tysiąc dziewięćset dziewięćdziesiąty szósty). Tematy w chemii fosforanów. World Scientific. Odzyskane z: books.google.co.ve
- Książka chemiczna. (2017). Siarczan potasu. Odzyskane z: chemicalbook.com
- Shoujiang L. i in. (2019). Oczyszczanie i szybkie rozpuszczanie siarczanu potasu w roztworach wodnych. DOI: 10.1039 / C8RA08284G
- DrugBank. (2019). Siarczan potasu. Odzyskany z: drugbank.ca
- The Mosaic Company. (2019). Siarczan potasu. Odżywianie roślin uprawnych. Odzyskany z: cropnutrition.com
- Leki. (2018). Siarczan sodu, siarczan potasu i siarczan magnezu (doustnie). Odzyskany z: drugs.com

Jeszcze bez komentarzy