
Uzasadnienie, materiały, technika i zastosowania plamy Wrighta

Plik Plama Wrighta to technika barwienia stworzona przez amerykańskiego patologa Jamesa Homera Wrighta w 1902 roku, oparta na barwie Romanowsky. Ponieważ plama Romanowsky'ego była niestabilna, Wright dodał metanol jako rozpuszczalnik i utrwalacz..
To zabarwienie jest polichromatyczne, co oznacza, że generuje kilka kolorów w zależności od struktury, która pochłania barwnik. Ta technika barwienia jest szeroko stosowana do wykonywania różnicowej liczby białych krwinek oraz do badania morfologii czerwonych krwinek, płytek krwi i leukocytów we krwi obwodowej i szpiku kostnym..
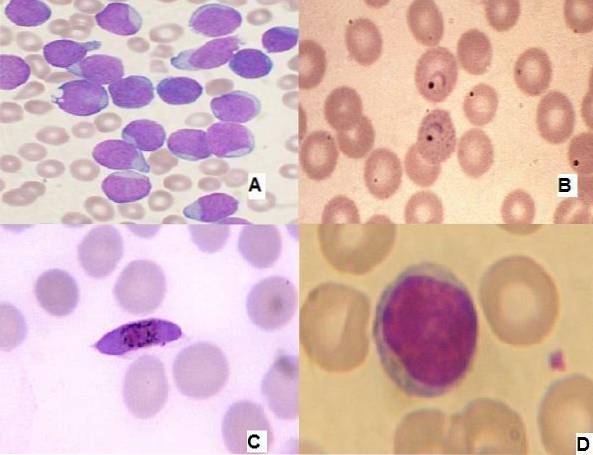
Jego zastosowanie jest bardzo ważne, ponieważ w różnych liniach komórkowych krwi można zaobserwować nieprawidłowości, co ułatwia diagnostykę chorób, takich jak białaczka czy infekcje bakteryjne lub pasożytnicze..
Być może są to najczęstsze zastosowania, w których ta technika jest wykorzystywana, ale nie jedyne. Jest również przydatny w próbkach innych niż krew i szpik kostny, takich jak między innymi wydzielina z nosa, śluz kałowy, plwocina, próbki skóry..
Indeks artykułów
- 1 Uzasadnienie dla plamy Wrighta
- 2 Materiały
- 2.1 Przygotowanie
- 2.2 Roztwór buforowy
- 2.3 Dodatkowe materiały potrzebne do wykonania barwienia
- 3 składniki bejcy Wrighta
- 3.1 Metanol
- 3.2 Amortyzator
- 3,3 Eozyna (Y)
- 3.4 Błękit metylenowy
- 4 Technika
- 5 Utility
- 5.1 Hematologia
- 5.2 Wydzielina z nosa
- 5.3 Parazytologia
- 5.4 Infekcje dróg oddechowych
- 5.5 Bakteriologia
- 5.6 Mykologia
- 6 Jak obserwuje się strukturę próbki krwi za pomocą barwienia Wrighta?
- 7 Zalecenia dotyczące dobrego barwienia
- 8 Typowych błędów w kolorowaniu Wrighta
- 8.1 Bardzo blade zabarwienie
- 8.2 Barwnik wytrąca się
- 8.3 Smugi o wyjątkowo czerwonawym lub niebieskim zabarwieniu
- 9 Tryb przechowywania
- 10 Referencje
Uzasadnienie dla plamy Wrighta
Barwnik Wright powstał z barwienia Romanowsky'ego, który składa się z roztworu barwnika kwasowego (eozyny Y) w alkoholu metylowym i barwnika zasadowego (błękit metylenowy) oraz produktów ich utleniania..
Mieszanina barwników zastosowana w barwieniu Wrighta powoduje efekt znany jako Romanowsky, czyli zapewnia piękne fioletowe zabarwienie jąderkom leukocytów i ziarnistościom neutrofilowym, podczas gdy krwinki czerwone zabarwiają się na różowo..
Składnikami odpowiedzialnymi za nadanie typowej gamy kolorów barwnika Wrighta są niebieski B i eozyna Y. Obserwowany efekt będzie zależał od wiązania barwników ze strukturami chemicznymi oraz interakcji błękitu B i eozyny Y.
Struktury kwasowe, takie jak kwasy nukleinowe, białka jądrowe i reaktywna niedojrzała cytoplazma niektórych typów komórek, utrwalają niebieskie B (podstawowe zabarwienie).
Podczas gdy podstawowe struktury, takie jak hemoglobina, granulki segmentowanych eozynofili, wśród innych struktur komórkowych, wiążą eozynę Y (barwnik kwasowy).
Na wynik barwienia mogą wpływać różne czynniki, takie jak pH barwnika Wrighta, bufor i roztwór do przemywania; jak również czas barwienia i utrwalania.
Dlatego każdy etap przygotowania odczynników jest kluczowy i należy go przeprowadzić z dbałością o każdy szczegół..
Materiały
Plama Wrighta. Do 100 ml wymagane jest:
Odważ 0,3 g barwnika Wrighta, odmierz 97 ml metanolu i 3 ml gliceryny.
Przygotowanie
W moździerzu umieść dużą ilość plamy Wrighta i stopniowo dodawaj glicerol, aż proszek całkowicie się rozpuści..
Następnie dodaje się metanol, miesza i wlewa do bursztynowej butelki.
Przed użyciem roztwór należy delikatnie wstrząsnąć i przefiltrować.
Buforowany roztwór buforowy
Do jednego litra wody destylowanej dodać 3,76 g hydrofosforanu disodowego (NadwaHPO4 2Hdwa0) plus 2,1 g diwodorofosforanu potasu (KHdwaPO4).
Bardzo dobrze wymieszaj, aż wszystkie włączone odczynniki zostaną rozpuszczone. Doprowadzić pH do 7,2. Wlej do szklanego słoika i trzymaj w temperaturze pokojowej.
Dodatkowe materiały potrzebne do wykonania kolorowania
Dodatkowo do wykonania techniki barwienia potrzebne są inne materiały, są to: szkiełka lub okładki obiektów, pomost do barwienia, koszulki z wodą lub buforem do prania, stoper do zapisywania czasów barwienia oraz trochę materiału do osuszania. (chłonny papier, gaza lub bawełna).
Składniki bejcy Wrighta
Metanol
Alkohol (metanol) służy jako utrwalacz rozmazu krwi na szkiełku.
Jest to w zasadzie odczynnik utrwalający redukujący, odwadniający i koagulujący. Dlatego jego funkcją jest koagulacja białek i uczynienie ich nierozpuszczalnymi, ale bez faktycznego ich denaturacji..
Metanol jest najczęściej używanym odczynnikiem utrwalającym rozmaz we wszystkich laboratoriach, ponieważ zapewnia lepsze wyniki niż etanol. Idealne stężenie to 99%.
Amortyzator
Bufor (roztwór buforowany) ma funkcję regulowania lub utrzymywania pH barwnika, ponieważ pH ustawione na 7,2 jest niezbędne, aby struktury komórkowe mogły prawidłowo wchłaniać barwniki..
Z drugiej strony, etap utrwalania metanolu odwadnia komórki, a bufor pomaga je ponownie nawodnić..
Eozyna (Y)
Eozyna ma powinowactwo do bloków budulcowych, ponieważ jest barwnikiem kwasowym. Znane są dwa rodzaje eozyny bardzo do siebie podobne, do tego stopnia, że można użyć każdego z nich, uzyskując ten sam wynik..
Jedna nazywa się eozyną Y, żółtą eozyną lub tetrabromofluoresceiną, a drugą nazywa się eozyną B, niebieskawą erytrozyną B lub dibromodinitrofluoresceiną. Jednak najczęściej stosowana jest eozyna Y.
Najważniejszą właściwością tego barwnika jest jego ujemna polaryzacja, co powoduje, że przyciąga on dodatnio naładowane struktury komórkowe.
Błękit metylenowy
To jest podstawowa kolorystyka. Jego główną właściwością jest metachromazja, czyli nie wszystkie struktury będą wybarwione na ten sam kolor, zależy to od składu chemicznego barwionych struktur..
Niektóre zmienią kolor na jasnoniebieski lub ciemnoniebieski, a inne na ciemnofioletowe lub bladoliliowe.
Technika
1-Rozprowadź próbkę tak, aby pozostała cienka błona na szkiełku lub szkiełku nakrywkowym.
2-Pozostaw do wyschnięcia na powietrzu na około 2 godziny.
3-Umieść suchy rozmaz na mostku barwiącym lub tacce do barwienia, tak aby rozprowadzona próbka była skierowana do góry..
4-Przykryj arkusz plamą Wright kropla po kropli, aż cała powierzchnia zostanie pokryta. Pozostaw na 5 - 8 minut.
5-Plama powinna całkowicie zakryć szkiełko, nie rozlewając się po krawędziach. Jeśli w czasie barwienia zacznie wyparowywać, dodaj kilka dodatkowych kropli.
6-Następnie dodaj taką samą ilość amortyzatora, lekko dmuchaj, aż pojawi się charakterystyczny metaliczny połysk. Czas od 10 do 15 minut.
7-Umyj wodą z kranu, delikatnym strumieniem, aż prześcieradło będzie różowe.
8-Gazą nasączoną alkoholem usuń barwnik przyklejony do tylnej części szkiełka.
9-Niech rozmaz wyschnie bardzo dobrze przed umieszczeniem olejku immersyjnego w celu obejrzenia go pod mikroskopem.
Użyteczność
Hematologia
Idealnie nadaje się do barwienia rozmazów krwi obwodowej, do badania rozmazów grubej krwi oraz do badania komórek z próbek szpiku kostnego.
Ze względu na właściwości chemiczne tej kombinacji barwników można łatwo rozpoznać struktury komórkowe, będąc w stanie rozróżnić różne typy obecnych komórek.
Katar
Technika ta jest bardzo przydatna do identyfikacji komórek wydzieliny z nosa (komórki nabłonka, segmentowane eozynofile, komórki polimorfojądrowe) w diagnostyce alergicznego nieżytu nosa..
parazytologia
W tym sensie był przydatny do badania Leishmania sp w histiocytach podskórnej tkanki komórkowej we wrzodach skóry. Podobnie służy do identyfikacji leukocytów w próbkach kału (leukogram kału).
W takim przypadku lekarz powinien wiedzieć, czy leukocytoza obecna w kale jest polimorfojądrowa czy jednojądrzasta. To odkrycie w leukogramie kału wskaże, czy jest to odpowiednio infekcja bakteryjna czy wirusowa..
Z drugiej strony pasożyty krążące we krwi można znaleźć w erytrocytach lub w osoczu. Poszukiwane pasożyty to Plasmodium spp, Trypanosoma cruzii i filariae, aw weterynarii jest to przydatne w poszukiwaniu Theileria equi Y Babesia caballi, czynniki wywołujące bebezjozę, zwłaszcza u koniowatych.
Barwienie Wrighta, a także barwienie Giemsa umożliwiają odróżnienie hemopasożytów od normalnych składników komórkowych. Można do tego wykorzystać dwa rodzaje spreadów:
Dobrze się rozprowadza
Krew jest rozprowadzana w postaci cienkiej warstwy na szkiełku. Barwione barwnikiem Wrighta, ujawniające cechy jądra i cytoplazmy.
Gruba kropla
Metodologia ta służy do badania obecności pasożytów w większej ilości krwi..
Aby to zrobić, na szkiełku umieszcza się dużą kroplę krwi. Tam należy go zdefibrylować, wykonując coraz większe koła od środka na zewnątrz, używając krawędzi innego szkiełka..
Wreszcie, aby móc obserwować pasożyty w gęstym rozmazie, erytrocyty muszą zostać poddane lizie wodą..
Infekcje dróg oddechowych
Na poziomie oddechowym technika ta jest również przydatna, ponieważ komórki obecne w próbkach plwociny, popłuczynach oskrzelowych czy oskrzelowo-pęcherzykowych są ważne dla ustalenia rozpoznania..
Podobnie można tutaj rozróżnić komórki polimorfojądrzaste i komórki jednojądrzaste..
Bakteriologia
Zastosowanie tej techniki w bakteriologii jest ograniczone, ponieważ nie jest ona dobra do barwienia bakterii, dlatego do ich barwienia stosuje się inne specjalistyczne techniki barwienia..
Jednak był on używany do poszukiwania komórek nabłonka z ciałami inkluzyjnymi Chlamydia trachomatis w rozmazach błony śluzowej cewki moczowej lub szyjki macicy, chociaż trzeba mieć świadomość, że nie jest to najlepsza metoda.
Można również zaobserwować bakterie spiralne, takie jak Borrelia burgdorferi u zakażonych pacjentów, a także morule lub ciałka wtrętowe Ehrlichia sp w cytoplazmie limfocytów, monocytów lub neutrofili w rozmazie krwi.
Mikologia
Plik Histoplasma capsulatum jest patogennym grzybem często rozpoznawanym przez obserwację mikroskopową różnych próbek tkanek, zabarwionych barwnikiem Wrighta.
Jak obserwuje się strukturę próbki krwi za pomocą barwienia Wrighta?
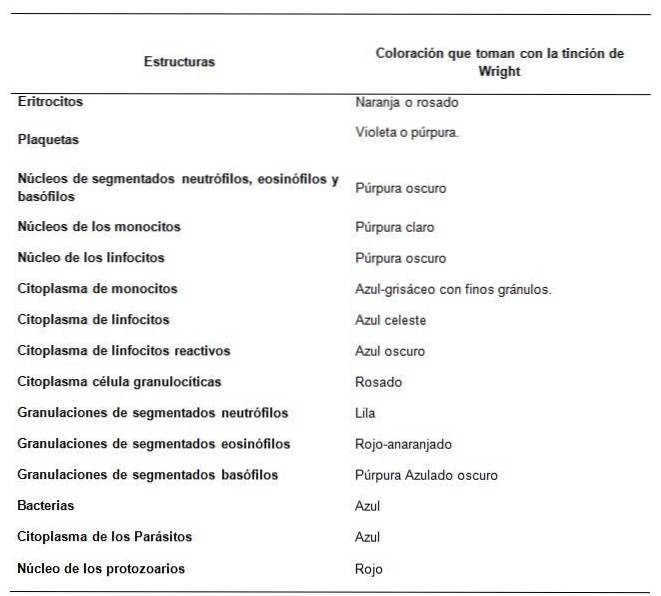
Zalecenia dotyczące dobrego barwienia
Rozmaz próbki krwi powinien samoistnie wyschnąć na powietrzu. Rozmazy powinny być jak najcieńsze, aby uzyskać lepsze utrwalenie barwnika i uniknąć przebarwień..
Aby uzyskać wysokiej jakości barwienie, zaleca się zabarwienie w ciągu dwóch godzin od przygotowania rozmazu. Z drugiej strony idealną próbką jest krew włośniczkowa, bez antykoagulantu.
Jeśli jednak używana jest krew żylna, powinna być stosowana jako antykoagulant EDTA, a nie heparyna, ponieważ ta ostatnia może deformować struktury komórkowe.
Aby uniknąć zepsucia przygotowanego barwnika należy go przechowywać w suchych miejscach.
Podczas mycia zaleca się stosowanie wody o neutralnym pH..
Wreszcie wskazane jest, aby co jakiś czas testować metody barwienia stosowane w laboratorium..
Odbywa się to poprzez barwienie próbek lub rozszerzone wzory, jako kontrola jakości. Ten krok jest ważny, ponieważ zapewnia prawidłowe przygotowanie barwienia i ustandaryzowanie czasów barwienia..
Jeśli arkusz wzoru jest słabo zabarwiony, występują problemy, które należy rozwiązać..
Typowe błędy w barwieniu Wrighta
Bardzo blade zabarwienie
Bardzo blade smugi są zwykle spowodowane bardzo krótkim czasem barwienia lub nadmiernym praniem. Koryguje się wydłużając czas kontaktu z barwnikiem lub skracając czas prania.
Barwnik wytrąca się
Obecność wytrącania się barwnika w rozmazie może mieć kilka przyczyn, jednak najczęstszymi przyczynami są: stosowanie niefiltrowanego barwnika, plamienie na nierównych mostkach barwiących, stosowanie arkuszy zabrudzonych kurzem lub tłuszczem, słabe zmywanie wykończenie barwienia.
Bardzo czerwona lub niebieska smuga
Bufor odpowiada za pH barwnika. Barwniki o pH poniżej wskazanego (kwaśne) spowodują bardzo czerwonawe rozmazania..
Jeśli pH barwnika jest powyżej (zasadowe), zostanie uzyskany bardzo niebieskawy rozmaz.
Tryb przechowywania
Odczynnik należy przechowywać w temperaturze pokojowej.
Bibliografia
- Gutiérrez V. Badanie porównawcze metody barwienia Wrighta i testu Elisa do diagnozy psiej erlichiozy w mieście San Pedro Sula w Hondurasie. 2008. Praca dyplomowa uprawniająca do nadania tytułu lekarza weterynarii. Uniwersytet San Carlos w Gwatemali.
- López-Jácome L, Hernández-Durán M, Colín-Castro C, Ortega-Peña S, Cerón-González G, Franco-Cendejas F. Podstawowe barwienia w laboratorium mikrobiologicznym. Badania niepełnosprawności. 2014; 3 (1): 10-18.
- "Plama Wrighta." Wikipedia, wolna encyklopedia. 18 maja 2018, 12:05 UTC. 8 grudnia 2018, 20:37
- Calderón A, Cardona J, Vergara Ó. Częstotliwość Babesia spp. na koniach Montería, Córdoba (Kolumbia). Rev. udcaactual ujawniający. 2013; 16 (2): 451–458.
- Forbes B, Sahm D, Weissfeld A (2009). Diagnoza mikrobiologiczna Bailey & Scott. 12 ed. Argentyna. Od redakcji Panamericana S.A.
- Retamales E, Mazo V. Institute of Public Health Government of Chile. Zalecenia dotyczące barwienia rozmazów krwi do odczytu morfologii krwi.


Jeszcze bez komentarzy