
Przepuszczalność, co to jest, schemat energii molekularnej i ćwiczeń
Plik przepuszczalność Optyczny jest ilorazem natężenia światła wychodzącego i natężenia światła padającego na próbkę półprzezroczystego roztworu, który został oświetlony światłem monochromatycznym..
Nazywa się fizyczny proces przechodzenia światła przez próbkę transmisja światła i przepuszczalność jest miarą przepuszczalności światła. Przepuszczalność jest ważną wartością do określenia stężenia próbki, która jest zwykle rozpuszczana między innymi w rozpuszczalniku, takim jak woda lub alkohol..
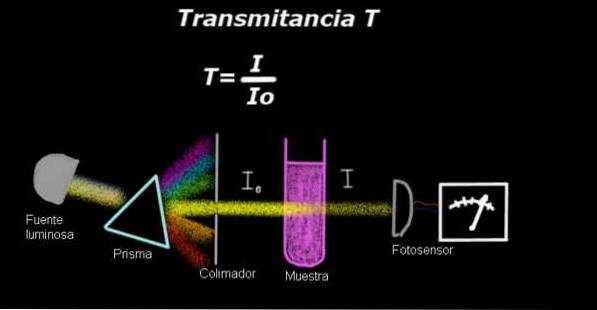
Elektrofotometr mierzy prąd proporcjonalny do natężenia światła padającego na jego powierzchnię. Aby obliczyć transmitancję, zwykle najpierw mierzy się sygnał natężenia odpowiadający samemu rozpuszczalnikowi, a ten wynik zapisuje się jako Io.
Następnie rozpuszczoną próbkę umieszcza się w rozpuszczalniku w tych samych warunkach oświetleniowych, a sygnał mierzony elektrofotometrem jest oznaczany jako ja, następnie przepuszczalność oblicza się według następującego wzoru:
T = I / Ilub
Należy zauważyć, że transmitancja jest wielkością bezwymiarową, ponieważ jest miarą światłości próbki w stosunku do intensywności przepuszczalności rozpuszczalnika..
Indeks artykułów
- 1 Czym jest przepuszczalność?
- 1.1 Absorpcja światła w medium
- 1.2 Molekularna teoria absorpcji światła
- 2 Diagram energii molekularnej
- 2.1 Czynniki, od których zależy przepuszczalność
- 3 Ćwiczenie rozwiązane
- 3.1 Ćwiczenie 1
- 4 Odnośniki
Co to jest przepuszczalność?
Absorpcja światła w medium
Kiedy światło przechodzi przez próbkę, cząsteczki absorbują część energii świetlnej. Przepuszczalność jest makroskopową miarą zjawiska zachodzącego na poziomie molekularnym lub atomowym.
Światło jest falą elektromagnetyczną, energia, którą niesie, znajduje się w polu elektrycznym i magnetycznym fali. Te oscylujące pola oddziałują z cząsteczkami substancji.
Energia przenoszona przez falę zależy od jej częstotliwości. Światło monochromatyczne ma jedną częstotliwość, podczas gdy światło białe ma zakres lub spektrum częstotliwości..
Wszystkie częstotliwości fali elektromagnetycznej poruszają się w próżni z tą samą prędkością 300 000 km / s. Jeśli oznaczymy przez do przy prędkości światła w próżni stosunek częstotliwości fa i długość fali λ to jest:
c = λ⋅f
Co do jest stałą dla każdej częstotliwości, co odpowiada jej odpowiedniej długości fali.
Do pomiaru transmitancji substancji wykorzystuje się obszary widzialnego widma elektromagnetycznego (380 do 780 nm), obszar ultrafioletu (180 do 380 nm) i obszar podczerwieni (780 nm do 5600 nm).
Prędkość propagacji światła w ośrodku materialnym zależy od częstotliwości i jest mniejsza niż do. To wyjaśnia rozpraszanie w pryzmacie, za pomocą którego można oddzielić częstotliwości tworzące białe światło..
Molekularna teoria absorpcji światła
Atomy i cząsteczki mają kwantowe poziomy energii. W temperaturze pokojowej cząsteczki mają najniższy poziom energii.
Foton to cząstka kwantowa związana z falą elektromagnetyczną. Energia fotonu jest również kwantowana, to znaczy foton o częstotliwości fa ma energię podaną przez:
E = h⋅f
gdzie godz jest stałą Plancka, której wartość wynosi 6,62 × 10 ^ -34 J⋅s.
Światło monochromatyczne to wiązka fotonów o określonej częstotliwości i energii.
Cząsteczki absorbują fotony, gdy ich energia odpowiada różnicy niezbędnej do podniesienia cząsteczki na wyższy poziom energii.
Przejścia energii w wyniku absorpcji fotonów w cząsteczkach mogą być kilku typów:
1- Przejścia elektronowe, kiedy elektrony orbitali molekularnych przechodzą na orbitale o wyższej energii. Te przejścia zwykle występują w zakresie widzialnym i ultrafioletowym i są najważniejsze.
2- Przejścia wibracyjne, energie wiązań molekularnych są również kwantowane, a kiedy foton z obszaru podczerwieni jest absorbowany, cząsteczka przechodzi do wyższego stanu wibracji.
3- Przejścia rotacyjne, kiedy absorpcja fotonu prowadzi cząsteczkę do stanu rotacyjnego o wyższej energii.
Diagram energii cząsteczkowej
Te przejścia najlepiej zrozumieć za pomocą diagramu energii molekularnej pokazanego na rysunku 2:
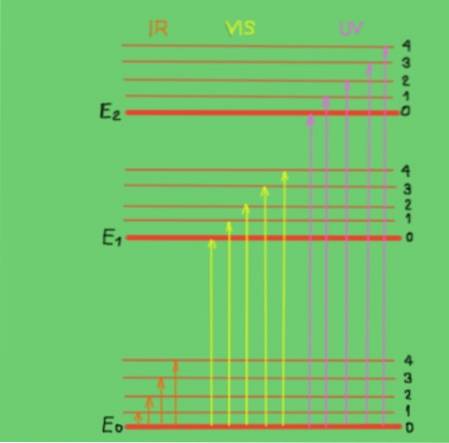
Na diagramie poziome linie przedstawiają różne poziomy energii molekularnej. Linia E0 to podstawowy lub niższy poziom energii. Poziomy E1 i E2 to wzbudzone poziomy wyższej energii. Poziomy E0, E1, E2 odpowiadają stanom elektronowym cząsteczki.
Podpoziomy 1, 2, 3, 4 na każdym poziomie elektronicznym odpowiadają różnym stanom wibracyjnym odpowiadającym każdemu poziomowi elektronicznemu. Każdy z tych poziomów ma subtelniejsze podziały, które nie są pokazane jako odpowiadające stanom rotacyjnym związanym z każdym poziomem wibracyjnym..
Diagram przedstawia pionowe strzałki przedstawiające energię fotonów w zakresie podczerwieni, widzialnego i ultrafioletu. Jak widać, fotony podczerwone nie mają wystarczającej energii, aby promować przejścia elektroniczne, podczas gdy promieniowanie widzialne i ultrafioletowe tak..
Kiedy padające fotony wiązki monochromatycznej zbiegają się pod względem energii (lub częstotliwości) z różnicą energii między stanami energii molekularnej, następuje absorpcja fotonów..
Czynniki, od których zależy przepuszczalność
Zgodnie z tym, co zostało powiedziane w poprzedniej sekcji, przepuszczalność będzie wtedy zależeć od kilku czynników, wśród których możemy wymienić:
1- Częstotliwość, z jaką próbka jest oświetlana.
2- Rodzaj analizowanych cząsteczek.
3- Stężenie roztworu.
4- Długość drogi pokonywanej przez wiązkę światła.
Dane eksperymentalne wskazują, że transmitancja T maleje wykładniczo wraz ze stężeniem do i z długością L ścieżki optycznej:
T = 10-a⋅C⋅L
W powyższym wyrażeniu do jest stałą zależną od częstotliwości i rodzaju substancji.
Ćwiczenie rozwiązane
Ćwiczenie 1
Standardowa próbka określonej substancji ma stężenie 150 mikromoli na litr (μM). Gdy mierzy się jego przepuszczalność światłem o długości 525 nm, uzyskuje się transmitancję równą 0,4..
Inna próbka tej samej substancji, ale o nieznanym stężeniu, ma transmitancję równą 0,5, mierzoną przy tej samej częstotliwości i przy tej samej grubości optycznej..
Oblicz stężenie drugiej próbki.
Odpowiedź
Przepuszczalność T spada wykładniczo wraz ze stężeniem C:
T = 10-b⋅L
Jeśli weźmie się logarytm poprzedniej równości, pozostaje:
log T = -b⋅C
Dzieląc element przez członka, poprzednia równość zastosowana do każdej próbki i rozwiązanie dla nieznanego stężenia pozostaje:
C2 = C1⋅ (log T2 / log T1)
C2 = 150 μM⋅ (log 0,5 / log 0,4) = 150 μM⋅ (-0,3010 / -0,3979) = 113,5 μM
Bibliografia
- Atkins, P. 1999. Physical Chemistry. Wydania Omega. 460-462.
- Przewodnik. Przepuszczalność i absorbancja. Odzyskany z: quimica.laguia2000.com
- Toksykologia środowiskowa. Przepuszczalność, absorbancja i prawo Lamberta. Odzyskany z: repositorio.innovacionumh.es
- Fizyczna przygoda. Absorbancja i przepuszczalność. Odzyskany z: rpfisica.blogspot.com
- Spektrofotometria. Źródło: chem.libretexts.org
- Toksykologia środowiskowa. Przepuszczalność, absorbancja i prawo Lamberta. Odzyskany z: repositorio.innovacionumh.es
- Wikipedia. Przepuszczalność. Odzyskane z: wikipedia.com
- Wikipedia. Spektrofotometria. Odzyskane z: wikipedia.com


Jeszcze bez komentarzy