
Struktura tlenku fosforu (v), właściwości, otrzymywanie, zastosowania, zagrożenia

Plik tlenek fosforu (v) Jest to nieorganiczna substancja stała utworzona przez fosfor (P) i tlen (O). Jej wzór empiryczny to PdwaLUB5, podczas gdy jego prawidłowy wzór cząsteczkowy to P4LUB10. Jest to bardzo higroskopijna biała substancja stała, to znaczy bardzo łatwo może wchłaniać wodę z powietrza, natychmiast z nią reagując. Reakcja może być niebezpieczna, ponieważ powoduje szybki wzrost temperatury.
Wysoka skłonność do wchłaniania wody sprawiła, że znalazł zastosowanie jako środek osuszający w laboratoriach chemicznych, a także jako odwadniacz niektórych związków, czyli do usuwania wody z jej molekuł..

Tlenek fosforu (v) jest również używany do przyspieszania reakcji wiązania różnych cząsteczek węglowodorów, reakcji nazywanej kondensacją. Ponadto pozwala na przekształcenie niektórych kwasów organicznych w estry.
Był używany m.in. do rafinacji benzyny, do przygotowania kwasu fosforowego H.3PO4, między innymi do otrzymywania związków opóźniających pożar, do produkcji szkła do zastosowań próżniowych.
Tlenek fosforu (v) należy przechowywać w szczelnie zamkniętych pojemnikach, aby zapobiec jego kontaktowi z wilgocią zawartą w powietrzu. Działa żrąco i może uszkodzić oczy, skórę i błony śluzowe..
Indeks artykułów
- 1 Struktura
- 2 Nazewnictwo
- 3 Właściwości
- 3.1 Stan fizyczny
- 3.2 Masa cząsteczkowa
- 3.3 Temperatura topnienia
- 3.4 Temperatura sublimacji
- 3.5 Gęstość
- 3.6 Rozpuszczalność
- 3.7 Właściwości chemiczne
- 3.8 Inne właściwości
- 4 Otrzymywanie
- 4.1 Obecność w przyrodzie
- 5 zastosowań
- 5.1 Jako środek odwadniający i suszący
- 5.2 W reakcjach chemii organicznej
- 5.3 W rafinacji paliw
- 5.4 W różnych zastosowaniach
- 6 Ryzyka
- 7 Referencje
Struktura
Tlenek fosforu (v) składa się z fosforu (P) i tlenu (O), przy czym fosfor ma wartościowość +5, a tlen -2. Cząsteczka tlenku fosforu (v) ma cztery atomy fosforu i dziesięć atomów tlenu, dlatego jej prawidłowy wzór cząsteczkowy to P4LUB10.
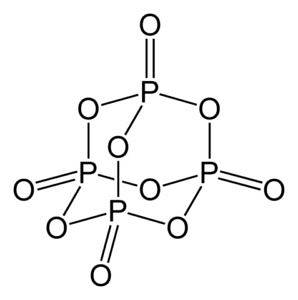
Występuje w trzech formach krystalicznych, jako bezpostaciowy proszek oraz w postaci szklistej (jako szkło). W sześciokątnej postaci krystalicznej każdy z atomów fosforu znajduje się na wierzchołkach czworościanu..
Nomenklatura
- Tlenek fosforu (v)
- Pięciotlenek fosforu
- Pięciotlenek difosforu
- Pięciotlenek fosforu
- Bezwodnik fosforowy
- Dekatlenek tetrafosforu
Nieruchomości
Stan fizyczny
Krystaliczne białe ciało stałe. Najbardziej rozpowszechnioną formą są sześciokątne kryształy.
Waga molekularna
283,89 g / mol
Temperatura topnienia
562 ºC
Temperatura sublimacji
360 ºC przy ciśnieniu 1 atmosfery. Oznacza to, że w tej temperaturze przechodzi ze stanu stałego w gaz bez przechodzenia w stan ciekły.
Gęstość
2,30 g / cm3
Rozpuszczalność
Bardzo dobrze rozpuszczalny w wodzie. Rozpuszczalny w kwasie siarkowym. Nierozpuszczalny w acetonie i amoniaku.
Właściwości chemiczne
Tlenek fosforu (v) bardzo szybko wchłania wodę z powietrza i reaguje z nią, tworząc kwas fosforowy H.3PO4. Ta reakcja jest egzotermiczna, co oznacza, że podczas reakcji wytwarzane jest ciepło..
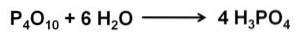
Reakcja P.4LUB10 z wodą prowadzi do powstania mieszaniny kwasów fosforowych, której skład zależy od ilości wody i warunków.
Reakcja z alkoholami prowadzi do powstania estrów kwasu fosforowego lub kwasów polimerowych w zależności od warunków eksperymentu..
P.4LUB10 + 6 ROH → 2 (RO)dwaPO.OH + 2 RO.PO (OH)dwa
Z tlenkami zasadowymi tworzy fosforany w postaci stałej.
Działa korodująco. Może niebezpiecznie reagować z kwasem mrówkowym i zasadami nieorganicznymi, takimi jak wodorotlenek sodu (NaOH), tlenek wapnia (CaO) lub węglan sodu NadwaWSPÓŁ3.
Jeśli wlejesz roztwór kwasu nadchlorowego HClO4 i chloroform CHCI3 w tlenku fosforu (v) P.4LUB10 następuje gwałtowna eksplozja.
Inne właściwości
Nie jest łatwopalny. Nie sprzyja spalaniu. Jednak jego reakcja z wodą jest tak gwałtowna i egzotermiczna, że może wystąpić ryzyko pożaru..
Otrzymywanie
Można go otrzymać przez bezpośrednie utlenianie fosforu w strumieniu suchego powietrza. Fosfor w kontakcie z nadmiarem tlenu utlenia się tworząc tlenek fosforu (v).
P.4 + 5 Odwa → P.4LUB10
Obecność w przyrodzie
Tlenek fosforu (v) znajduje się w minerałach, takich jak ilmenit, rutyl i cyrkon.
Ilmenit to minerał zawierający żelazo i tytan, a czasem tlenek fosforu (v) w stężeniach wahających się od 0,04 do 0,33% wagowych. Rutyl jest minerałem tlenku tytanu i może zawierać około 0,02% wagowych PdwaLUB5.
Piaski cyrkonowe (minerał pierwiastka cyrkonu) zawierają tlenek fosforu (v) w ilości 0,05-0,39% masy.
Aplikacje
Jako środek odwadniający i suszący
Ze względu na wielką chciwość wody jest jednym z najbardziej znanych środków odwadniających i bardzo skutecznym w temperaturach poniżej 100 ° C..
Może usuwać wodę z substancji, które same są uważane za środki odwadniające. Na przykład można usunąć wodę z kwasu siarkowego H.dwapołudniowy zachód4 przekształcając go w SO3 i kwas azotowy HNO3 przekształcając go w NdwaLUB5.

Zasadniczo może wysuszyć wszystkie te ciecze i gazy, z którymi nie reaguje, dzięki czemu pozwala usunąć ślady wilgoci z systemów próżniowych.
W reakcjach chemii organicznej
Tlenek fosforu (v) służy do zamykania pierścieni związków organicznych i innych reakcji kondensacji.
Pozwala na estryfikację kwasów organicznych z możliwością rozróżnienia między pierwszorzędowymi alifatycznymi kwasami karboksylowymi (łańcuch węglowy bez pierścieni z grupą -COOH na jednym końcu) i kwasami aromatycznymi (grupa -COOH przyłączona do pierścienia benzenowego), gdyż te ostatnie nie reagują.
Służy również do usuwania cząsteczki H.dwaO z amidów R (C = O) NHdwa i przekształca je w nitryle R-CN. Ponadto katalizuje lub przyspiesza reakcje utleniania, odwodornienia i polimeryzacji asfaltów.

W rafinacji paliw
Od lat 30-tych XX wieku niektóre badania wykazały, że tlenek fosforu (v) wywierał działanie rafinujące na benzynę, zwiększając jej liczbę oktanową.
Oczyszczające działanie P.4LUB10 wynika to głównie z reakcji kondensacji (połączenie różnych cząsteczek), a nie polimeryzacji (połączenie równych cząsteczek).
P4LUB10 przyspiesza bezpośrednie alkilowanie węglowodorów aromatycznych olefinami, przemianę olefin do naftenów i ich częściową polimeryzację. Reakcja alkilowania zwiększa liczbę oktanową benzyny.
W ten sposób uzyskuje się rafinowaną benzynę wysokiej jakości.

W różnych zastosowaniach
Tlenek fosforu (v) jest używany do:
- Przygotuj kwas fosforowy H.3PO4
- Uzyskaj estry akrylanowe i środki powierzchniowo czynne
- Przygotuj estry fosforanowe, które są używane jako środki zmniejszające palność, rozpuszczalniki i rozcieńczalniki
- Konwersja trichlorku fosforu do tlenochlorku fosforu
- Odczynnik laboratoryjny
- Produkcja specjalnego szkła do lamp próżniowych
- Zwiększyć temperaturę topnienia asfaltu
- Służy jako standardowa cząsteczka w oznaczaniu fosforu lub fosforanów w fosforytach, nawozach i cemencie portlandzkim w postaci fosforudwaLUB5
- Popraw wiązania między niektórymi polimerami a warstwą kości słoniowej, którą mają zęby

Ryzyka
Tlenek fosforu (v) należy przechowywać w szczelnych pojemnikach oraz w chłodnych, suchych i dobrze wentylowanych miejscach.
Służy to zapobieganiu kontaktowi z wodą, ponieważ może z nią gwałtownie reagować, wytwarzając dużo ciepła, aż do spalenia pobliskich materiałów, które są palne..
Pył tlenku fosforu (v) działa drażniąco na oczy i drogi oddechowe oraz działa żrąco na skórę. Może powodować oparzenia oczu. Spożycie powoduje śmiertelne oparzenia wewnętrzne.
Bibliografia
- NAS. National Library of Medicine. (2019). Bezwodnik fosforowy. Odzyskany z pubchem.ncbi.nlm.nih.gov.
- Nayler, P. (2001). Bitumeny: zmodyfikowane. Modyfikacja chemiczna. W Encyklopedii materiałów: nauka i technologia. Odzyskany z sciencedirect.com.
- Malishev, B.W. (1936). Pentoksyd fosforu jako czynnik rafinacyjny do benzyny. Chemia przemysłowa i inżynieryjna 1936, 28, 2, 190-193. Odzyskany z pubs.acs.org.
- Epps Jr. E.A. (1950). Fotometryczne oznaczanie dostępnego pięciotlenku fosforu w nawozach. Analytical Chemistry 1950, 22, 8, 1062-1063. Odzyskany z pubs.acs.org.
- Banerjee, A. i in. (1983). Zastosowanie pięciotlenku fosforu: estryfikacja kwasów organicznych. J. Org. Chem., 1983,48, 3108-3109. Odzyskany z pubs.acs.org.
- Cotton, F. Albert i Wilkinson, Geoffrey. (1980). Zaawansowana chemia nieorganiczna. Czwarta edycja. John Wiley & Sons.
- Kirk-Othmer (1994). Encyklopedia technologii chemicznej. Czwarta edycja. John Wiley & Sons.
- Ogliari, F.A. et al. (2008). Synteza monomerów fosforanowych i wiązanie z zębiną: Metody estryfikacji i zastosowanie pięciotlenku fosforu. Journal of Dentistry, tom 36, wydanie 3, marzec 2008, strony 171-177. Odzyskany z sciencedirect.com.


Jeszcze bez komentarzy