
Charakterystyka, struktura, funkcje peroksydazy jodkowej
Plik peroksydaza jodkowa o peroksydaza tarczycy (TPO) to hemoglikoproteina należąca do rodziny peroksydaz ssaków (takich jak mieloperoksydaza, laktoperoksydaza i inne), która uczestniczy w szlaku syntezy hormonów tarczycy.
Jej główną funkcją jest „jodowanie” reszt tyrozyny w tyrooglobulinie oraz tworzenie 3-3'-5-trijodotyroniny (T3) i tyroksyny (T4) poprzez reakcję „sprzęgania”. Wewnątrzcząsteczkowe jodowane tyrozyny.
Trójjodotyronina i tyroksyna to dwa hormony wytwarzane przez tarczycę, które pełnią podstawowe funkcje w rozwoju ssaków, różnicowaniu się i metabolizmie. Jego mechanizm działania zależy od interakcji jego receptorów jądrowych z określonymi sekwencjami genów docelowych genów..
Istnienie enzymu peroksydazy jodkowej zostało potwierdzone w latach sześćdziesiątych XX wieku przez różnych autorów, a obecnie poczyniono znaczne postępy w określaniu jego struktury, funkcji i właściwości kodującego go genu. W różnych organizmach.
W dużej części literatury związanej z tym enzymem jest on znany jako mikrosomalny „autoantygen” i jest powiązany z niektórymi autoimmunologicznymi chorobami tarczycy..
Enzym ten, dzięki swoim właściwościom immunogennym, jest cząsteczką docelową lub docelową dla przeciwciał obecnych w surowicy wielu pacjentów z patologiami tarczycy, a jego wady mogą prowadzić do niedoborów hormonalnych, które mogą mieć znaczenie patofizjologiczne.
Indeks artykułów
- 1 Funkcje
- 1.1 Regulacja ekspresji
- 2 Struktura
- 3 Funkcje
- 3.1 Jaka jest synteza hormonu tarczycy?
- 4 Powiązane choroby
- 5 Referencje
Charakterystyka
Peroksydaza jodkowa jest kodowana przez gen umiejscowiony na chromosomie 2 u ludzi, który mierzy ponad 150 kpz i składa się z 17 eksonów i 16 intronów..
To białko przezbłonowe, z pojedynczym segmentem zanurzonym w błonie, jest blisko spokrewnione z mieloperoksydazą, z którą ma ponad 40% podobieństwa sekwencji aminokwasów.
Jej synteza zachodzi w poliryboosomach (zbiorze rybosomów odpowiedzialnych za translację tego samego białka), a następnie jest wprowadzana do błony retikulum endoplazmatycznego, gdzie podlega procesowi glikozylacji.
Po zsyntetyzowaniu i glikozylacji peroksydaza jodkowa jest transportowana do wierzchołkowego bieguna tyreocytów (komórek tarczycy lub komórek tarczycy), gdzie jest w stanie odsłonić swoje centrum katalityczne do światła pęcherzykowego tarczycy..
Regulacja ekspresji
Ekspresja genu kodującego peroksydazę tarczycową lub peroksydazę jodkową jest kontrolowana przez specyficzne dla tarczycy czynniki transkrypcyjne, takie jak TTF-1, TTF-2 i Pax-8.
Elementy genetyczne, które umożliwiają zwiększenie lub wzmocnienie ekspresji tego genu u ludzi, opisano w regionach otaczających jego koniec 5 ', zwykle między pierwszymi 140 parami zasad tego „flankującego” regionu..
Istnieją również elementy, które tłumią lub zmniejszają ekspresję tego białka, ale w przeciwieństwie do „wzmacniaczy”, zostały one opisane poniżej sekwencji genu..
Duża część regulacji ekspresji genetycznej peroksydazy jodkowej zachodzi w sposób specyficzny dla tkanki, a to zależy od działania elementów wiążących DNA, które działają na cis, takie jak czynniki transkrypcyjne TTF-1 i inne.
Struktura
To białko o aktywności enzymatycznej ma około 933 reszt aminokwasowych i zewnątrzkomórkowy koniec C o długości 197 aminokwasów, który pochodzi z ekspresji innych modułów genów, które kodują inne glikoproteiny..
Jego masa cząsteczkowa wynosi około 110 kDa i należy do grupy glikozylowanych białek transbłonowych typu 1, ponieważ ma glikozylowany segment transbłonowy i grupę hemową w miejscu aktywnym..
Struktura tego białka ma co najmniej jeden mostek dwusiarczkowy w obszarze zewnątrzkomórkowym, który tworzy charakterystyczną zamkniętą pętlę, która jest odsłonięta na powierzchni tyrocytów..
funkcje
Główna funkcja fizjologiczna peroksydazy jodkowej związana jest z jej udziałem w syntezie hormonu tarczycy, gdzie katalizuje „jodowanie” reszt tyrozynowych monoiodotyrozyny (MIT) i dijodotyrozyny (DIT), oprócz sprzęgania reszt jodotyrozyny w tyroglobulina.
Jaka jest synteza hormonu tarczycy?
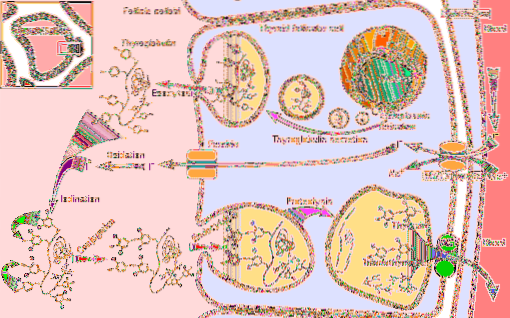
Aby zrozumieć funkcję enzymu peroksydazy tarczycy, należy rozważyć etapy syntezy hormonalnej, w których bierze udział:
1-Rozpoczyna się transportem jodku do tarczycy i trwa dalej
2-Wytwarzanie środka utleniającego, takiego jak nadtlenek wodoru (H2O2)
3-Następnie syntetyzowane jest białko receptorowe tyroglobulina
4-Jodek jest następnie utleniany do wyższego stanu walencyjnego
5-Jodek wiąże się z resztami tyrozyny obecnymi w tyreoglobulinie
6-W tyreoglobulinie jodotyroniny (rodzaj hormonów tarczycy) powstają przez sprzężenie reszt jodotyrozyny
Następnie 7-Tyreoglobulina jest przechowywana i rozszczepiana
8-Jod jest usuwany z wolnych jodotyrozyn i na koniec,
9-tyroksyna i trójjodotyronina są uwalniane do krwi; Hormony te wywierają swoje działanie poprzez interakcję z ich specyficznymi receptorami, które znajdują się na błonie jądrowej i które są zdolne do interakcji z docelowymi sekwencjami DNA, pełniąc rolę czynników transkrypcyjnych..
Jak można wywnioskować ze znajomości funkcji dwóch hormonów, w których syntezie bierze udział (T3 i T4), peroksydaza jodkowa ma ważne implikacje na poziomie fizjologicznym..
Brak obu hormonów podczas rozwoju człowieka powoduje zaburzenia wzrostu i upośledzenie umysłowe, a także zaburzenia równowagi metabolicznej w życiu dorosłym.
Powiązane choroby
Peroksydaza jodkowa jest jednym z głównych autoantygenów tarczycy u ludzi i jest związana z cytotoksycznością, w której pośredniczy układ dopełniacza. Jego funkcja jako autoantygenu jest podkreślona u pacjentów z autoimmunologicznymi chorobami tarczycy.
Na przykład choroba dny moczanowej jest spowodowana niedoborem zawartości jodu podczas syntezy hormonów w tarczycy, co z kolei jest związane z niedoborem jodowania tyreoglobuliny w wyniku pewnych defektów peroksydazy jodkowej..
Niektóre raki charakteryzują się zmienionymi funkcjami peroksydazy jodkowej, to znaczy poziomy aktywności tego enzymu są znacznie niższe niż u pacjentów bez raka.
Jednak badania potwierdziły, że jest to wysoce zmienna cecha, która zależy nie tylko od pacjenta, ale także od rodzaju raka i dotkniętych nim regionów..
Bibliografia
- Degroot, L. J. i Niepomniszcze, H. (1977). Biosynteza hormonu tarczycy: aspekty podstawowe i kliniczne. Postęp w endokrynologii i metabolizmie, 26(6), 665-718.
- Fragu, P. i Nataf, B. M. (1976). Aktywność ludzkiej peroksydazy tarczycy w łagodnych i złośliwych zaburzeniach tarczycy. Towarzystwo Endokrynologiczne, Cztery pięć(5), 1089-1096.
- Kimura, S., & Ikeda-saito, M. (1988). Ludzka mieloperoksydaza i peroksydaza tarczycy, dwa enzymy o oddzielnych i wyraźnych funkcjach fizjologicznych, są ewolucyjnie powiązanymi członkami tej samej rodziny genów. Białka: struktura, funkcja i bioinformatyka, 3, 113-120.
- Nagasaka, A., Hidaka, H. i Ishizuki, Y. (1975). Badania ludzkiej peroksydazy jodkowej: jej aktywność w różnych chorobach tarczycy. Klinika Chimica Acta, 62, 1-4.
- Ruf, J. i Carayon, P. (2006). Strukturalne i funkcjonalne aspekty peroksydazy tarczycowej. Archiwa Biochemii i Biofizyki, 445, 269-277.
- Ruf, J., Toubert, M., Czarnocka, B., Durand-gorde, M., Ferrand, M. i Carayon, P. (2015). Związek między strukturą immunologiczną a właściwościami biochemicznymi ludzkiej peroksydazy tarczycowej. Recenzje endokrynologiczne, 125(3), 1211-1218.
- Taurog, A. (1999). Ewolucja molekularna peroksydazy tarczycowej. Biochimie, 81, 557-562.
- Zhang, J., & Lazar, M. A. (2000). Mechanizm działania hormonów tarczycy. Annu. Rev. Physiol., 62(1), 439-466.



Jeszcze bez komentarzy