
Struktura, właściwości, zastosowania i zagrożenia octanu amonu
Plik octan amonu jest solą nieorganiczną, której wzór chemiczny to NH4CH3COOH. Pochodzi z mieszaniny kwasu octowego obecnego w occie handlowym w stężeniu 5% i amoniaku. Obie substancje wyjściowe mają charakterystyczny zapach, więc można się zorientować, dlaczego ta sól pachnie jak ocet-amoniak.
Jednak najbardziej wyróżniającym się aspektem tej soli nie jest jej zapach, ale niska temperatura topnienia. Jest tak niska, że w każdym laboratorium można by go otrzymać w wersji płynnej, w której jony swobodnie przepływają, przenosząc ładunki elektryczne..

Z drugiej strony octan amonu rozpływa się; to znaczy pochłania wodę lub wilgoć z otoczenia, aż do całkowitego rozpuszczenia. Dlatego chociaż w stanie bezwodnym jego kryształy są białe, szybko stają się jasne (jak te w zlewce na powyższym obrazku).
Będąc stałym źródłem amoniaku, należy obchodzić się z nim w taki sposób, aby zminimalizować wdychanie jego oparów. Ale pomimo tej negatywnej cechy NH4CH3COOH jest przydatny do przygotowywania roztworów buforowych, które konserwują żywność, a także jest składnikiem niektórych rozpuszczalników do ekstrakcji białek.
Indeks artykułów
- 1 Struktura octanu amonu
- 1.1 Inne kompozycje i woda
- 2 Właściwości
- 2.1 Wygląd fizyczny
- 2.2 Masa molowa
- 2.3 Gęstość
- 2.4 Temperatura topnienia
- 2.5 Rozpuszczalność
- 2.6 Stabilność
- 2,7 pKa
- 2.8 Standardowa entalpia formacji
- 3 Zastosowania
- 3.1 Analityczne
- 3.2 Średni przewodnik
- 3.3 Bufor
- 3.4 Na lodzie i glebie
- 3.5 Środek strącający
- 3.6 Medycyna
- 4 Ryzyka
- 5 Referencje
Struktura octanu amonu
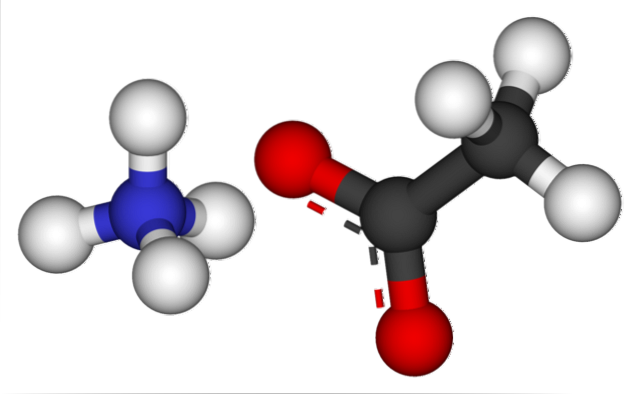
Powyższy obrazek przedstawia jony tworzące octan amonu w modelu kulek i prętów. Po lewej stronie znajduje się kation o geometrii czworościennej, NH4+, podczas gdy po jego prawej stronie anion cząsteczkowy z dwoma elektronami zdelokalizowanymi między dwoma atomami tlenu, CH3GRUCHAĆ- (przerywana linia między czerwonymi kulami).
Więc oba jony, NH4+ i CH3GRUCHAĆ-, są trzymane razem przez przyciąganie elektrostatyczne, które wraz z odpychaniem między równymi ładunkami ostatecznie definiuje kryształ. Ten kryształ octanu amonu ma strukturę rombową, którą można było zaobserwować w mikroskopijnych próbkach lub nawet w widocznych rozmiarach..
W przypadku tej soli ważne są nie tylko wiązania jonowe, ale także wiązania wodorowe. NH4+ możesz przekazać do czterech z tych mostów; to znaczy w każdym z wierzchołków jego czworościanu znajduje się atom tlenu z CH3GRUCHAĆ- sąsiad (H.3N+-H- OCOCH3).
W teorii siły wewnątrz twoich kryształów powinny być wtedy bardzo silne; ale doświadczalnie dzieje się odwrotnie, ponieważ topi się tylko w 114 ° C. Dlatego wiązania wodorowe nie kompensują słabego wiązania jonowego ani niskiej energii sieci krystalicznej rombowego kryształu NH.4CH3GRUCHAĆ.
Inne kompozycje i woda
Pierwotnie mówiono, że octan amonu jest przygotowywany przez zmieszanie kwasu octowego i amoniaku. Dlatego sól można również wyrazić jako: NH3CH3COOH. Zatem w zależności od składu można otrzymać inne struktury: NH32CH3COOH lub NH35CH3Na przykład COOH.
Wspomniano również, że pochłania sporo wilgoci. W ten sposób włącza cząsteczki wody do swoich kryształów, które hydrolizują, dając NH3 lub CH3COOH; dlatego sól wydziela zapach amoniaku lub octu.
Nieruchomości
Wygląd fizyczny
Rozpływające się białe kryształy o zapachu octu i amoniaku.
Masa cząsteczkowa
77,083 g / mol.
Gęstość
1073 g / ml w 25 ° C.
Temperatura topnienia
114 ° C Ta wartość jest znacznie niższa w porównaniu z innymi solami lub związkami jonowymi. Ponadto nie ma temperatury wrzenia z powodu tworzenia się amoniaku, co oznacza rozkład soli..
Rozpuszczalność
143 g / 100 ml w temperaturze 20 ° C. Zwróć uwagę na jego niezwykłą rozpuszczalność w wodzie, która świadczy o powinowactwie cząsteczek wody do jonów NH.4+ i CH3GRUCHAĆ-, nawilżając je w sferach wodnych.
Jego rozpuszczalność nie jest taka w mniej polarnych rozpuszczalnikach. Na przykład w 100 ml metanolu w temperaturze 15 ° C rozpuszcza się 7,89 g NH4CH3GRUCHAĆ.
Stabilność
Jest rozpuszczalny, dlatego należy unikać przechowywania go w wilgotnych pomieszczeniach. Ponadto wchłaniając wodę uwalnia amoniak i dlatego ulega rozkładowi.
pKa
9.9.
Ta stała odpowiada kwasowości jonu amonowego:
NH4+ + b <=> NH3 + HB
Gdzie HB jest słabym kwasem. Jeśli zasada B dotyczy wody, będzie miała reakcję hydrolizy:
NH4+ + H.dwaLUB <=> NH3 + H.3LUB+
W którym gatunek H.3LUB+ określa pH roztworu.
Z drugiej strony octan przyczynia się również do pH:
CH3GRUCHAĆ- + H.dwaLUB <=> CH3COOH + OH-
Zatem oba gatunki H.3LUB+ i OH- są neutralizowane dając neutralne pH 7. Jednak według Pubchem wysoko stężone roztwory octanu amonu mają kwaśne pH; co oznacza, że przeważa hydroliza NH4+ na CH3GRUCHAĆ-.
Standardowa entalpia formacji
ΔfaH.298 = -615 kJ / mol.
Aplikacje
Analityczny
Wodne roztwory octanu sodu pozwalają na rozpuszczenie siarczanów ołowiu, żelaza i cynku w celu późniejszego określenia ich stężenia metodą atomowej spektroskopii absorpcyjnej.
Średni przewodnik
Ponieważ topi się w niskiej temperaturze w porównaniu z innymi solami, jego ciecz może służyć do przewodzenia prądu elektrycznego, który zapala obwód żarówki..
Bufor
Może regulować zmiany pH w zakresie kwaśnym lub zasadowym, co służy do utrzymania stałego pH np. W mięsach, czekoladach, serach, warzywach lub innych produktach spożywczych.
Na lodzie i glebach
Jest to stosunkowo tania i biodegradowalna sól, używana do odladzania oblodzonych dróg. Podobnie, ponieważ jest źródłem azotu rozpuszczalnego w wodzie, służy do celów rolniczych do oznaczania poziomu potasu..
Środek strącający
Sól ta służy do wytrącania białek do analizy chromatograficznej..
Lekarstwo
Octan amonu działa jako środek moczopędny w weterynarii, a także jest niezbędną solą do syntezy insuliny i penicyliny.
Ryzyka
Poniżej, na końcu, wymieniono niektóre zagrożenia lub negatywne konsekwencje spowodowane przez octan amonu:
- Może powodować łagodne podrażnienie skóry, ale nie jest przez nią wchłaniany.
- Po spożyciu powoduje rozstrój żołądka, biegunkę, diurezę, niepokój, zwiększoną potrzebę oddawania moczu, drżenie i inne objawy zatrucia amoniakiem, a także uszkodzenie wątroby.
- Wdychanie podrażnia nos, gardło i płuca.
Poza tym nie wiadomo, czy może powodować raka, i wykluczone jest jakiekolwiek ryzyko pożaru tej soli (przynajmniej w normalnych warunkach przechowywania)..
Bibliografia
- Inger Nahringbauer. (1967). Badania wiązania wodorowego. XIV. Struktura krystaliczna octanu amonu. Institute of Chemistry, University of Uppsala, Uppsala, Szwecja. Acta Cryst. 23, 956.
- Narodowe Centrum Informacji Biotechnologicznej. (2019). Octan amonu. Baza danych PubChem. CID = 517165. Odzyskany z: pubchem.ncbi.nlm.nih.gov
- Sullivan Randy. (2012). Przewodnictwo octanu amonu. Odzyskany z: chemdemos.uoregon.edu
- Viachem, Ltd. (s.f.). Octan amonu. Odzyskany z: viacheminc.com
- Wikipedia. (2019). Octan amonu. Odzyskane z: en.wikipedia.org
- Departament Zdrowia stanu New Jersey. (2012). Octan amonu - Arkusz informacyjny o niebezpiecznych substancjach. [PDF]. Odzyskany z: nj.gov
- Xueyanghu. (s.f.). Zastosowania i zagrożenia związane z octanem amonu. Odzyskany z: xueyanghu.wordpress.com


Jeszcze bez komentarzy