
Właściwości alkanów lub węglowodorów nasyconych, przykłady
Plik alkany lub węglowodory nasycone charakteryzują się tym, że posiadają w swojej strukturze tylko pojedyncze wiązania kowalencyjne. Oznacza to, że atomy węgla obecne w tych gatunkach są związane z maksymalną liczbą atomów wodoru, z którymi mogą tworzyć wiązania, z tego powodu są one znane jako nasycony.
W świecie chemii organicznej alkany, zwane również parafinami, są uważane za dość rozpowszechnione i bardzo ważne gatunki, należące do grupy węglowodorów alifatycznych (np. Węglowodory nienasycone)..
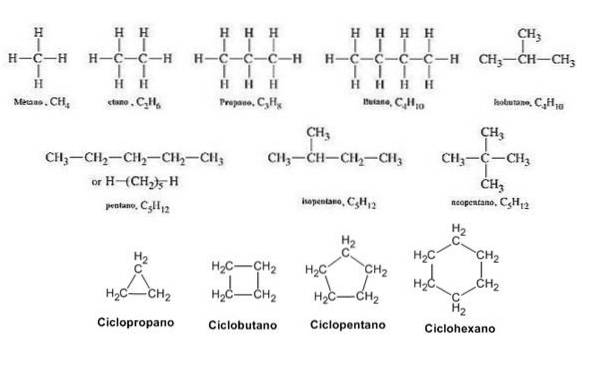
Przykładem może być najprostszy węglowodór nasycony, jaki może powstać: metan, związek występujący w fazie gazowej w standardowych warunkach otoczenia (25 ° C i atm), którego wzór to CH4.
Jak widać, jedyny atom węgla obecny w tej cząsteczce ma cztery proste wiązania, po jednym z każdym atomem wodoru..
Alkeny i alkiny mają ważne zastosowania handlowe, jak w przypadku etylenu i propylenu; ale są one również bardziej reaktywnymi związkami niż węglowodory nasycone, co powoduje, że mają szeroki zakres reakcji, które powstają w przypadku zwykłych alkenów i alkinów..
Indeks artykułów
- 1 Nazewnictwo alkanów
- 1.1 Nomenklatura liniowych węglowodorów nasyconych
- 1.2 Nazewnictwo rozgałęzionych węglowodorów nasyconych
- 1.3 Nazewnictwo cyklicznych węglowodorów nasyconych
- 2 Właściwości
- 2.1 Izomeryzacja geometryczna
- 2.2 Kwasowość
- 2.3 Biegunowość
- 2.4 Temperatury wrzenia i topnienia
- 3 Przykłady alkanów
- 3.1 Liniowe alkany
- 3.2 Alkany rozgałęzione
- 3.3 Cykloalkany
- 4 Odnośniki
Nazewnictwo alkanów
Aby poprawnie nazwać alkany lub węglowodory nasycone, należy przede wszystkim pamiętać, że zgodnie z IUPAC (Międzynarodowa Unia Chemii Czystej i Stosowanej) nie należy stosować systematycznej nomenklatury czterech najprostszych alkanów..
Nazewnictwo liniowych węglowodorów nasyconych
Te związki mają ogólny wzór CnH.2n + 2, gdzie wartość n może być tylko dodatnimi liczbami całkowitymi (n = 1,2, ...) i nazywa się je za pomocą przedrostka odpowiadającego liczbie atomów węgla i dodaje się sufiks -rok.
Tak więc pierwsze cztery nasycone cząsteczki to: metan (CH4), etan (C.dwaH.6), propan (C.3H.8) i butan (C.4H.10).
Na początek nazewnictwo alkanów, które mają od pięciu do dziesięciu atomów węgla, liczy się liczbę tych atomów obecnych w najdłuższym łańcuchu, o ile jest on ciągły.
Ponadto w przypadku odjęcia atomu wodoru od alkanu staje się on podstawnikiem, czyli grupą, której terminacja ulega zmianie -rok dla -ilo. Na przykład metan (CH4) stałoby się metylem (-CH3) i podobnie z innymi cząsteczkami.
Biorąc pod uwagę to, co zostało powiedziane do tej pory i dodając, że zliczanie zawsze należy rozpoczynać od atomu węgla, który ma najbliższy podstawnik, wskazuje się pozycję podstawnika, a następnie nazwę alkanu..
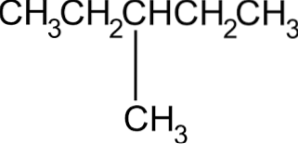
Tak więc powyższy związek nazywa się 3-metylopentanem.
Nazewnictwo rozgałęzionych węglowodorów nasyconych
Podobnie, alkany o rozgałęzionych łańcuchach mają ten sam ogólny wzór co alkany liniowe, ale n> 2. Zatem za każdym razem, gdy jeden lub więcej atomów lub grup atomów zastępuje jeden lub więcej atomów wodoru, należy wskazać lokalizację tych podstawników..
Jeśli istnieje kilka gałęzi grup tego samego typu alkilu, wyrażenia dał-, tri- lub tetra- wskazanie ilości tych podstawników, poprzedzone wskazaniem ich pozycji i zakończone nazwą alkanu.
W przypadku, gdy podstawniki są różne, nazywane są one w kolejności alfabetycznej i mogą również zawierać podstawniki niewęglowe, takie jak chlor (Cl) lub nitro (NOdwa).
We wszystkich przypadkach, aby policzyć liczby atomów węgla w łańcuchu głównym, najmniejszą liczbę podaje się atomowi węgla, który jest połączony z najniższym podstawnikiem w kolejności alfabetycznej i kontynuuje się w tym kierunku.
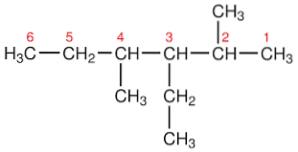
Nazewnictwo cyklicznych węglowodorów nasyconych
Węglowodory nasycone typu cyklicznego, lepiej znane jako cykloalkany mają ogólny wzór CnH.2n, gdzie n = 3,4,…
W tych organicznych cząsteczkach atomy węgla, które ją tworzą, są ułożone w sposób zamknięty, to znaczy ich struktura tworzy pierścień.
Aby nazwać te gatunki, postępuje się zgodnie z wytycznymi opisanymi powyżej dla liniowych i rozgałęzionych alkanów, dodając jedynie przedrostek cykl-. Podobnie cyklopropan (C.3H.6) jako najprostszy cykloalkan.
Podobnie cząsteczki te mogą zawierać więcej niż jeden pierścień zintegrowany z ich głównym łańcuchem, z co najmniej trzema atomami węgla, a nawet tworzyć bardzo złożone struktury..
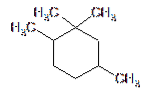
Nieruchomości
Główną cechą węglowodorów nasyconych jest tworzenie prostych wiązań między ich atomami, co czyni je bardzo dużą grupą cząsteczek i nadaje im dość specyficzne właściwości, jak wyszczególniono poniżej:
Izomeryzacja geometryczna
Struktura cząsteczek alkanów powoduje modyfikacje ich właściwości fizycznych i chemicznych ze względu na konformację czterech wiązań, które może tworzyć węgiel..
Oznacza to, że pomimo faktu, że w tych cząsteczkach węgiel ma hybrydyzację typu sp3, kąty między sąsiednimi atomami mogą się różnić w zależności od typu atomu.
Aby wyjaśnić to dokładniej, cykloalkany mają kąty skręcenia, które nadają im unikalną cechę zwaną stereochemią, która może wpływać na energie cząsteczki i inne związane z nią czynniki, takie jak nadawanie jej właściwości spektroskopowych i optycznych..
Kwasowość
Węglowodory nasycone wykazują dość niską reaktywność z jonami i innymi gatunkami polarnymi. Jednocześnie praktycznie nie mają interakcji z substancjami kwaśnymi i zasadowymi..
Biegunowość
Alkany są uważane za nieprzewodzące, ponieważ mają praktycznie zerową biegunowość w obecności pola elektrycznego. Zatem nie można utworzyć wiązań wodorowych, aby umożliwić jego rozpuszczalność w rozpuszczalnikach polarnych..
Są więc praktycznie rozpuszczalne we wszystkich rozpuszczalnikach niepolarnych, nie mieszając się z rozpuszczalnikami polarnymi, takimi jak woda..
Temperatury wrzenia i topnienia
W węglowodorach nasyconych oddziaływania międzycząsteczkowe zachodzą pod wpływem sił van der Waalsa, w których silniejsze oddziaływania przekładają się na wyższe temperatury wrzenia..
Podobną tendencję obserwuje się w przypadku temperatur topnienia, ale wynika to ze zdolności pakowania cząsteczki..
Ponieważ te interakcje są bezpośrednio związane z masą cząsteczkową gatunku, im większa cząsteczka, jej temperatury wrzenia i topnienia będą wyższe..
Tak więc, mając bardziej sztywną strukturę, która daje im międzycząsteczkową płaszczyznę kontaktu, cykloalkany mają wyższą temperaturę wrzenia i topnienia niż odpowiadające im liniowe alkany..
Przykłady alkanów
Alkany liniowe
Metan: Jest to bezbarwny i bezwonny gaz, który występuje w dużej ilości w przyrodzie i jest produktem niektórych działań człowieka. Metan jest najprostszym składnikiem alkanów i jednym z najsilniejszych gazów cieplarnianych (Encyclopædia Britannica, 2017).
Etan: jest to gaz, który występuje głównie w gazie ziemnym i jest używany w mieszaninach z innymi gazami do produkcji paliw.
Propan: jest to bezbarwny gaz występujący w gazie ziemnym i stosowany jako paliwo w domach i przemyśle. Wzór chemiczny propanu to C.3H.8 a rozszerzona formuła to CH3CHdwaCHdwa (Propan Formula, S.F).
Butan: n-butan jest jednym z kilkudziesięciu gazów wydobywanych z surowego gazu ziemnego i może być również produkowany z ropy naftowej. N-butan to bezbarwny gaz wielofunkcyjny. Butan może być używany do ogrzewania, chłodzenia i lżejszego paliwa.
N-pentan: jest przezroczystą, bezbarwną cieczą o zapachu przypominającym zapach ropy naftowej. Pentan znajduje się w napojach alkoholowych i oleju chmielowym. Alkan ten jest składnikiem niektórych paliw i jest używany jako specjalny rozpuszczalnik w laboratorium..
N-heksan: Jest to bezbarwna, przezroczysta ciecz o zapachu przypominającym zapach ropy naftowej. Występuje w owocach cytrusowych, służy do ekstrakcji olejów jadalnych z nasion i warzyw, jako rozpuszczalnik specjalnego przeznaczenia oraz jako środek czyszczący.
N-heptan: Jest to bezbarwna, przezroczysta ciecz o zapachu ropy naftowej. Występuje w kardamonie. Mniej gęsty niż woda i nierozpuszczalny w wodzie. Opary cięższe od powietrza.
N-oktan: jest bezbarwną cieczą o zapachu benzyny. Mniej gęsty niż woda i nierozpuszczalny w wodzie. Dlatego unosi się na wodzie. Wytwarza drażniącą parę.
Chlorek metylu: Nazywany również chlorometanem, jest to bezbarwny gaz. Jest to najprostszy haloalkan, stosowany przy produkcji polimerów silikonowych oraz przy produkcji innych wyrobów chemicznych.
Chloroform: jest to bezbarwna, pachnąca i bardzo lotna ciecz, która jest szeroko stosowana ze względu na swoje właściwości znieczulające. Ze względu na te właściwości ma reputację zdolności ogłuszania lub uderzania ludzi, nawet po spożyciu w małych dawkach (MoviesDoes Chloroform naprawdę powala cię tak szybko, jak pokazują w filmach?, 2016).
Tetrachlorek węgla: zwany także tetrachlorometanem, bezbarwna, gęsta, silnie toksyczna, lotna, niepalna ciecz o charakterystycznym zapachu, stosowana jako rozpuszczalnik.
Chloroetan: to gaz, który skrapla się pod niewielkim ciśnieniem. Chloroetan jest stosowany głównie do miejscowego uśmierzania bólu w medycynie sportowej (National Center for Biotechnology Information., 2017).
Bromoetan: znany również jako bromek etylu, jest bezbarwną lotną cieczą, słabo rozpuszczalną i gęstszą niż woda. Opary są cięższe od powietrza. Używany do produkcji farmaceutyków oraz jako rozpuszczalnik.
Rozgałęzione alkany
Izobutan: jest bezbarwnym gazem o słabym zapachu ropy naftowej. Jest wysyłany jako skroplony gaz pod ciśnieniem pary. Kontakt z cieczą może spowodować odmrożenia. Łatwo się świeci.
IzopentanNazywany również 2-metylobutanem, jest bezbarwną wodną cieczą o zapachu benzyny. Unosi się w wodzie. Wytwarza łatwopalne i drażniące opary (National Center for Biotechnology Information. PubChem Compound Database;, 2017).
2-metylopentan: jest alkanem o rozgałęzionym łańcuchu o wzorze cząsteczkowym C.6H14. Jest to wodnisty płyn o zapachu benzyny, który unosi się na wodzie i wytwarza drażniącą parę.
3,3-dimetyloheksan: występuje w ziołach i przyprawach. 3, 3-Dimethylhexane jest składnikiem Osmanthus fragrans (słodkiego osmantusa) i olejku żeń-szenia.
2,3-dimetyloheksan: występuje w owocach. 2,3-Dimetyloheksan jest lotnym składnikiem skrobi.
Neopentan: jest to ciecz mniej gęsta niż woda. Nierozpuszczalny w wodzie, ale rozpuszczalny w alkoholu (National Center for Biotechnology Information., 2015).
2,2,4-trimetylopentan: o Izooktan jest uwalniany do środowiska podczas produkcji, użytkowania i utylizacji produktów związanych z przemysłem naftowym. 2,2,4-trimetylopentan wnikał w skórę człowieka i powodował martwicę skóry i tkanek dłoni wymagającą operacji (National Center for Biotechnology Information., 2017).
Cykloalkany
Cyklopropan: Jest to bezbarwny gaz o zapachu podobnym do ropy naftowej. Kontakt z cieczą może spowodować odmrożenia. Może się udusić z powodu przemieszczania się powietrza, aw wysokich stężeniach ma działanie narkotyczne.
Cyklobutan: Gaz, który skrapla się do postaci cieczy w temperaturze 13 ° C. Nierozpuszczalny w wodzie. Rozpuszczalny w alkoholu, acetonie i eterze.
Cyklopentan: Jest to bezbarwna, przezroczysta ciecz o zapachu ropy naftowej. Mniej gęsty niż woda i nierozpuszczalny w niej. Opary są cięższe od powietrza.
Cykloheksan: występuje w kalarepie. Rozcieńczalnik w mieszankach barwników do użytku spożywczego.
Cykloheptan: jest to bezbarwna, oleista ciecz, nierozpuszczalna i mniej gęsta niż woda. Wdychanie wysokich stężeń może mieć działanie narkotyczne. Używany do produkcji innych chemikaliów.
Cyklooktan: jest wielopierścieniowym węglowodorem z dziewięcioma atomami węgla. Nierozpuszczalne w wodzie.
Metylocykloheksan: Jest to bezbarwna, przezroczysta ciecz o zapachu ropy naftowej. W metylocykloheksanie konformacja krzesła, w której duża grupa metylowa jest równikowa, jest najbardziej stabilna, a zatem najbardziej zaludniona ze wszystkich możliwych konformacji (Carey, 2011).
Cykloheksan izopropylowy: to bezbarwna ciecz występująca w owocach. Izopropylocykloheksan znajduje się w Carica papaya (papaja).
metylocyklopentan: jest to bezbarwna, nierozpuszczalna ciecz i mniej gęsta niż woda. Opary mogą działać odurzająco i drażniąco. Metylocyklopentan jest izolowany z Helianthus annuus (słonecznik).
Norborano: jest to bicykliczny alkan zwany również bicyklo [2,2,1] heptanem o wzorze C7H12.
Bibliografia
- Alkany. (28 listopada 2016). Odzyskany z chem.libretexts.org.
- Alkany. (S.F.). Pobrane z hyperphysics.phy-astr.gsu.edu.
- (2014). Alkany. Odzyskany z bbc.co.uk.
- Carey, F. A. (2 grudnia 2011). Węglowodór. Odzyskany z Britannica.
- Encyclopædia Britannica. (2017, 24 marca). Metan. Odzyskany z britannica.com.
- Khan academy. (S.F.). Alkany, cykloalkany i grupy funkcyjne. Odzyskany z khanacademy.org.
- MoviesDoes Chloroform naprawdę Cię znokautuje tak szybko, jak pokazują się w filmach? (2016). Odzyskany z scienceabc.
- National Center for Biotechnology Information… (06 maja 2017). Baza danych PubChem Compound; CID = 6337. Odzyskane z PubChem.
- Narodowe Centrum Informacji Biotechnologicznej. (6 maja 2015). Baza danych PubChem Compound; CID = 10041. Odzyskane z PubChem.
- Narodowe Centrum Informacji Biotechnologicznej. (2017, 6 maja). Baza danych PubChem Compound; CID = 10907. Odzyskane z PubChem.
- Narodowe Centrum Informacji Biotechnologicznej. Baza danych PubChem Compound; (2017, 6 maja). Baza danych PubChem Compound; CID = 6556,. Odzyskane z PubChem.
- Formuła propanu. (S.F.). Odzyskany z softschools.com.



Jeszcze bez komentarzy