
Struktura trzeciorzędowego alkoholu butylowego, właściwości, zagrożenia i zastosowania
Plik trzeciorzędowy alkohol butylowy jest związkiem organicznym, którego wzór to (CH3)3COH lub t-BuOH. Jest to najprostszy trzeciorzędowy alkohol ze wszystkich. W zależności od temperatury otoczenia występuje jako bezbarwne ciało stałe lub ciecz. Poniższy obrazek przedstawia na przykład jego bezbarwne kryształy.
Alkohol ten nie jest substratem enzymu dehydrogenazy alkoholowej ani aktywności peroksydazy katalazy, dlatego jest klasyfikowany jako alkohol nieulegający metabolizmowi. Ze względu na swoje właściwości biochemiczne uważa się, że może być przydatny do wykrywania rodników hydroksylowych in vivo w nienaruszonych komórkach..

Jest to jeden z czterech izomerów alkoholu izobutylowego, przy czym izomer jest najmniej podatny na utlenianie i najmniej reaktywny. W naturze występuje w ciecierzycy i manioku, korzeniu fermentowanym w celu produkcji napojów alkoholowych..
Trzeciorzędowy alkohol butylowy jest bardzo dobrze rozpuszczalny w wodzie i rozpuszczalnikach organicznych. Jego głównym zastosowaniem jest rozpuszczalnik spełniający tę rolę przy produkcji tworzyw sztucznych, perfum, zmywaczy do farb itp..
Podobnie jak wiele związków organicznych jest nieco toksyczny, ale w dużych dawkach działa narkotycznie, charakteryzując się bólami głowy, zawrotami głowy, zawrotami głowy, zawrotami głowy i oszołomieniem..
Indeks artykułów
- 1 Struktura alkoholu tert-butylowego
- 2 Właściwości
- 2.1 Nazwy chemiczne
- 2.2 Wzór cząsteczkowy
- 2.3 Masa cząsteczkowa
- 2.4 Opis fizyczny
- 2.5 Zapach
- 2.6 Temperatura wrzenia
- 2.7 Temperatura topnienia
- 2.8 Temperatura zapłonu
- 2.9 Rozpuszczalność w wodzie
- 2.10 Rozpuszczalność w rozpuszczalnikach organicznych
- 2.11 Gęstość
- 2.12 Gęstość par
- 2.13 Prężność par
- 2.14 Współczynnik podziału oktanol / woda
- 2.15 Termostabilność
- 2.16 Temperatura samozapłonu
- 2.17 Rozkład
- 2.18 Ciepło parowania
- 2.19 Pojemność kaloryczna
- 2.20 Entalpia formacji
- 2.21 Temperatura przechowywania
- 2.22 Stabilność
- 2.23 Potencjał jonizacyjny
- 2.24 Próg zapachu
- 2.25 Współczynnik załamania światła
- 2.26 Stała dysocjacji
- 2.27 Maksymalne stężenie oparów
- 2.28 Reakcje
- 3 Ryzyka
- 4 Zastosowania
- 5 Referencje
Struktura alkoholu tert-butylowego
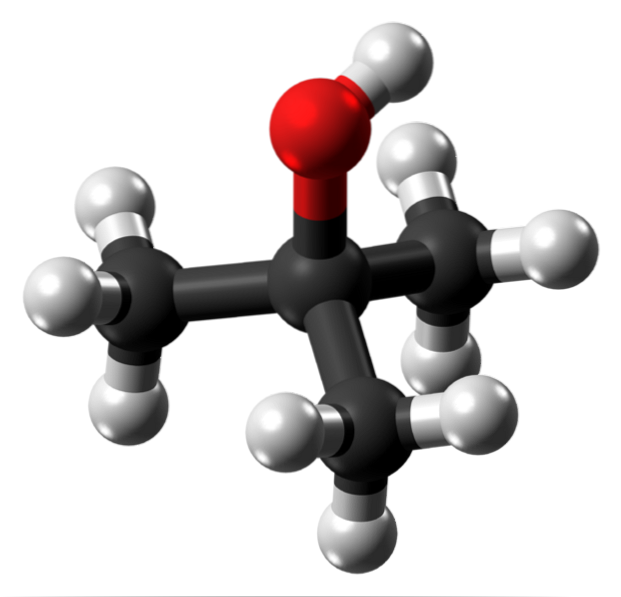
Górny obraz przedstawia strukturę molekularną alkoholu tert-butylowego z modelem kulek i słupków. Cała cząsteczka ma globalną tetraedryczną geometrię, z trzecim atomem węgla znajdującym się w jej centrum i grupami CH3 i OH na wierzchołkach.
Obserwując tę strukturę, można zrozumieć, dlaczego ten alkohol jest trzeciorzędowy: węgiel w środku jest połączony z trzema innymi atomami węgla. Kontynuując czworościan, jego dolną część można uznać za niepolarną, a górną za biegunową.
W tym wierzchołku znajduje się grupa OH, która tworzy trwały moment dipolowy, a także umożliwia cząsteczkom t-BuOH oddziaływanie poprzez wiązania wodorowe; w taki sam sposób, jak to robi z cząsteczkami wody i innymi substancjami polarnymi.
W kryształach t-BuOH te wiązania wodorowe są kluczowym czynnikiem dla pozostawania razem cząsteczek; chociaż nie ma zbyt wielu informacji na temat struktury krystalicznej tego alkoholu.
Ponieważ grupa OH jest tak blisko i otoczona niepolarnymi grupami CH3, cząsteczki wody są w stanie uwodnić prawie cały alkohol w tym samym czasie, w którym oddziałują z OH. To wyjaśniałoby jego świetną rozpuszczalność w wodzie..
Nieruchomości
Nazwy chemiczne
-Trzeciorzędowy alkohol butylowy
-tert-butanol
-2-metylo-2-propanol
-2-metylopropan-2-ol.
Formuła molekularna
do4H.10O lub (CH3)3COH.
Waga molekularna
74,123 g / mol.
Opis fizyczny
Bezbarwne ciało stałe lub bezbarwna ciecz, w zależności od temperatury otoczenia, ponieważ temperatura topnienia wynosi 77,9ºF (25,4ºC). Powyżej 77,9ºF jest to ciecz.
Zapach
Podobny do kamfory.
Temperatura wrzenia
82,4 ° C.
Temperatura topnienia
77,9 ° F (25,4 ° C).
punkt zapłonu
52 ° F (11 ° C). Zamknięty kubek.
Rozpuszczalność w wodzie
Bardzo dobrze rozpuszczalny. W rzeczywistości, niezależnie od proporcji, alkohol ten jest zawsze mieszalny z wodą..
Rozpuszczalność w rozpuszczalnikach organicznych
Mieszalny z etanolem, eterem etylowym i rozpuszczalny w chloroformie.
Gęstość
0,78 g / cm3.
Gęstość pary
2,55 (względem powietrza = 1).
Ciśnienie pary
4,1 kPa w 20 ºC.
Współczynnik podziału oktanol / woda
Log P = 0,35.
Termostabilność
Niestabilny w upale
Temperatura samozapłonu
896 ° F (470 ° C).
Rozkład
Po podgrzaniu może wydzielać tlenek węgla i opary izobutylenu.
Ciepło parowania
39,07 kJ / mol.
Pojemność kaloryczna
215,37 JK-1kret-1.
Entalpia formacji
-360,04 do -358,36 kJmol-1.
Temperatura przechowywania
2-8 ºC.
Stabilność
Jest stabilny, ale niekompatybilny z silnymi utleniaczami, miedzią, stopami miedzi, metalami alkalicznymi i aluminium.
Potencjał jonizacyjny
9,70 eV.
Próg zapachu
219 mg / m23 (słaby zapach).
Współczynnik załamania światła
1382 przy 25 ° C.
Stała dysocjacji
pKa = 19,20.
Maksymalne stężenie par
5,53% przy 25 ºC.
Reakcje
-Jest deprotonowany przez mocną zasadę, dając początek anionowi alkoholanowemu; w szczególności terbutoksyd (CH3)3WSPÓŁ-.
-Trzeciorzędowy alkohol butylowy reaguje z chlorowodorem, tworząc trzeciorzędowy chlorek butylu..
(CH3)3COH + HCl => (CH3)3CCl + HdwaLUB
Alkohole trzeciorzędowe mają większą reaktywność z halogenowodorami niż alkohole drugorzędowe i pierwszorzędowe.
Ryzyka
Alkohol tert-butylowy w kontakcie ze skórą powoduje drobne zmiany, takie jak łagodny rumień i przekrwienie. Nie przechodzi również przez skórę. Wręcz przeciwnie, w oczach powoduje silne podrażnienie.
Wdychany podrażnia nos, gardło i oskrzela. W przypadku dużego narażenia może wystąpić efekt narkotyczny, senność, a także zawroty głowy, oszołomienie i ból głowy.
Alkohol ten jest eksperymentalnym środkiem teratogennym, dlatego u zwierząt zaobserwowano, że może wpływać na pojawienie się wad wrodzonych.
Jeśli chodzi o przechowywanie, jego ciecz i opary są łatwopalne, dlatego w pewnych okolicznościach może powodować pożary i wybuchy..
OSHA ustalił stężenie graniczne 100 ppm (300 mg / m3) na 8-godzinną zmianę.
Aplikacje
-Alkohol tert-butylowy służy do włączania grupy tert-butylowej do związków organicznych w celu wytworzenia żywic rozpuszczalnych w olejach oraz trinitro-tert-butylotoluenu, sztucznego piżma. Ponadto stanowi materiał wyjściowy do przygotowania nadtlenków.
-Został zatwierdzony przez FDA jako środek przeciwpieniący do stosowania na tworzywach sztucznych i komponentach, które mają kontakt z żywnością. Znajduje zastosowanie w produkcji esencji owocowych, tworzyw sztucznych i lakierów.
-Jest półproduktem do produkcji chlorku tert-butylu i tributylofenolu. Działa jako środek skażający etanol.
-Służy do produkcji środków flotacyjnych, jako rozpuszczalnik organiczny do usuwania farb oraz do rozpuszczania esencji stosowanych w perfumach..
-Jest stosowany jako wzmacniacz oktanowy w benzynie; paliwo i dodatek do paliwa; rozpuszczalnik do czyszczenia i odtłuszczania.
-Alkohol tert-butylowy jest pośrednikiem w produkcji eteru tert-butylometylowego (MTBE) i eteru tributyloetylowego (ETBE), reagując odpowiednio z metanolem i etanolem.
-Działa również w ten sam sposób przy wytwarzaniu wodoronadtlenku tributylu (TBHP) w reakcji z nadtlenkiem wodoru..
-Jest używany jako odczynnik w procesie znanym jako przegrupowanie Curtiusa..
Bibliografia
- Graham Solomons T.W., Craig B. Fryhle. (2011). Chemia organiczna. Aminy. (10th wydanie.). Wiley plus.
- Wikipedia. (2019). Alkohol tert-butylowy. Odzyskane z: en.wikipedia.org
- CommonOrganicChemistry. (s.f.). t-butanol. Źródło: commonorganicchemistry.com
- Narodowe Centrum Informacji Biotechnologicznej. (2019). Butanol tert. Baza danych PubChem. Odzyskany z: pubchem.ncbi.nlm.nih.gov
- Carey F. A. (2008). Chemia organiczna. (Wydanie szóste). Mc Graw Hill.



Jeszcze bez komentarzy