
Struktura, właściwości, nazewnictwo i zastosowania alkoholi
Plik alkohole są to związki organiczne, które charakteryzują się grupą hydroksylową (-OH) połączoną z nasyconym węglem; to znaczy węgiel, który jest połączony z czterema atomami pojedynczymi wiązaniami (bez podwójnych lub potrójnych wiązań).
Ogólny wzór tej rozległej i wszechstronnej rodziny związków to ROH. Aby można było uznać go za alkohol w ściśle chemicznym sensie, grupa OH musi być najbardziej reaktywna w strukturze molekularnej. Jest to ważne, aby móc potwierdzić, pośród kilku cząsteczek z grupami OH, która z nich jest alkoholem..

Jednym z kwintesencji alkoholi i najbardziej znanym w kulturze popularnej jest alkohol etylowy lub etanol, CH3CHdwaO. W zależności od naturalnego pochodzenia, a tym samym środowiska chemicznego, ich mieszanki mogą tworzyć nieograniczone spektrum smaków; niektóre, które nawet wykazują pozytywne zmiany na podniebieniu latem.
Są to mieszaniny związków organicznych i nieorganicznych z alkoholem etylowym, które powodują jego spożycie podczas wydarzeń społecznych i religijnych od czasów przed Chrystusem; na przykład do wina gronowego lub do kieliszków podawanych na uroczystość, oprócz ponczów, cukierków, panettonów itp..
Przyjemność z tych napojów, z umiarem, jest wynikiem synergii między alkoholem etylowym a otaczającą go chemiczną matrycą; bez niej, jako czysta substancja, staje się niezwykle niebezpieczna i wywołuje szereg negatywnych konsekwencji zdrowotnych.
Z tego powodu zużycie wodnych mieszanin CH3CHdwaOH, podobnie jak te kupowane w aptekach w celach antyseptycznych, stanowi duże zagrożenie dla organizmu.
Inne alkohole, które są również bardzo popularne, to mentol i gliceryna. Ten ostatni, podobnie jak erytrol, znajduje się jako dodatek do wielu produktów spożywczych, służący do ich słodzenia i konserwowania podczas przechowywania. Istnieją jednostki rządowe, które dyktują, które alkohole mogą być używane lub konsumowane bez skutków ubocznych..
Pomijając codzienne stosowanie alkoholi, pod względem chemicznym są substancjami bardzo wszechstronnymi, ponieważ wychodząc z nich można syntetyzować inne związki organiczne; do tego stopnia, że niektórzy autorzy uważają, że przy kilkunastu z nich można stworzyć wszystkie niezbędne związki do życia na bezludnej wyspie.
Indeks artykułów
- 1 Struktura alkoholi
- 1.1 Charakter amfifilny
- 1.2 Struktura R
- 2 Właściwości fizyczne i chemiczne
- 2.1 Temperatura wrzenia
- 2.2 Pojemność rozpuszczalnika
- 2.3 Amfoterycyzm
- 3 Nazewnictwo
- 3.1 Nazwa zwyczajowa
- 3.2 System IUPAC
- 4 Synteza
- 4.1 Uwodnienie alkenów
- 4.2 Proces Oxo
- 4.3 Fermentacja węglowodanów
- 5 zastosowań
- 5.1 Napoje
- 5.2 Surowiec chemiczny
- 5.3 Rozpuszczalniki
- 5.4 Paliwa
- 5.5 Antyseptyki
- 5.6 Inne zastosowania
- 6 Odnośniki
Struktura alkoholi
Alkohole mają ogólny wzór ROH. Grupa OH jest połączona z grupą alkilową R, której struktura różni się w zależności od alkoholu. Połączenie między R i OH zachodzi poprzez pojedyncze wiązanie kowalencyjne, R-OH.
Poniższy obraz przedstawia trzy ogólne struktury alkoholi, pamiętając, że atom węgla jest nasycony; to znaczy tworzy cztery proste linki.
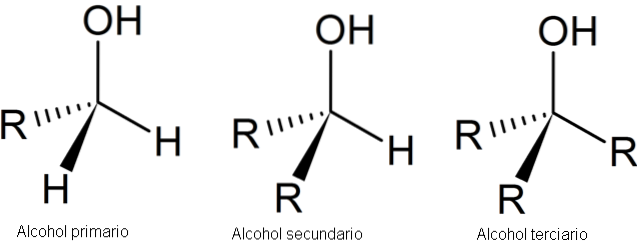
Jak widać, R może być dowolnym szkieletem węglowym, o ile nie ma podstawników bardziej reaktywnych niż grupa OH..
W przypadku pierwszorzędowego alkoholu pierwsza grupa OH jest połączona z pierwszorzędowym węglem. Można to łatwo zweryfikować, obserwując, że atom w środku lewego czworościanu jest związany z jednym R i dwoma H.
Alkohol drugorzędowy, 2º, jest weryfikowany za pomocą węgla w czworościanie pośrodku, teraz połączonego z dwiema grupami R i jednym H.
I wreszcie trzeciorzędowy alkohol, 3º, z atomem węgla połączonym z trzema grupami R..
Charakter amfifilny
W zależności od rodzaju węgla związanego z OH istnieje klasyfikacja alkoholi pierwszorzędowych, drugorzędowych i trzeciorzędowych. W czworościanach szczegółowo opisano różnice strukturalne między nimi. Ale wszystkie alkohole, niezależnie od ich struktury, mają coś wspólnego: charakter amfifilowy..
Nie musisz zajmować się strukturą, aby ją zauważyć, wystarczy jej wzór chemiczny ROH. Grupa alkilowa składa się prawie w całości z atomów węgla, „składających” hydrofobowy szkielet; to znaczy bardzo słabo oddziałuje z wodą.
Z drugiej strony grupa OH może tworzyć wiązania wodorowe z cząsteczkami wody, dzięki czemu jest hydrofilowa; to znaczy kocha wodę lub ma do niej powinowactwo. Tak więc alkohole mają hydrofobowy szkielet, przyłączony do grupy hydrofilowej. Są jednocześnie niepolarne i polarne, co oznacza to samo, co stwierdzenie, że są substancjami amfifilowymi.
R-OH
(Hydrofobowy) - (hydrofilowy)
Jak zostanie wyjaśnione w następnej sekcji, amfifilowy charakter alkoholi określa niektóre z ich właściwości chemicznych..
Struktura R
Grupa alkilowa R może mieć dowolną strukturę, ale jest ważna, ponieważ umożliwia katalogowanie alkoholi.
Na przykład R może być łańcuchem otwartym, jak ma to miejsce w przypadku etanolu lub propanolu; rozgałęzione, takie jak alkohol t-butylowy (CH3)dwaCHCHdwaO; może być cykliczny, jak w przypadku cykloheksanolu; lub może mieć pierścień aromatyczny, jak w alkoholu benzylowym (C.6H.5) CHdwaOH lub w 3-fenylopropanolu (C6H.5) CHdwaCHdwaCHdwaO.
Łańcuch R może nawet zawierać podstawniki, takie jak halogeny lub podwójne wiązania, takie jak dla alkoholi 2-chloroetanol i 2-buten-1-ol (CH3CHdwa= CHCHdwaO).
Biorąc więc pod uwagę strukturę R, klasyfikacja alkoholi staje się złożona. Z tego powodu klasyfikacja oparta na ich strukturze (alkohole I, II i III) jest prostsza, ale mniej szczegółowa, chociaż wystarczy wyjaśnić reaktywność alkoholi..
Fizyczne i chemiczne właściwości
Temperatura wrzenia
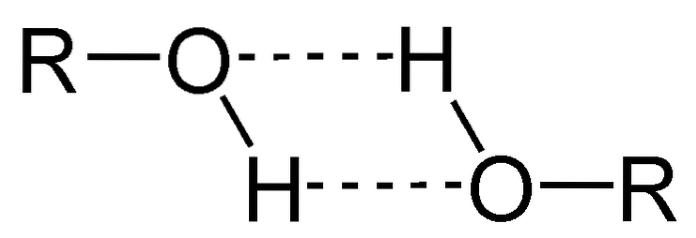
Jedną z głównych właściwości alkoholi jest to, że łączą się poprzez wiązania wodorowe.
Na powyższym obrazku możesz zobaczyć, jak dwie cząsteczki ROH tworzą ze sobą wiązania wodorowe. Dzięki temu alkohole to najczęściej ciecze o wysokiej temperaturze wrzenia..
Na przykład alkohol etylowy ma temperaturę wrzenia 78,5 ° C. Wartość ta rośnie, gdy alkohol staje się cięższy; to znaczy, grupa R ma większą masę lub liczbę atomów. Zatem alkohol n-butylowy, CH3CHdwaCHdwaCHdwaOH ma temperaturę wrzenia 97ºC, nieco niższą niż woda.
Glicerol należy do alkoholi o najwyższej temperaturze wrzenia 290ºC.
Dlaczego? Ponieważ wpływa nie tylko masa lub struktura R, ale także liczba grup OH. Glicerol ma w swojej strukturze trzy OH: (HO) CHdwaCH (OH) CHdwa(O). Dzięki temu jest w stanie tworzyć wiele wiązań wodorowych i mocniej trzymać swoje cząsteczki razem..
Z drugiej strony, niektóre alkohole są stałe w temperaturze pokojowej; jak ta sama gliceryna w temperaturze poniżej 18 ° C. Dlatego twierdzenie, że wszystkie alkohole są substancjami płynnymi, jest błędne..
Pojemność rozpuszczalnika
W domach bardzo często stosuje się alkohol izopropylowy w celu usunięcia plam, które są trudne do usunięcia z powierzchni. Ta zdolność rozpuszczania, bardzo przydatna w syntezie chemicznej, wynika z jego amfifilowego charakteru, wyjaśnionego wcześniej.
Tłuszcze charakteryzują się hydrofobowością, dlatego trudno je usunąć wodą. Jednak w przeciwieństwie do wody alkohole mają w swojej strukturze część hydrofobową.
W ten sposób jego grupa alkilowa R oddziałuje z tłuszczami, podczas gdy grupa OH tworzy wiązania wodorowe z wodą, pomagając je wypierać..
Amfoterycyzm
Alkohole mogą reagować jako kwasy i zasady; to znaczy są substancjami amfoterycznymi. Przedstawiają to następujące dwa równania chemiczne:
ROH + H+ => ROHdwa+
ROH + OH- => RO-
RO- to ogólny wzór tego, co jest znane jako alkoholan.
Nomenklatura
Istnieją dwa sposoby na nazwanie alkoholi, których złożoność zależy od ich struktury.
Nazwa zwyczajowa
Alkohole można nazwać ich potocznymi nazwami. Które są? W tym celu należy znać nazwę grupy R, do której dodaje się końcówkę -ico, i jest poprzedzona słowem „alkohol”. Na przykład CH3CHdwaCHdwaOH to alkohol propylowy.
Inne przykłady to:
-CH3OH: alkohol metylowy
-(CH3)dwaCHCHdwaOH: alkohol izobutylowy
-(CH3)3COH: alkohol tert-butylowy
System IUPAC
Jeśli chodzi o nazwy zwyczajowe, musisz zacząć od zidentyfikowania R. Zaletą tego systemu jest to, że jest on znacznie dokładniejszy od drugiego..
R, będący szkieletem węglowym, może mieć rozgałęzienia lub kilka łańcuchów; najdłuższy łańcuch, to znaczy zawierający więcej atomów węgla, będzie nazywany alkoholem.
Do nazwy alkanu o najdłuższym łańcuchu dodaje się końcówkę „l”. Dlatego w CH3CHdwaOH nazywa się etanolem (CH3CHdwa- + O).
Generalnie OH powinien mieć najniższe możliwe wyliczenie. Na przykład BrCHdwaCHdwaCHdwa(OH) CH3 nazywa się 4-Bromo-2-butanol, a nie 1-Bromo-3-butanol.
Synteza
Nawodnienie alkenu
W procesie krakowania oleju powstaje mieszanina alkenów o czterech lub pięciu atomach węgla, które można łatwo oddzielić.
Te alkeny można przekształcić w alkohole przez bezpośrednie dodanie wody lub przez reakcję alkenu z kwasem siarkowym, a następnie dodanie wody, która rozszczepia kwas, z którego pochodzi alkohol..
Proces Oxo
W obecności odpowiedniego katalizatora alkeny reagują z tlenkiem węgla i wodorem, tworząc aldehydy. Aldehydy można łatwo zredukować do alkoholi poprzez katalityczną reakcję uwodornienia.
Często dochodzi do takiej synchronizacji procesu okso, że redukcja aldehydów jest prawie równoczesna z ich powstawaniem..
Najczęściej stosowanym katalizatorem jest dikobalt oktokarbonyl, otrzymywany w reakcji kobaltu z tlenkiem węgla.
Fermentacja węglowodanów
Fermentacja węglowodanów przez drożdże ma nadal duże znaczenie w produkcji etanolu i innych alkoholi. Cukry pochodzą z trzciny cukrowej lub skrobi uzyskanej z różnych ziaren. Z tego powodu etanol nazywany jest również „alkoholem zbożowym”
Aplikacje
Napoje
Chociaż nie jest to główna funkcja alkoholi, obecność etanolu w niektórych napojach jest jedną z najpopularniejszych wiedzy. Tak więc etanol, produkt fermentacji trzciny cukrowej, winogron, jabłek itp., Jest obecny w wielu napojach do spożycia społecznego..
Surowiec chemiczny
-Metanol jest wykorzystywany do produkcji formaldehydu, poprzez jego katalityczne utlenianie. Formaldehyd jest używany do produkcji tworzyw sztucznych, farb, tekstyliów, materiałów wybuchowych itp..
-Butanol jest używany do produkcji etanianu butanu, estru używanego jako środek aromatyzujący w przemyśle spożywczym i cukierniczym..
-Alkohol allilowy jest wykorzystywany do produkcji estrów, w tym ftalanu diallilu i izoftalanu diallilu, które służą jako monomery.
-Fenol jest używany do produkcji żywic, produkcji nylonu, dezodorantów, kosmetyków itp..
-Alkohole o prostym łańcuchu o 11-16 atomach węgla są używane jako półprodukty do otrzymywania plastyfikatorów; na przykład polichlorek winylu.
-Jako półprodukty w syntezie detergentów stosuje się tzw. Alkohole tłuszczowe.
Rozpuszczalniki
-Jako rozcieńczalnik do farb stosuje się metanol, podobnie jak 1-butanol i alkohol izobutylowy.
-Alkohol etylowy jest stosowany jako rozpuszczalnik dla wielu nierozpuszczalnych w wodzie związków, stosowany jako rozpuszczalnik w farbach, kosmetykach itp..
-Alkohole tłuszczowe są stosowane jako rozpuszczalniki w przemyśle tekstylnym, barwnikach, detergentach i farbach. Izobutanol jest stosowany jako rozpuszczalnik w materiałach powłokowych, farbach i klejach.
Paliwa
-Metanol jest stosowany jako paliwo w silnikach spalinowych oraz jako dodatek do benzyny poprawiający spalanie.
-Alkohol etylowy jest używany w połączeniu z paliwami kopalnymi w pojazdach silnikowych. W tym celu rozległe regiony Brazylii przeznaczone są pod uprawę trzciny cukrowej do produkcji alkoholu etylowego. Ten alkohol ma tę zaletę, że podczas spalania wytwarza tylko dwutlenek węgla..
Spalony alkohol etylowy wytwarza czysty, bezdymny płomień, dlatego jest używany jako paliwo w kuchniach polowych..
-Alkohol zżelowany powstaje w wyniku połączenia metanolu lub etanolu z octanem wapnia. Alkohol ten jest używany jako źródło ciepła w piecach polowych, a ponieważ się rozlewa, jest bezpieczniejszy niż alkohole płynne.
-Paliwem w transporcie jest tzw. Biobutanol oraz alkohol izopropylowy, który można wykorzystać jako paliwo; chociaż jego użycie nie jest zalecane.
Antyseptyki
Alkohol izopropylowy o stężeniu 70% jest stosowany jako zewnętrzny środek antyseptyczny w celu wyeliminowania zarazków i opóźnienia ich wzrostu. W tym celu stosuje się również alkohol etylowy..
Inne zastosowania
Cykloheksanol i metylocykloheksanol są używane do wykańczania tekstyliów, obróbki mebli i odplamiaczy.
Bibliografia
- Graham Solomons T.W., Craig B. Fryhle. (2011). Chemia organiczna. Aminy. (10th wydanie.). Wiley plus.
- Carey F. (2008). Chemia organiczna. (Wydanie szóste). Mc Graw Hill.
- Morrison i Boyd. (1987). Chemia organiczna. (Piąta edycja). Addison-Wesley Iberoamericana.
- Dr JA Colapret. (s.f.). Alkohole. Odzyskany z: colapret.cm.utexas.edu
- Partnerstwo na rzecz edukacji w zakresie farmakologii alkoholowej. (s.f.). Co to jest alkohol? Duke University. Odzyskany z: sites.duke.edu
- Whittemore F. (s.f.). Rodzaje i zastosowania alkoholu. Odzyskany z: livestrong.com
- Wikipedia. (2018). Alkohol. Odzyskane z: en.wikipedia.org



Jeszcze bez komentarzy