
Struktura, właściwości, zagrożenia, zastosowania cyjanku sodu (NaCN)

Plik Cyjanek sodowy jest nieorganiczną solą utworzoną przez kation sodu Na+ i anion cyjankowy CN-. Jego wzór chemiczny to NaCN. Znany również jako cyjanek sodu, jest białą krystaliczną substancją stałą. Jest higroskopijny, czyli pochłania wodę z otoczenia, a jego kryształy są sześcienne jak chlorek sodu NaCl.
Po rozpuszczeniu w wodzie ma tendencję do tworzenia cyjanowodoru HCN. Jego roztwory łatwo rozpuszczają złoto i srebro. Ta cecha sprawia, że jest używany do wydobywania złota i srebra z minerałów. Zastosowane w tym celu rozwiązania są poddawane recyklingowi, czyli są wielokrotnie ponownie wykorzystywane.

Jednak część cyjanku przedostaje się do niektórych zbiorników ściekowych, co stanowi zagrożenie dla dzikich zwierząt i ludzi, ponieważ cyjanek jest bardzo toksyczny i może spowodować śmierć..
NaCN jest stosowany w przemyśle chemicznym jako półprodukt do wytwarzania różnego rodzaju związków, takich jak barwniki, chemia rolnicza oraz leki czy leki..
Cyjanek sodu jest bardzo niebezpiecznym związkiem, ponieważ może spowodować śmierć, dlatego należy obchodzić się z nim z najwyższą ostrożnością.
Indeks artykułów
- 1 Struktura
- 2 Nazewnictwo
- 3 Właściwości
- 3.1 Stan fizyczny
- 3.2 Masa cząsteczkowa
- 3.3 Temperatura topnienia
- 3.4 Temperatura wrzenia
- 3.5 Temperatura zapłonu
- 3.6 Gęstość
- 3.7 Rozpuszczalność
- 3.8 Stała dysocjacji
- 3,9 pH
- 3.10 Właściwości chemiczne
- 4 Ryzyka
- 5 Otrzymywanie
- 6 zastosowań
- 6.1 W wydobyciu minerałów złota i srebra. Konsekwencje
- 6.2 Przy produkcji innych związków chemicznych
- 6.3 W przemyśle metalowym
- 6.4 Do innych zastosowań
- 6.5 Nieużywane, kwestionowane lub bardzo rzadkie aplikacje
- 7 Referencje
Struktura
Cyjanek sodu składa się z jonu Na + i jonu CN-.
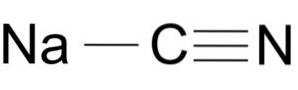
Jon cyjanek ma atom węgla C i atom azotu N połączone ze sobą potrójnym wiązaniem..
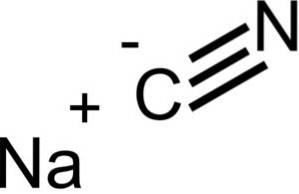
NaCN ma taką samą strukturę krystaliczną jak NaCl, więc jego kryształy są sześcienne.
Nomenklatura
-Cyjanek sodowy
-Cyjanek sodowy
Nieruchomości
Stan fizyczny
Higroskopijna biała krystaliczna substancja stała (pochłania wodę z otoczenia).
Waga molekularna
49,007 g / mol
Temperatura topnienia
563,7 ° C
Temperatura wrzenia
1496 ºC
Temperatura zapłonu
Nie jest łatwopalny. Ale w przypadku wystawienia na działanie ognia powstaje cyjanowodór HCN i tlenki azotu..
Gęstość
1595 g / cm3 przy 20 ºC
Rozpuszczalność
Bardzo dobrze rozpuszczalny w wodzie: 48 g / 100 ml w 10 ° C, 82 g / 100 ml w 35 ° C. Słabo rozpuszczalny w alkoholu
Stała dysocjacji
Jest hydrolizowany w roztworze wodnym, w wyniku czego powstaje cyjanowodór HCN. Stała tej hydrolizy wynosi Kgodz = 2,5 x 10-5.
pH
Wodne roztwory NaCN są silnie zasadowe
Właściwości chemiczne
Po rozpuszczeniu w wodzie rozdziela się na jony Na+ i CN-. W roztworze wodnym jon cyjanku CN- weź proton H.+ wody H.dwaLub tworząc HCN i jon OH-, więc roztwór staje się zasadowy.
CN- + H.dwaO → HCN + OH-
Z tego powodu jego wodne roztwory rozkładają się szybko podczas przechowywania, tworząc cyjanowodór HCN..
Działa korodująco na aluminium. Jego roztwory łatwo rozpuszczają złoto Au i srebro Ag w obecności powietrza..
Jest środkiem chelatującym od anionu cyjankowego CN- łatwo wiąże się z innymi metalami, takimi jak srebro, złoto, rtęć, cynk, kadm itp..
Ma słaby gorzki zapach migdałów.
Ryzyka
Należy się z nim obchodzić bardzo ostrożnie. Jest związkiem silnie trującym, hamuje ważne procesy metaboliczne i prowadzi do śmierci przez połknięcie, wdychanie, wchłonięcie przez skórę lub kontakt z oczami..
Wdychany NaCN rozpuszcza się w błonie śluzowej dróg oddechowych i przenika do krwiobiegu. Jon cyjankowy NaCN ma silne powinowactwo do żelaza na stopniu utlenienia +3, czyli kation żelazowy Fe3+.
Wchłonięty cyjanek szybko reaguje z Fe3+ ważnego enzymu mitochondriów komórek (oksydaza cytochromowa), zapobiegając niektórym procesom oddychania tego.
W związku z tym oddychanie komórkowe jest hamowane lub spowalniane, co prowadzi do hipoksji cytotoksycznej. Oznacza to, że komórki i tkanki nie są w stanie zużywać tlenu, zwłaszcza komórki mózgu i serca.
W ten sposób dochodzi do trwałego lub śmiertelnego uszkodzenia ciała. Może to wystąpić zarówno u ludzi, jak iu zwierząt..
Połknięty powoduje przekrwienie naczyń krwionośnych i korozję błony śluzowej żołądka, oprócz wyżej wymienionych.

Nie jest palny, ale w kontakcie z kwasami uwalnia HCN, który jest wysoce łatwopalny i toksyczny.
Jeśli topi się z azotynami lub chloranami, może eksplodować.
Otrzymywanie
Można otrzymać z sodem Na, amoniakiem NH3 i węgiel C. Sód reaguje z amoniakiem, dając amidek sodu NaNHdwa:
2 Na + 2 NH3 → 2 NaNHdwa + H.dwa↑
Amidek sodu jest podgrzewany węglem drzewnym do 600 ° C i wytwarza cyjanamid sodu NadwaNCN, który jest następnie przekształcany w cyjanek sodu za pomocą węgla drzewnego w temperaturze 800 ° C:
2 NaNHdwa + C → 2 H.dwa↑ + NadwaNCN
NadwaNCN + C → 2 NaCN
Inną metodą jest stopienie cyjanamidu wapnia CaNCN i węgla C z węglanem sodu NadwaWSPÓŁ3:
CaNCN + C + NadwaWSPÓŁ3 → CaCO3 + 2 NaCN
Można go również przygotować przepuszczając azot Ndwa za pomocą gorącej mieszaniny Na węglanu sodudwaWSPÓŁ3 i sproszkowany węgiel C, wykorzystujący żelazo Fe jako katalizator lub przyspieszacz reakcji:
NadwaWSPÓŁ3 + 4 C + Ndwa → 2 NaCN + 3 CO ↑
Aplikacje
W wydobyciu minerałów złota i srebra. Konsekwencje
Cyjanek sodu był od dawna używany do ekstrakcji metali złota i srebra z ich rud..
Cyjanek użyty w procesie jest poddawany recyklingowi, ale wraz z nieodzyskanymi metalami ciężkimi przedostaje się do stawu ściekowego.
Ptaki, nietoperze i inne zwierzęta pijące z lagun cyjankowych zostały zatrute.
Istnieją zapisy o tamie w Rumunii, która odizolowała staw ściekowy i została uszkodzona przez zjawisko pogodowe..
W rezultacie tony cyjanku zostały uwolnione do rzeki Sasar i pobliskich systemów wodonośnych, takich jak Lapus, Somes i Cisa, kończąc się na Dunaju..
Spowodowało to kaskadę śmierci zwierząt lub innymi słowy katastrofę ekologiczną..

W produkcji innych związków chemicznych
Cyjanek sodu NaCN jest stosowany w syntezie różnego rodzaju związków organicznych.
Na przykład przygotowuje się pigmenty i barwniki (w tym rozjaśniacze optyczne), związki do użytku w rolnictwie lub w agrochemikaliach oraz różne farmaceutyki..
Służy również do otrzymywania środków chelatujących lub maskujących jony metali..
Związki zwane nitrylami są przygotowywane z cyjanku sodu NaCN, który po potraktowaniu gorącym kwaśnym lub zasadowym roztworem wodnym pozwala na otrzymanie kwasów karboksylowych.
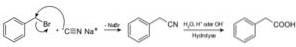
Pozwala na przygotowanie kwasów tłuszczowych z grupami cyjanowymi, cyjankami metali ciężkich i kwasem cyjanowodorowym lub cyjanowodorem HCN.
W przemyśle metalowym
NaCN jest stosowany w roztworach stosowanych w galwanotechnice lub galwanizacji metali (powlekanie metali innymi), np. Cynk.
Jest składnikiem ze stali hartowanej. Służy również do czyszczenia metali.
W innych zastosowaniach
Cyjanek sodu jest półproduktem w produkcji nylonu.
Służy do oddzielania minerałów metodą flotacji piany.
Aplikacje nieużywane, kwestionowane lub bardzo rzadkie
NaCN był używany do zabijania gryzoni, takich jak króliki i szczury oraz ich nor, a także do zabijania gniazd termitów.
Obecnie jest stosowany sporadycznie w celu wyeliminowania kojotów, lisów i dzikich psów. Stosowany w postaci kapsułek jako pojedyncze lub wielokrotne dawki na pastwiskach, terenach łowieckich i lasach.
Ze względu na ekstremalną toksyczność NaCN powinien być stosowany wyłącznie przez przeszkolone osoby..
To użycie jest uważane za bardzo niebezpieczne dla ludzi, ale są tacy, którzy nadal go używają.

W rolnictwie był dawniej używany do fumigacji drzew cytrusowych i innych owoców. Był również stosowany jako środek owadobójczy i roztoczobójczy (eliminator roztoczy) do stosowania po zbiorach, w przypadku nie przechowywanych owoców cytrusowych lub do fumigacji ciężarówek używanych do ich transportu. Służył również do odkażania statków, wagonów i magazynów..
Wszystkie te zastosowania zostały zakwestionowane ze względu na wysoką toksyczność cyjanku sodu. Z tego powodu nie jest już używany lub tylko bardzo rzadko iw bardzo kontrolowanych warunkach..
Bibliografia
- NAS. National Library of Medicine. (2019). Cyjanek sodowy. Odzyskany z pubchem.ncbi.nlm.nih.gov.
- Kirk-Othmer (1994). Encyklopedia technologii chemicznej. Czwarta edycja. John Wiley & Sons.
- Hurst, H.E. i Martin, M.D. (2017). Toksykologia. Cyjanek. In Pharmacology and Therapeutics for Dentistry (wydanie siódme). Odzyskany z sciencedirect.com.
- Coppock, R.W. oraz Dziwenka, M. (2015). Zagrożenia dla dzikiej przyrody ze strony agentów broni chemicznej. W Handbook of Toxicology of Chemical Warfare Agents (wydanie drugie). Odzyskany z sciencedirect.com.
- Morrison, R.T. i Boyd, R.N. (2002). Chemia organiczna. 6th Edition. Prentice-Hall.


Jeszcze bez komentarzy