
Izomeria
Co to jest izomeria?
Izomeria to zjawisko chemiczne charakteryzujące się tym, że cząsteczki o tej samej liczbie atomów mają różne właściwości chemiczne lub fizyczne. Występuje więc w izomerach, które z kolei są cząsteczkami, których wzory chemiczne są takie same, ale ich budowa lub rozmieszczenie przestrzenne znacznie się od siebie różni..
Mamy izomeria konstytucyjna lub strukturalna oraz izomeria przestrzenna, która skupia dużo uwagi na stereochemii. Schemat blokowy na poniższym obrazku pokazuje, że izomery są głównie podzielone na dwa typy izomerii, o których właśnie wspomniano: konstytucyjne i stereoizomery..
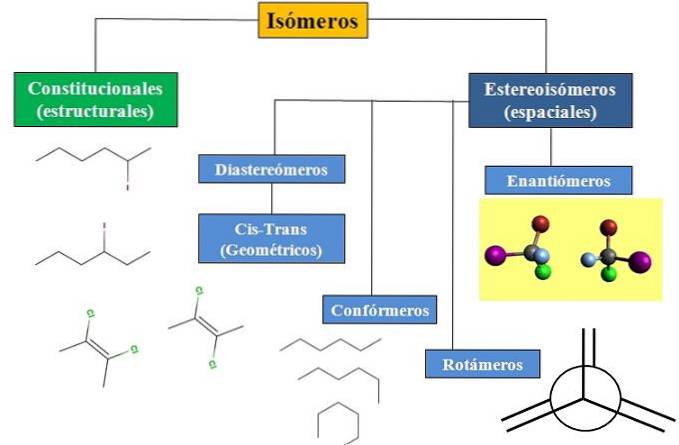
Wszystkie izomery dla określonego związku mają ten sam wzór chemiczny. Ale struktury, które te atomy mogą zbudować, i ich proporcje są unikalne dla każdej cząsteczki lub izomeru. Ponadto, chociaż sama struktura jest taka sama, atomy lub grupy mogą zajmować różne pozycje przestrzenne..
Schemat blokowy pokazuje kilka przykładów izomerów, które zostaną omówione w następnych rozdziałach..
Rodzaje izomerów
Konstytucyjny
Izomery konstytucyjne lub strukturalne to te, które różnią się kolejnością szkieletu molekularnego. Oznacza to, że ich atomy nie są połączone w ten sam sposób, więc struktura lub grupy funkcyjne, o których mowa, mogą się bardzo różnić..
Na przykład dla tego samego wzoru chemicznego C.7H.10Lub może istnieć wiele cząsteczek, które mają taką liczbę atomów; wszystkie będą miały jeden atom tlenu, ale układ strukturalny pozostałych atomów będzie niepowtarzalny dla każdego izomeru.
Stąd właściwości chemiczne i fizyczne wszystkich izomerów konstytucyjnych dla wzoru C.7H.10Lub też będą się znacznie od siebie różnić.
Z drugiej strony izomery konstytucyjne mogą być bardzo proste, różniąc się jedynie względną pozycją pojedynczego atomu lub grupy. W następnej sekcji zobaczysz przykład tego i powyższego.
Stereoizomery
Stereoizomery to te, które mają ten sam porządek strukturalny, ale różnią się położeniem i przestrzenną orientacją swoich atomów lub grup..
Aby ich istnienie było możliwe, cząsteczki muszą zawierać centra stereogeniczne, z których najsłynniejsze w chemii organicznej są asymetryczne lub chiralne atomy węgla; to znaczy z czterema różnymi podstawnikami.
Oprócz asymetrycznych atomów węgla w rozważanej cząsteczce musi brakować elementów symetrii. W przeciwnym razie porządkowanie przestrzenne nie może stać się stereoizomerią..
Enancjomery
Enancjomery są stereoizomerami składającymi się z nienakładających się odbić lustrzanych. Na przykład prawa i lewa ręka nie zachodzą na siebie, podobnie jak buty lub rękawiczki. Następna sekcja zajmie się klasycznym przykładem enancjomeru: bromochlorodometan: CBrClI.
Diastereomery
Z drugiej strony, diastereoizomery są również stereoizomerami, ale nie są odbiciami lustrzanymi. To znaczy, że umieszczone jedno przed drugim nie są odbiciem samych siebie. Spośród najbardziej znanych diastereoizomerów mamy izomię cis-trans, zwaną także izomerią geometryczną, zwłaszcza w przypadku zastosowania do alkenów.
Zgodni
Konformery, chociaż mieszczą się w spektrum stereoizomerii, w rzeczywistości nie są izomerami. Są to konfiguracje przestrzenne, które cząsteczka w pewnym momencie lub stanie energetycznym uzyskuje poprzez obroty kilku swoich wiązań. W następnej sekcji zobaczymy przykład konformerów n-heksan.
Rotamers
Wreszcie mamy rotamery, które przypominają konformery w tym sensie, że zależą od rotacji wiązań kowalencyjnych..
Jednak jako odniesienie przyjmuje się pojedyncze wiązanie między dwoma atomami węgla i porównuje się względne pozycje podstawników obu atomów węgla, zaćmione lub naprzemienne. Później zobaczymy przykład rotamerów propylenu.
Przykłady izomerów
Jod heksanu
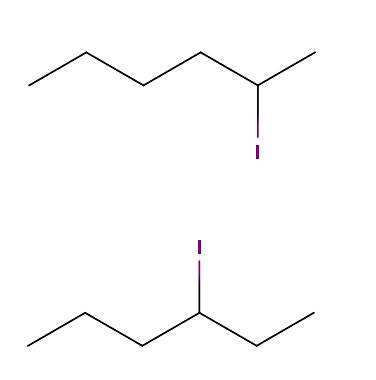
Powyżej mamy dwie cząsteczki, których wzory chemiczne to C6H.13I. W pierwszej mamy 2-jodoheksan, w drugiej 3-jodoheksan. Są to izomery konstytucyjne typu pozycyjnego, ponieważ szkielet jest taki sam, z tą różnicą, że położenie atomu jodu zmienia się w zależności od węgla..
do3H.8LUB
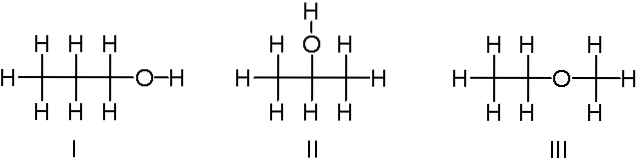
Powyżej mamy inny przykład izomerów konstytucyjnych dla wzoru chemicznego C.3H.8O. Cząsteczki I i II to odpowiednio 1-propanol i 2-propanol. Oba są alkoholami. Zamiast tego cząsteczka III dotyczy eteru etylowo-metylowego.
Dlatego mówimy o innej grupie funkcjonalnej. Zwróć uwagę, że te trzy cząsteczki mają taką samą liczbę atomów, ale ich struktury są różne..
2,3-dichloro-2-buten
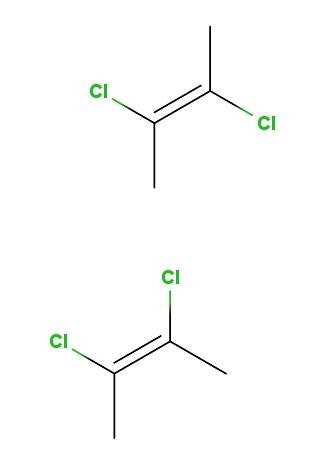
Powyżej mamy izomer trans-2,3-dichloro-2-butenu, a poniżej izomer cis-2,3-dichloro-2-butenu. W pierwszym atomy chloru znajdują się w przeciwnych pozycjach w stosunku do wiązania podwójnego, podczas gdy w drugim znajdują się po tej samej stronie wiązania podwójnego..
Szkielet obu cząsteczek jest taki sam, ale różnią się one przestrzennymi położeniami atomów chloru; dlatego są stereoizomerami, a ponieważ nie są odbiciami lustrzanymi, stają się diastereomerami.
3-fluoro-2-metylocykloheksan
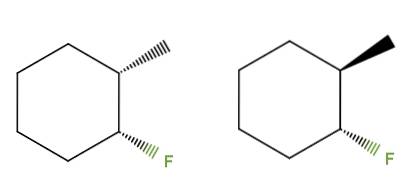
Tym razem zamiast podwójnego wiązania mamy pierścień cykloheksanowy dla związku 3-fluoro-2-metylocykloheksanu. W lewym izomerze grupy CH3 a F są poniżej płaszczyzny pierścienia; podczas gdy w tym po prawej stronie, CH3 jest w górę, a F jest w dół.
Dlatego ten po lewej stronie odpowiadałby izomerowi cis, a ten po prawej byłby izomerem trans. Są zatem diastereomerami, ponieważ znowu nie są odbiciami lustrzanymi.
Zgodni z n-heksan
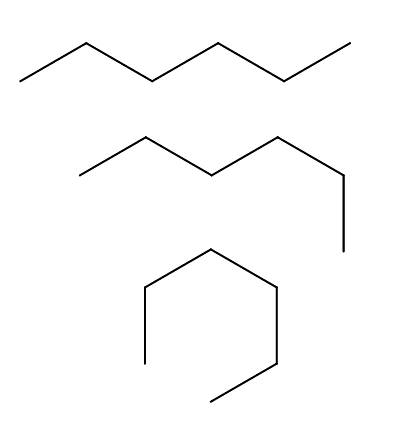
Mamy powyżej trzech konformerów n-heksan, które powstają w wyniku rotacji i „zagięć” łańcucha węglowego w różnych orientacjach. Wszystkie odpowiadają tej samej cząsteczce n-heksan o różnych poziomach fałdowania, które będą zależeć od środowiska i energii wewnętrznej każdej cząsteczki.
3-bromo-2-pentanol
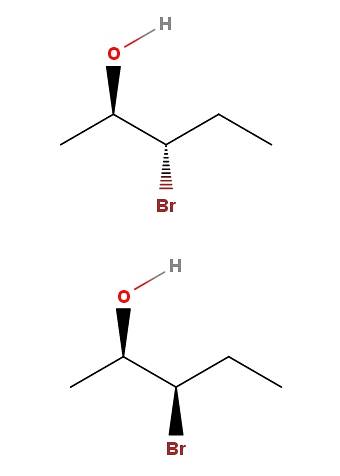
W 3-bromo-2-pentanolu mamy inny przykład pary diastereomerów. Zauważ, że ponownie w izomerze powyżej mamy OH i Br wskazujące w przeciwnych kierunkach płaszczyzny szkieletu; podczas gdy w niższym izomerze obie grupy wskazują kierunek czytelnika.
1-bromo-3-chloro-5-etylocykloheksan
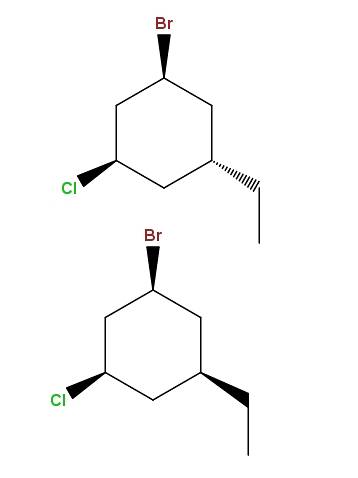
I znowu mamy kolejną parę diastereoizomerów, z tą różnicą, że teraz różnica polega na położeniu przestrzennym pojedynczej grupy: etylowej, -CHdwaCH3.
Ten typ izomerów ma bardzo specyficzną nazwę: epimery, które są diastereomerami, których zmienność obserwuje się tylko w konfiguracji przestrzennej pojedynczego asymetrycznego węgla; w tym przypadku ten powiązany z -CHdwaCH3.
Bromochlorooyodometan
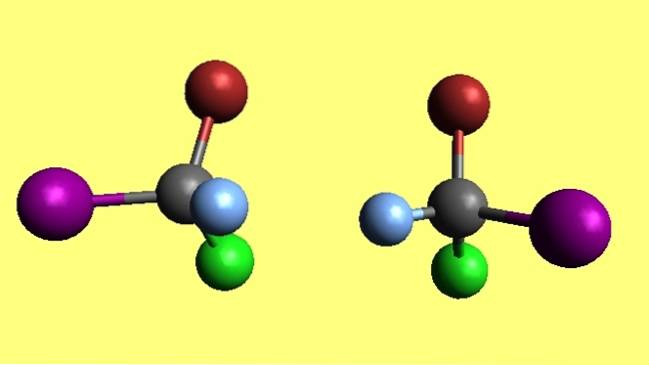
Należy zauważyć, że dwie cząsteczki bromochlorojodometanu, CBrClI, są enancjomerami, ponieważ jedna jest nienakładającym się odbiciem drugiej. Bez względu na to, jak bardzo się starasz, jego cztery atomy nigdy nie będą pasować. Mówi się, że mają przeciwne konfiguracje przestrzenne.
2-bromo-4-etylocykloheksan
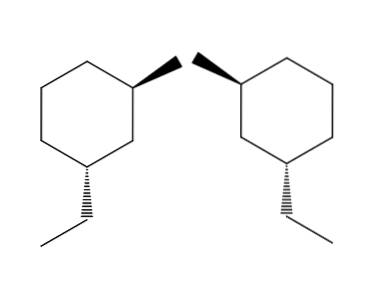
Na przykładzie pary cząsteczek 2-bromo-4-etylocykloheksan enancjomer jest jeszcze bardziej oczywisty. Jeśli spróbujemy odwrócić cząsteczkę po prawej stronie, zobaczymy, że jest to grupa -CHdwaCH3 nie będzie znajdować się poniżej pierścienia, ale powyżej.
Podobnie CH3 Nie będzie skierowany w górę pierścienia, ale poniżej. Konfiguracje przestrzenne są odwrócone, są przeciwne. To kolejna z najważniejszych cech enancjomeru..
Rotamery propylenowe
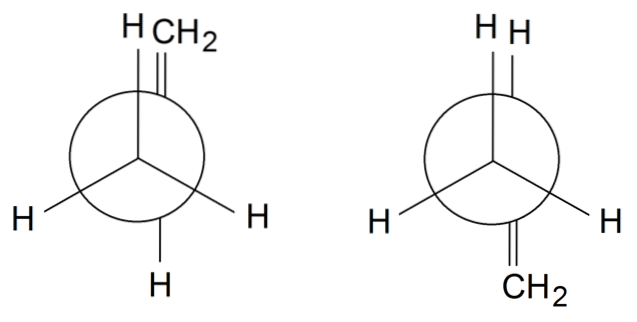
W rotamerach propylenowych, aby zakończyć, obracamy pojedyncze wiązanie między C1 i Cdwa: H3C-CH = CHdwa. Grupa = CHdwa znajduje się w zaćmionej pozycji z jednym z H grupy CH3 przód na rotametrze po lewej stronie. Tymczasem = CHdwa i H są w naprzemiennych pozycjach na prawym rotamerze.
W zależności od zaćmienia grup lub nie, będziemy mieli zawadę steryczną, która zdestabilizuje rotamer. Dlatego rotamer po prawej stronie jest bardziej stabilny niż ten po lewej..
Bibliografia
- Graham Solomons T.W., Craig B. Fryhle. (2011). Chemia organiczna. (10th wydanie.). Wiley plus.
- Carey F. (2008). Chemia organiczna. (Wydanie szóste). Mc Graw Hill.
- Morrison i Boyd. (1987). Chemia organiczna. (Piąta edycja). Addison-Wesley Iberoamericana.
- Dr. S. Gevorg. (2020). Enancjomery, diastereoizomery, identyczne lub konstytucyjne izomery. Etapy chemii. Źródło: chemistrysteps.com
- Wikipedia. (2020). Izomer. Odzyskane z: en.wikipedia.org
- Allison Soult. (13 sierpnia 2020). Izomery. Chemia LibreTexts. Źródło: chem.libretexts.org
- James Ashenhurst. (2020). Stereochemia i chiralność. Odzyskane z: masterorganicchemistry.com



Jeszcze bez komentarzy