
Struktura azotku boru (BN), właściwości, wytwarzanie, zastosowania

Plik azotek boru Jest to nieorganiczna substancja stała utworzona przez połączenie atomu boru (B) z atomem azotu (N). Jego wzór chemiczny to BN. Jest to białe ciało stałe, które jest bardzo odporne na wysokie temperatury i jest dobrym przewodnikiem ciepła. Służy na przykład do produkcji tygli laboratoryjnych.
Azotek boru (BN) jest odporny na wiele kwasów, ma jednak pewną słabość do ataku kwasu fluorowodorowego i stopionych zasad. Jest dobrym izolatorem prądu.
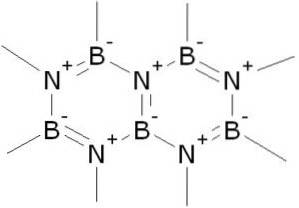
Otrzymywany jest w różnych strukturach krystalicznych, z których najważniejsze są heksagonalne i sześcienne. Struktura heksagonalna przypomina grafit i jest śliska, dlatego znajduje zastosowanie jako smar.
Sześcienna struktura jest prawie tak twarda jak diament i służy do wykonywania narzędzi skrawających i poprawiania udarności innych materiałów.
Azotek boru może wytwarzać mikroskopijne (niezwykle cienkie) rurki zwane nanorurkami, które mają zastosowania medyczne, takie jak transport w organizmie i uwalnianie leków przeciw nowotworom..
Indeks artykułów
- 1 Struktura
- 2 Nazewnictwo
- 3 Właściwości
- 3.1 Stan fizyczny
- 3.2 Masa cząsteczkowa
- 3.3 Temperatura topnienia
- 3.4 Gęstość
- 3.5 Rozpuszczalność
- 3.6 Właściwości chemiczne
- 3.7 Inne właściwości fizyczne
- 4 Otrzymywanie
- 5 zastosowań
- 5.1 - Zastosowania cienkich warstw BN
- 5.2 - Zastosowania nanorurek BN
- 6 Możliwa toksyczność materiałów BN
- 7 Referencje
Struktura
Azotek boru (BN) to związek, w którym atomy boru i azotu są kowalencyjnie połączone wiązaniem potrójnym.
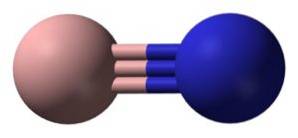
W fazie stałej BN tworzy równa liczba atomów boru i azotu w postaci 6-członowych pierścieni..
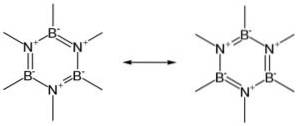
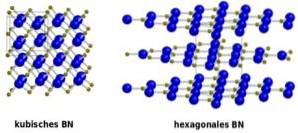
BN występuje w czterech formach krystalicznych: heksagonalnej (h-BN) podobnej do grafitu, sześciennej (c-BN) podobnej do diamentu, romboedrycznej (r-BN) i wurtzytu (w-BN).
Struktura h-BN jest podobna do grafitu, to znaczy ma płaszczyzny sześciokątnych pierścieni, które mają naprzemiennie atomy boru i azotu..
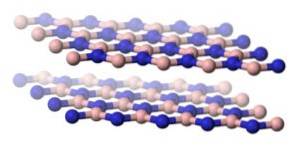
Między płaszczyznami h-BN jest duża odległość, co sugeruje, że łączą je tylko siły van der Waalsa, które są bardzo słabymi siłami przyciągania i płaszczyzny mogą łatwo ślizgać się po sobie..
Z tego powodu h-BN jest tłusty w dotyku..
Struktura sześciennego BN c-BN jest podobna do diamentu.
Nomenklatura
Azotek boru
Nieruchomości
Stan fizyczny
Tłuste białe ciało stałe lub śliskie w dotyku.
Waga molekularna
24,82 g / mol
Temperatura topnienia
Sublimuje w temp. Ok. 3000 ºC.
Gęstość
Sześciokąt BN = 2,25 g / cm3
Sześcienny BN = 3,47 g / cm3
Rozpuszczalność
Słabo rozpuszczalny w gorącym alkoholu.
Właściwości chemiczne
Dzięki silnemu wiązaniu azotu i boru (wiązanie potrójne) azotek boru ma wysoką odporność na atak chemiczny i jest bardzo stabilny.
Jest nierozpuszczalny w kwasach, takich jak kwas solny HCl, kwas azotowy HNO3 i kwas siarkowy H.dwapołudniowy zachód4. Ale jest rozpuszczalny w stopionych zasadach, takich jak wodorotlenek litu LiOH, wodorotlenek potasu KOH i wodorotlenek sodu NaOH.
Nie reaguje z większością metali, szkieł ani soli. Czasami reaguje z kwasem fosforowym H.3PO4. Może być odporny na utlenianie w wysokich temperaturach. BN jest stabilny w powietrzu, ale jest powoli hydrolizowany przez wodę.
BN jest atakowany przez gaz fluorowy F.dwa i kwasem fluorowodorowym HF.
Inne właściwości fizyczne
Ma wysoką przewodność cieplną, wysoką stabilność termiczną i wysoką rezystywność elektryczną, to znaczy jest dobrym izolatorem energii elektrycznej. Ma dużą powierzchnię.
H-BN (heksagonalny BN) to tłusta substancja stała w dotyku, podobna do grafitu.
Podczas ogrzewania h-BN w podwyższonej temperaturze i ciśnieniu przekształca się w sześcienną formę c-BN, która jest niezwykle twarda. Według niektórych źródeł jest w stanie zarysować diament.
Materiały na bazie BN mają zdolność pochłaniania zanieczyszczeń nieorganicznych (takich jak jony metali ciężkich) i zanieczyszczeń organicznych (takich jak barwniki i cząsteczki leków)..
Sorpcja oznacza, że oddziałuje z nimi i może je adsorbować lub absorbować.
Otrzymywanie
Proszek H-BN jest wytwarzany w reakcji między trójtlenkiem boru B.dwaLUB3 lub kwas borowy H.3BO3 z amoniakiem NH3 lub z mocznikiem NHdwa(CO) NHdwa w atmosferze azotu Ndwa.
BN można również otrzymać w reakcji boru z amoniakiem w bardzo wysokiej temperaturze..
Innym sposobem przygotowania jest diboran B.dwaH.6 i amoniak NH3 przy użyciu gazu obojętnego i wysokich temperatur (600-1080 ° C):
bdwaH.6 + 2 NH3 → 2 BN + 6 Hdwa
Aplikacje
H-BN (heksagonalny azotek boru) ma wiele ważnych zastosowań w oparciu o jego właściwości:
-Jako stały smar
-Jako dodatek do kosmetyków
-W izolatorach elektrycznych o wysokiej temperaturze
-W tyglach i naczyniach reakcyjnych
-W formach i naczyniach wyparnych
-Do przechowywania wodoru
-W katalizie
-Do adsorpcji zanieczyszczeń ze ścieków
Zastosowano sześcienny azotek boru (c-BN) ze względu na jego twardość prawie równą twardości diamentu:
-W narzędziach skrawających do obróbki twardych materiałów żelaznych, takich jak twarde stopy stali, żeliwa i stale narzędziowe
-Aby poprawić twardość i odporność na zużycie innych twardych materiałów, takich jak niektóre materiały ceramiczne do narzędzi skrawających.

- Zastosowania cienkich folii BN
Są bardzo przydatne w technologii przyrządów półprzewodnikowych, które są elementami wyposażenia elektronicznego. Służą między innymi:
-Aby zrobić płaskie diody; diody to urządzenia, które umożliwiają przepływ energii elektrycznej tylko w jednym kierunku
-W diodach pamięci metal-izolator-półprzewodnik, takich jak Al-BN-SiOdwa-tak
-W układach scalonych jako ogranicznik napięcia
-Aby zwiększyć twardość niektórych materiałów
-Aby chronić niektóre materiały przed utlenianiem
-Aby zwiększyć stabilność chemiczną i izolację elektryczną wielu typów urządzeń
-W kondensatorach cienkowarstwowych

- Zastosowania nanorurek BN
Nanorurki to struktury, które na poziomie molekularnym mają kształt rur. Są to rurki tak małe, że można je zobaczyć tylko za pomocą specjalnych mikroskopów.
Oto niektóre cechy nanorurek BN:
-Mają wysoką hydrofobowość, czyli odpychają wodę
-Posiadają wysoką odporność na utlenianie i ciepło (wytrzymują utlenianie do 1000 ° C)
-Wykazują dużą zdolność magazynowania wodoru
-Absorbuj promieniowanie
-Są bardzo dobrymi izolatorami elektryczności
-Mają wysoką przewodność cieplną
-Ich doskonała odporność na utlenianie w wysokich temperaturach sprawia, że można je stosować do zwiększania stabilności oksydacyjnej powierzchni..
-Ze względu na swoją hydrofobowość mogą być stosowane do przygotowania powierzchni superhydrofobowych, czyli nie mają powinowactwa do wody i woda ich nie przenika.
-Nanorurki BN poprawiają właściwości niektórych materiałów, np. Zastosowano je w celu zwiększenia twardości i odporności na pękanie szkła.

W zastosowaniach medycznych
Nanorurki BN zostały przetestowane jako nośniki leków przeciwnowotworowych, takich jak doksorubicyna. Pewne kompozycje zawierające te materiały zwiększały skuteczność chemioterapii tym lekiem..
W kilku doświadczeniach wykazano, że nanorurki BN mają potencjał do transportowania nowych leków i ich prawidłowego uwalniania.
Zastosowanie nanorurek BN w biomateriałach polimerowych zostało zbadane w celu zwiększenia ich twardości, szybkości degradacji i trwałości. Są to materiały, które znajdują zastosowanie np. W implantach ortopedycznych.
Jako czujniki
Nanorurki BN zostały wykorzystane do budowy nowatorskich urządzeń do wykrywania wilgoci, dwutlenku węgla i COdwa i do diagnozy klinicznej. Czujniki te wykazały szybką reakcję i krótki czas przywracania..
Możliwa toksyczność materiałów BN
Istnieją pewne obawy co do możliwych toksycznych skutków nanorurek BN. Nie ma jasnego konsensusu co do ich cytotoksyczności, ponieważ niektóre badania wskazują, że są toksyczne dla komórek, podczas gdy inne wskazują na coś przeciwnego..
Wynika to z jej hydrofobowości lub nierozpuszczalności w wodzie, co utrudnia prowadzenie badań na materiałach biologicznych..
Niektórzy badacze pokryli powierzchnię nanorurek BN innymi związkami, które sprzyjają ich rozpuszczalności w wodzie, ale zwiększyło to niepewność w doświadczeniach.
Chociaż większość badań wskazuje, że jego poziom toksyczności jest niski, szacuje się, że należy przeprowadzić dokładniejsze badania.
Bibliografia
- Xiong, J. i in. (2020). Sześciokątny adsorbent azotku boru: synteza, dostosowywanie wydajności i zastosowania. Journal of Energy Chemistry 40 (2020) 99-111. Odzyskany z reader.elsevier.com.
- Mukasyan, A.S. (2017). Azotek boru. W zwięzłej encyklopedii samorozprężającej się syntezy wysokotemperaturowej. Odzyskany z sciencedirect.com.
- Kalay, S. i in. (2015). Synteza nanorurek z azotku boru i ich zastosowania. Beilstein J. Nanotechnol. 2015, 6, 84-102. Odzyskany z ncbi.nlm.nih.gov.
- Arya, S.P.S. (1988). Przygotowanie, właściwości i zastosowania cienkich warstw azotku boru. Thin Solid Films, 157 (1988) 267-282. Odzyskany z sciencedirect.com.
- Zhang, J. i in. (2014). Kompozyty na osnowie ceramicznej zawierające regularny azotek boru do narzędzi skrawających. Postępy w kompozytach z matrycą ceramiczną. Odzyskany z sciencedirect.com.
- Cotton, F. Albert i Wilkinson, Geoffrey. (1980). Zaawansowana chemia nieorganiczna. Czwarta edycja. John Wiley & Sons.
- Sudarsan, V. (2017). Materiały dla wrogich środowisk chemicznych. W materiałach w ekstremalnych warunkach. Odzyskany z sciencedirect.com
- Dean, J.A. (redaktor) (1973). Podręcznik chemii Lange'a. McGraw-Hill Company.
- Mahan, B.H. (1968). Chemia uniwersytecka. Inter-American Educational Fund, S.A.


Jeszcze bez komentarzy