
Charakterystyka papopawirusa, taksonomia, morfologia, patologia
Papopavirus (Papovaviridae) to rodzina małych wirusów, która obejmuje Wirus poliomawirusowy Y Wirus brodawczaka. Organizacja genomu między tymi wirusami znacznie się różni. Dlatego niektórzy autorzy określają go jako podrodziny, czyli podrodzinę Polyomaviridae i podrodziny Papilomaviridae.
Plik Polyomaviridae zawierają wirusa JC wyizolowanego z tkanek mózgu pacjentów z postępującą wieloogniskową leukoencefalopatią; Wirus BK, izolowany z moczu biorców nerki z immunosupresją, powodujący krwotoczne zapalenie pęcherza moczowego lub nefropatię; oraz wirus SV40, wirus wakuolizacji Simios 40, który atakuje głównie te zwierzęta.
Ze swojej strony Papilomaviridae zawierają ponad 70 serotypów ludzkiego wirusa brodawek, lepiej znanego jako wirus brodawczaka ludzkiego (HPV). Wirusy te są szeroko rozpowszechnione na całym świecie.
Czynniki te mają powolny cykl rozwojowy, stymulują syntezę komórkowego DNA i replikują się w jądrze. Dlatego infekcje, które wywołują, są utajone i przewlekłe u ich naturalnych żywicieli..
Cierpienie z powodu tych patologii wiąże się z rozwojem chorób rakotwórczych u ssaków.
W przypadku wirusa brodawczaka występuje to u żywicieli naturalnych, u których zakażenie HPV jest silnie związane z pojawieniem się przednowotworowych i złośliwych chorób sromu, szyjki macicy, prącia i odbytu..
Podczas gdy w poliomawirusach pojawienie się guzów obserwowano tylko u zwierząt doświadczalnych, z wyjątkiem SV40, który powoduje nowotwory u ludzi..
Indeks artykułów
- 1 Charakterystyka ogólna
- 1.1 Charakterystyka wirusa brodawczaka ludzkiego
- 2 Taksonomia
- 3 Morfologia
- 3.1 Poliomawirus
- 3.2 Wirus brodawczaka
- 4 Patogeneza
- 4.1 Poliomawirus
- 4.2 Wirus brodawczaka
- 5 Patologia
- 5.1 Poliomawirus
- 5.2 Wirus brodawczaka
- 6 Diagnoza
- 6.1 Wirus brodawczaka
- 6.2 Poliomawirus
- 7 Referencje
Ogólna charakterystyka
Wirusy te mają ludzi i zwierzęta jako swoje naturalne środowisko. Formą przenoszenia jest kontakt z zakażonymi wydzielinami.
Drogi wnikania są skórne, narządów płciowych (ETS) lub oddechowe w przypadku wirusów brodawczaka, podczas gdy w przypadku poliomawirusów nie są znane, ale uważa się, że może to być droga oddechowa.
Zarówno wirusy poliomawirusowe, jak i wirusy brodawczaka, po dostaniu się do organizmu, pozostają w tkankach w stanie utajonym.
Patologie można leczyć, ale jeśli występuje immunosupresja, mogą wystąpić nawroty z powodu reaktywacji wirusa.
Charakterystyka wirusa brodawczaka ludzkiego
HPV dzieli się na 2 grupy ze względu na powinowactwo do tkanek: skórne tropiki to te, które mają skłonność do skóry, a śluzowate to te, które mają największe powinowactwo do błon śluzowych..
Wśród serotypów HPV zaobserwowano powiązania między niektórymi genotypami a typem zmiany klinicznej. Istnieją również serotypy bardziej onkogenne niż inne. Na przykład serotypy HPV 16 i HPV 18, które powodują brodawki narządów płciowych, są obarczone wysokim ryzykiem.
W przypadku serotypu HPV-16 kojarzy się z rogowaciejącymi rakami płaskonabłonkowymi, natomiast HPV-18 z gruczolakorakami..
Podobnie, u pacjentów dotkniętych brodawkowatym naskórkiem wywołanym przez serotypy 5 i 8 HPV, odnotowuje się wysoki wskaźnik późniejszego rozwoju raka płaskonabłonkowego w wyniku zmian..
Podsumowując, serotypy wysokiego ryzyka to: 16, 18, 31, 33, 35, 39, 45, 51, 52, 56, 58, 59, 68, 82, 26, 53, 66. I niskiego ryzyka: 6, 11, 40, 42, 43, 44, 54, 62, 72, 81.
Taksonomia
Grupa DsDNA 1.
Rodzina: Papovaviridae.
Rodzaj: Polyomavirus i Papillomavirus.
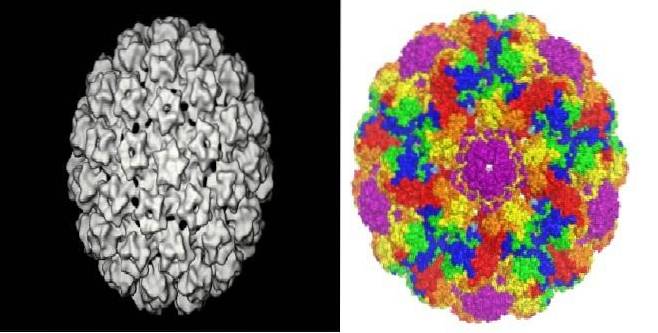
Morfologia
Plik Papowawirus na ogół mają rozmiar 45-55 nm, symetrię ikozaedryczną i nie mają otoczki lipidowej. Posiadają genom kolistego dwuniciowego DNA.
Wirus poliomawirusowy
Poliomawirusy składają się z dwóch lub 3 replikacyjnych genów zwanych antygenami nowotworowymi kodowanymi przez jedną z nici DNA i trzech genów strukturalnych, zwanych antygenami kapsydu, kodowanymi na drugiej nici..
Poliomawirusy ludzkie i zwierzęce różnią się pod względem antygenowym, a każdy z nich ma tylko jeden serotyp. Prototypowym wirusem jest małpi wirus 40 małp.
Wirus brodawczaka
Wirusy brodawczaków są podobne do wirusów poliomawirusowych, jednak wykazują pewne różnice. Wśród nich: cząsteczki wirusa mają średnicę 55 nm, a budowa genomu jest bardziej złożona. Wszystkie geny wirusowe są kodowane na pojedynczej nici DNA.
Wirus HPV zawiera 2 białka L1 i L2, a także ma onkoproteiny wirusowe, które oddziałują z białkami supresorowymi nowotworów.
Patogeneza
Wirus poliomawirusowy
U ludzi wywołują utajone infekcje w różnych miejscach w zależności od wirusa. Na przykład wirusy KV i SV40 przetrwały w komórkach nerek.
Podczas gdy wirus JC pozostaje utajony w tkance migdałków, w tkance zrębowej szpiku kostnego, w komórkach nabłonka okrężnicy i nerek, pośród innych tkanek, przez czas nieokreślony..
Większość infekcji przebiega bezobjawowo. Wirusy te reaktywują się i powodują objawową chorobę tylko u pacjentów z obniżoną odpornością..
Wirus brodawczaka
W przypadku wirusa HPV łuski powstałe w wyniku złuszczania skóry są ważnym źródłem zakażenia, podobnie jak kontakty seksualne.
Wirus brodawczaka ludzkiego ma predyspozycje do infekowania komórek miejsca przyczepu nabłonka płaskiego i walcowatego, sromu, szyjki macicy i odbytu, które są najbardziej wrażliwymi miejscami..
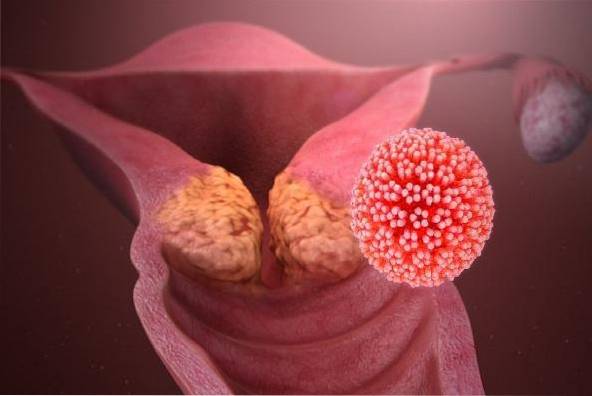
Replikacja i składanie wirusa zachodzi w warstwach nabłonka płaskiego w procesie różnicowania, ponieważ wirus początkowo infekuje warstwę podstawną nabłonka, w której znajduje się wirusowe DNA..
Ale ekspresja białek kapsydu i tworzenie całego wirusa zachodzi w najbardziej powierzchownej warstwie zróżnicowanych keratynocytów, czyli wtedy, gdy komórki kończą dojrzewanie.
Dlatego, aby móc się namnażać, wirus potrzebuje, aby komórki znajdowały się w procesie różnicowania (dojrzewania), przez co nie jest możliwa hodowla in vitro, ponieważ chociaż istnieją hodowle komórkowe, nie są w stanie ukończyć ich etap różnicowania w tych warunkach i dlatego wirus również nie może się replikować.
Należy zauważyć, że wirus HPV może wywołać lityczną infekcję w zrogowaciałych komórkach nabłonka powierzchownego lub może pozostawać uśpiony w głębszych warstwach, utrzymując się w nim przez lata..
Podobnie ważne jest, aby pamiętać, że komórki, które złuszczają się lub złuszczają z zaatakowanego nabłonka, zostaną obciążone wirusem, co pomoże w jego rozprzestrzenianiu..
Z drugiej strony, jeśli DNA jest zintegrowane z DNA komórkowym, może powodować onkogenną transformację komórki gospodarza..
W ten sposób aktywowane są wirusowe geny E6 i E7, które uszkadzają gen p53 komórki podstawnej. Ten gen jest odpowiedzialny za korygowanie błędów, które mogą wystąpić podczas rozmnażania komórek. Kiedy gen jest uszkodzony, nie może pełnić swojej funkcji, dlatego komórki stają się nowotworowe.
Z drugiej strony wirus wytwarza onkogenne białko p105 i tworzy kompleks z genem RB, aby je uszkodzić..
Gen RB kontroluje i reguluje rozmnażanie komórek, informując komórki, kiedy mają się rozmnażać, a kiedy odpoczywać.
Blokując jego funkcję, komórki rozmnażają się bez zatrzymywania się i stają się rakowe.
Patologia
Wirus poliomawirusowy
Wirus JC jest neurotropowy i powoduje postępującą wieloogniskową leukoencefalopatię. Ta rzadka choroba atakuje pacjentów z obniżoną odpornością. Wirus replikuje się w oligodendrocytach, powodując demielinizację ośrodkowego układu nerwowego (destrukcyjne zapalenie mózgu).
Podobnie wirus stymuluje układ odpornościowy i indukuje humoralną i komórkową odpowiedź immunologiczną (cytotoksyczna T), kontrolując infekcję, która pozostaje utajona. Wirus jest reaktywowany, gdy układ odpornościowy jest osłabiony, co powoduje pogorszenie odporności komórkowej niezbędnej do rozwoju choroby.
Interferon może hamować poliomawirusa, chociaż jest słabo indukowany podczas infekcji.
Wirus JC powoduje nowotwory u myszy laboratoryjnych, ale nie u ludzi. Zarówno wirusy JC, BK, jak i SV40 były związane z przypadkami krwotocznego zapalenia pęcherza moczowego i postępującej wieloogniskowej leukoencefalopatii.
Chociaż BK i SV40 są również związane z przypadkami nefropatii.
Z drugiej strony, SV40 wiązano z niektórymi nowotworami u ludzi, w tym pierwotnymi guzami mózgu, złośliwymi międzybłoniakami, rakami kości i chłoniakami nieziarniczymi..
Jeśli chodzi o formę przenoszenia wirusów JC i BK, nie jest znana, ale uważa się, że może to być droga oddechowa, podczas gdy wirus wakuolizujący małpi 40 dotknął ludzi z powodu przypadkowego skażenia szczepionek przeciwko polio wirusem SV 40.
Wirus brodawczaka
Wirusy brodawczaków są odpowiedzialne za łagodne zmiany brodawczakowate skóry i błon śluzowych.
Zmiany te mogą przedstawiać się jako brodawki zwykłe, brodawki płaskie, brodawki podeszwowe, brodawki odbytowo-płciowe, brodawczaki naskórka i brodawczaki krtani..
Z drugiej strony istnieje bardzo ścisły związek między pojawieniem się śródnabłonkowej neoplazji szyjki macicy, rakiem szyjki macicy i guzami dróg oddechowych z zakażeniem wirusem brodawczaka ludzkiego..
Diagnoza
Wirus brodawczaka
Prostym testem w profilaktyce raka szyjki macicy jest coroczny test cytologiczny z szyjki macicy, barwiony techniką cytologii. Ten test ujawnia patognomoniczne cechy zakażenia HPV..
Cechą diagnostyczną komórki zakażonej wirusem HPV jest koilocytoza, czyli obecność okołojądrowego halo nabłonka płaskonabłonkowego, któremu towarzyszy atypia jądrowa.
Do zidentyfikowania zaangażowanego serotypu niezbędne są testy biologii molekularnej. Podobnie, kolposkopia jest techniką, która pomaga w poszukiwaniu zmian na szyjce macicy, które mogą być spowodowane przez HPV..
Wirus poliomawirusowy
DNA VBK można wykryć w osadzie moczu, krwi lub komórkach zakażonych wtrąceniami wirusowymi, z próbek tkanki nerki lub nabłonka dróg moczowych, poprzez badanie wykrywania DNA metodą PCR..
W diagnostyce postępującej wieloogniskowej leukoencefalopatii wirusa JC ważny jest aspekt kliniczny, a także pomocne jest wykorzystanie badań obrazowych i laboratoryjnych..
Bibliografia
- Burgos B, Jironda C, Martín M González-Molina M, Hernández, D. Nephropathy Associated with Infection by Polyomavirus Bk. Nefrologia 2010; 30: 613-7
- Walker DL, Padgett BL, ZuRhein GM, Albert AE, Marsh RF. Papowawirus ludzki (JC): indukcja guzów mózgu u chomików. Nauka. 1973 17 sierpnia; 181 (4100): 674-6.
- Koneman E, Allen S, Janda W, Schreckenberger P, Winn W. (2004). Diagnoza mikrobiologiczna. (Wyd. 5). Argentyna, od redakcji Panamericana S.A.
- Forbes B, Sahm D, Weissfeld A (2009). Diagnoza mikrobiologiczna Bailey & Scott. 12 ed. Argentyna. Od redakcji Panamericana S.A;
- Ryan KJ, Ray C. 2010. Sherris. Mikrobiologia Medical, 6. wydanie McGraw-Hill, Nowy Jork, USA
- González M, González N. Podręcznik mikrobiologii medycznej. 2. edycja, Wenezuela: Dyrekcja ds. Mediów i publikacji Uniwersytetu w Carabobo; 2011.
- Cedeno F, Penalva de Oliveira AC, Vidal JE, Trujillo JR. Wirusy neurotropowe: wirus JC i postępująca wieloogniskowa leukoencefalopatia. Rev Mex Neuroci 2006; 7 (1): 46–54
- Vilchez R, Kozinetz C, Arrington A, Madden C, Butel J. Małpi wirus 40 w raku człowieka. Am J. Med. 1 czerwca 2003; 114 (8): 675–84.



Jeszcze bez komentarzy