
Struktura chemiczna propylenu, właściwości i zastosowania

Plik propylen lub propen w temperaturze otoczenia i ciśnieniu atmosferycznym jest w stanie gazowym i podobnie jak inne alkeny jest bezbarwny. Ma zapach podobny do oleju, ale mniej intensywny. Przedstawia moment dipolowy, ponieważ chociaż brakuje mu silnego wiązania polarnego, jego cząsteczka jest asymetryczna.
Podobnie propylen jest izomerem strukturalnym cyklopropanu (mają ten sam wzór chemiczny C.3H.6). Występuje w przyrodzie w wyniku procesów wegetacji i fermentacji. Jest sztucznie wytwarzany podczas przetwarzania paliw kopalnych, takich jak ropa naftowa, gaz ziemny i, w mniejszym stopniu, węgiel.

Podobnie etylen i propylen są produktami rafinacji ropy naftowej w procesie rozszczepiania dużych cząsteczek węglowodorów w celu wytworzenia małych węglowodorów, na które jest duże zapotrzebowanie..
Propylen można również otrzymać różnymi metodami:
- W wyniku odwracalnej reakcji etylenu i butenu, gdzie podwójne wiązania są rozrywane i przekształcane w propylen.
- Poprzez proces odwodornienia (utraty wodoru) propanu.
- W ramach programu produkcji olefin z metanolu (MTO) propylen został wyprodukowany z metanolu. Zostało to przepuszczone przez katalizator zeolitowy, który sprzyja jego odwodnieniu i prowadzi do powstania etylenu i propylenu..
3CH3OH (metanol) => CH3CH = CHdwa (propylen) + 3HdwaO (woda)
Indeks artykułów
- 1 Struktura chemiczna
- 2 Właściwości
- 2.1 Masa cząsteczkowa
- 2.2 Temperatura wrzenia
- 2.3 Temperatura topnienia
- 2.4 Temperatura zapłonu
- 2.5 Rozpuszczalność
- 2.6 Rozpuszczalność wyrażona jako masa
- 2.7 Gęstość
- 2.8 Gęstość par
- 2.9 Prężność par
- 2.10 Samozapłon
- 2.11 Lepkość
- 2.12 Ciepło spalania
- 2.13 Ciepło parowania
- 2.14 Napięcie powierzchniowe
- 2.15 Polimeryzacja
- 2.16 Punkt zamarzania
- 2.17 Próg zapachu
- 3 Zastosowania
- 3.1 Polipropylen
- 3.2 Akrylonitryl
- 3.3 Tlenek propylenu
- 3.4 Do syntezy alkoholi i innych zastosowań
- 4 Odnośniki
Struktura chemiczna
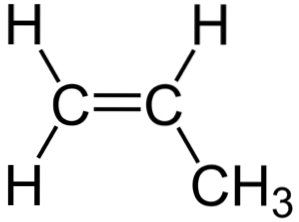
Na górnym zdjęciu widać budowę chemiczną propylenu, w której wyróżnia się jego asymetria (prawa strona różni się od lewej). Jego szkielet węglowy, z wyłączeniem atomów H, można postrzegać jako bumerang.
Ten bumerang ma nienasycenie lub podwójne wiązanie na jednej ze swoich stron (C1), a zatem jest płaski z powodu hybrydyzacji spdwa atomów węgla.
Jednak druga strona jest zajęta przez grupę metylową (-CH3), którego hybrydyzacją jest sp3 i ma geometrię czworościenną. Zatem widziany z przodu bumerang jest płaski z atomami H wystającymi z niego pod kątem około 109,5º..
W fazie gazowej cząsteczka słabo oddziałuje z innymi poprzez siły dyspersji. Podobnie interakcjom między podwójnymi wiązaniami (π-π) dwóch cząsteczek propylenu zapobiega grupa metylowa.
Powoduje to zmniejszenie jego sił międzycząsteczkowych, co znajduje odzwierciedlenie w jego właściwościach fizycznych. Tylko w bardzo niskich temperaturach propylen może przyjąć solidną strukturę, w której bumerang pozostaje zgrupowany z ich słabymi oddziaływaniami.
Nieruchomości
Jest to bezbarwny gaz o aromatycznym zapachu. Jest transportowany w postaci skroplonego gazu, a wydostając się z pojemników, które go zawierają, to w postaci gazu lub cieczy. W niskich stężeniach tworzy wybuchową i łatwopalną mieszaninę z powietrzem, przy większej gęstości propylenu niż powietrza..
Waga molekularna
42,081 g / mol
Temperatura wrzenia
53,9ºF przy 760 mmHg
48 ºC do 760 mmHg
Temperatura topnienia
301,4 ° F.
185 ºC
Temperatura zapłonu
162ºF
Rozpuszczalność
44,6 ml / 100 ml w wodzie.
1250 ml / 100 ml w etanolu.
524,5 ml / 100 ml w kwasie octowym.
Rozpuszczalność wyrażona jako masa
200 mg / l 25 ºC
Gęstość
0,609 mg / ml w temperaturze -52,6 ° F
0,5139 przy 20º C
Gęstość pary
1,46 przy 32ºF (w stosunku do powietrza wziętego jako odniesienie).
1,49 (powietrze = 1).
1,91 kg / m3 przy 273,15 ºK
Ciśnienie pary
1 mmHg przy -205,4ºF
760 mmHg przy -53,9ºF
8,69 × 103 mmHg przy 25 ºC (wartość ekstrapolowana).
1158 kPa w 25 ° C
15,4 atm przy 37 ºC
Samozapłon
851ºF
455 ºC
Lepkość
83,4 mikropazarów przy 16,7 ° C.
Ciepło spalania
16 692 BTU / funt
10 940 cal / g
Ciepło parowania
104,62 cal / g (w temperaturze wrzenia)
Napięcie powierzchniowe
16,7 dyn / cm w temperaturze 90 ° C
Polimeryzacja
Polimeryzuje w wysokich temperaturach i pod wysokim ciśnieniem w obecności katalizatorów.
Punkt zamarzania
185,25 ° C.
Próg zapachu
10-50 mg / m3 (wykrycie)
100 mg / m3 (uznanie)
Aplikacje
Znajduje zastosowanie w przemyśle petrochemicznym jako paliwo i środek alkilujący. W przemyśle chemicznym jest używany jako surowiec do produkcji i syntezy wielu pochodnych.
Znajduje zastosowanie głównie w produkcji polipropylenu, akrylonitrylu (ACN), tlenku propylenu (PO), alkoholi, kumenu i kwasów akrylowych.
Polipropylen
Polipropylen jest jednym z głównych tworzyw sztucznych stosowanych w elektronice i akcesoriach elektrycznych, artykułach gospodarstwa domowego, kapslach do butelek i walizkach..
Laminat służy do pakowania słodyczy, etykiet, płyt kompaktowych itp., Natomiast z włókien wykonujemy foldery i ubrania..
Akrylonitryl
Polimery i włókna elastomerowe otrzymywane są z akrylonitrylu. Włókna te są wykorzystywane do produkcji różnych form odzieży, np. Swetrów, skarpet i odzieży sportowej. Wykorzystywane są również w wyposażeniu domu, teczkach, tapicerce, poduszkach i kocach..
OXID propylenu
Tlenek propylenu uczestniczy jako składnik w syntezie poliuretanu. Służy do produkcji pianki elastycznej i pianki sztywnej. Pianka elastyczna stosowana jest jako wypełniacz w meblach domowych oraz w przemyśle motoryzacyjnym.
Z drugiej strony sztywna pianka jest używana głównie jako izolacyjny materiał budowlany..
Do produkcji glikolu propylenowego wykorzystuje się również tlenek propylenu. Związek ten jest używany do produkcji nienasyconych żywic poliestrowych oraz jako środek przeciw zamarzaniu..
Dodatkowo do produkcji eteru glikolu propylenowego wykorzystuje się tlenek propylenu. Eter ten znajduje zastosowanie w produkcji farb, ubrań, tuszy, żywic i środków czyszczących.
Do syntezy alkoholu i innych zastosowań
Propylen pozwala na otrzymywanie niektórych alkoholi, w tym izopropanolu, używanego jako rozpuszczalnik w kosmetykach i produktach do pielęgnacji ciała. Ponadto spełnia funkcję środka antyseptycznego.
- Izopropanol jest zaangażowany w produkcję farb, żywic, tuszy i taśm klejących. Znajduje również zastosowanie w przemyśle farmaceutycznym.
- Oksoalkohol 2-etyloheksanol jest stosowany do produkcji ftalanów, plastyfikatorów, materiałów klejących i farb.
- Butanol jest używany do produkcji farb, powłok, żywic, barwników, farmaceutyków i polimerów.
Z drugiej strony kumen jest wytwarzany z połączenia propylenu i benzenu. Kumen jest głównym związkiem do produkcji fenolu i acetonu, używanym w wielu produktach, takich jak poliwęglany, żywice fenolowe, żywice epoksydowe i metakrylan metylu..
Wreszcie kwas akrylowy - kolejny produkt pochodzący z propylenu - jest używany do produkcji estrów akrylowych i żywic do farb, powłok i zastosowań klejących..
Bibliografia
- Michał Osmenda. (26 grudnia 2007). Wznieć we mnie ogień. [Postać]. Pobrane 23 maja 2018 z: commons.wikimedia.org
- Grupa Linde. (2018). Propylen. Pobrane 23 maja 2018 r. Z: linde-gas.com
- Wikipedia. (2018). Propen. Pobrane 23 maja 2018 r. Z: en.wikipedia.org
- PubChem. (2018). Propylen. Pobrane 27 maja 2018 z: pubchem.ncbi.nlm.nih.gov
- Vesovic Velisa. (7 lutego 2011). Propylen. Pobrane 27 maja 2018 z: thermopedia.com
- Jeffrey S. Plotkin. (8 sierpnia 2016). Kwestionariusz propylenu. Pobrane 27 maja 2018 z: acs.org
- ICIS. (6 listopada 2017). Zastosowania propylenu i dane rynkowe. Pobrane 27 maja 2018 r. Z: icis.com


Jeszcze bez komentarzy