
Struktura, właściwości, zastosowania acetonitrylu (C2H3N)
Plik acetonitryl Jest to substancja pochodzenia organicznego złożona wyłącznie z węgla, wodoru i azotu. Ten gatunek chemiczny należy do grupy nitryli, przy czym acetonitryl jest jednym z najprostszych struktur wśród nitryli organicznych..
Nitryle to klasa związków chemicznych, których struktura składa się z grupy cyjankowej (CN-) i łańcuch rodnikowy (-R). Elementy te są reprezentowane przez następujący ogólny wzór: R-C≡N.
Wiadomo, że substancja ta powstaje głównie podczas produkcji innego gatunku zwanego akrylonitrylem (inny prosty nitryl o wzorze cząsteczkowym C3H.3N, który jest używany do wytwarzania produktów w przemyśle tekstylnym) jako ich produkt uboczny.
Ponadto acetonitryl jest uważany za rozpuszczalnik o średniej polarności, dlatego jest stosowany dość regularnie w analizach RP-HPLC (wysokosprawna chromatografia cieczowa z odwróconymi fazami)..
Indeks artykułów
- 1 Struktura
- 2 Właściwości
- 3 Zastosowania
- 4 Ryzyka
- 5 Referencje
Struktura
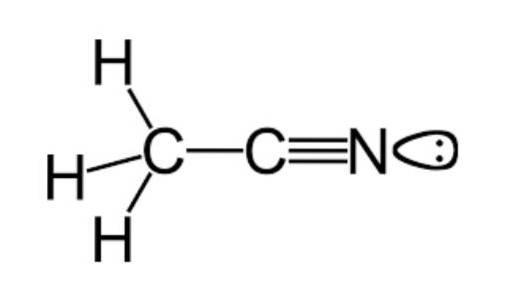
Jak wspomniano wcześniej, acetonitryl należy do grupy funkcyjnej nitryli, której wzór cząsteczkowy jest powszechnie przedstawiany jako CdwaH.3N, co można zobaczyć we wzorze strukturalnym, którego przykład przedstawiono na górnym rysunku.
To zdjęcie przedstawia rodzaj płata przyłączonego do atomu azotu, który reprezentuje parę niesparowanych elektronów, które ma ten atom, i które nadają mu dużą część charakterystycznych dla niego właściwości reaktywności i stabilności..
W ten sposób gatunek ten wykazuje bardzo szczególne zachowanie ze względu na swój układ strukturalny, co przekłada się na słabość do przyjmowania wiązań wodorowych i niewielką zdolność do oddawania elektronów..
Również ta substancja powstała po raz pierwszy w drugiej połowie lat czterdziestych XIX wieku, wytwarzana przez naukowca o nazwisku Jean-Baptiste Dumas, którego narodowość była francuska..
Strukturalna konformacja tej substancji pozwala jej mieć właściwości własnego rozpuszczalnika o charakterze organicznym..
Z kolei ta właściwość pozwala na mieszanie acetonitrylu z wodą, a także szeregiem innych rozpuszczalników pochodzenia organicznego, z wyjątkiem węglowodorów lub węglowodorów typu nasyconego..
Nieruchomości
Ten związek ma szereg właściwości, które odróżniają go od innych z tej samej klasy, które są wymienione poniżej:
- Jest w stanie ciekłym agregacji w normalnych warunkach ciśnienia i temperatury (1 atm i 25 ° C).
- Jego konfiguracja cząsteczkowa daje masę molową lub masę cząsteczkową około 41 g / mol.
- Uważany jest za nitryl o najprostszej strukturze spośród typu organicznego.
- Jego właściwości optyczne sprawiają, że jest bezbarwny w tej fazie ciekłej i ma przejrzyste właściwości, oprócz aromatycznego zapachu..
- Ma temperaturę zapłonu około 2 ° C, co odpowiada 35,6 ° F lub 275,1 K..
- Ma temperaturę wrzenia w zakresie od 81,3 do 82,1 ° C, gęstość około 0,786 g / cm3 i temperatura topnienia, która wynosi od -46 do -44 ° C.
- Jest mniej gęsty niż woda, ale miesza się z nią i różnymi rozpuszczalnikami organicznymi.
- Wykazuje stałą dielektryczną 38,8 oprócz momentu dipolowego około 3,92 D..
- Jest w stanie rozpuszczać wiele różnych substancji pochodzenia jonowego i niepolarnego.
- Jest szeroko stosowany jako faza ruchoma w analizie HPLC, która ma właściwości wysoce łatwopalne.
Aplikacje
Wśród dużej liczby zastosowań acetonitrylu można wymienić:
- Podobnie inne gatunki nitryli mogą ulegać procesowi metabolizacji w mikrosomach (elementach pęcherzykowych wchodzących w skład wątroby), zwłaszcza w tym narządzie, do produkcji kwasu cyjanowodorowego..
- Jest szeroko stosowany jako faza ruchoma w rodzaju analizy zwanej wysokosprawną chromatografią cieczową z odwróconymi fazami (RP-HPLC); to znaczy jako substancja eluująca, która ma wysoką stabilność, dużą moc eluowania i niską lepkość.
- W przypadku zastosowań na skalę przemysłową, ten związek chemiczny jest używany w rafineriach ropy naftowej jako rozpuszczalnik w niektórych procesach, takich jak oczyszczanie alkenu zwanego butadienem..
- Jest również stosowany jako ligand (rodzaj chemiczny, który łączy się z atomem pierwiastka metalicznego, uważanego za centralny w danej cząsteczce, tworząc związek lub kompleks koordynacyjny) w dużej liczbie związków nitrylowych z metalami z grupy przejściowej.
- Podobnie jest stosowany w syntezie organicznej dla wielu tak korzystnych związków chemicznych, jak kwas α-naftalenooctowy, tiamina czy chlorowodorek acetamidyny..
Ryzyka
Ryzyko związane z narażeniem na acetonitryl jest zróżnicowane. Wśród nich jest zmniejszona toksyczność, gdy narażenie trwa przez krótszy okres i jest metabolizowany w małych ilościach do produkcji kwasu cyjanowodorowego..
Podobnie, rzadko odnotowywano przypadki zatrucia tym związkiem chemicznym osób, które zostały zatrute cyjankiem obecnym w cząsteczce po kontakcie z acetonitrylem w różnym stopniu (przy wdychaniu, spożyciu lub wchłonięciu przez skórę)..
Z tego powodu konsekwencje jego toksyczności są opóźnione, ponieważ organizm nie łatwo metabolizuje tę substancję do cyjanku, ponieważ zajmuje to od dwóch do dwunastu godzin..
Jednak acetonitryl jest łatwo wchłaniany z płuc i przewodu pokarmowego. Następnie jego dystrybucja zachodzi w całym organizmie, zachodząc u ludzi, a nawet u zwierząt, docierając do nerek i śledziony..
Z drugiej strony, oprócz ryzyka związanego z palnością, acetonitryl jest prekursorem substancji tak toksycznych jak kwas cyjanowodorowy czy formaldehyd. Jego stosowanie w produktach należących do branży kosmetycznej było nawet zabronione w tzw. Europejskim Obszarze Gospodarczym w 2000 roku..
Bibliografia
- Wikipedia. (s.f.). Acetonitryl. Pobrane z en.wikipedia.org
- PubChem. (s.f.). Acetonitryl. Odzyskany z pubchem.ncbi.nlm.nih.gov
- Brown, P. R. (2000). Postępy w chromatografii. Uzyskane z books.google.co.ve
- ScienceDirect. (s.f.). Acetonitryl. Odzyskany z sciencedirect.com
- ChemSpider. (s.f.). Acetonitryl. Pobrane z chemspider.com



Jeszcze bez komentarzy