
Charakterystyka, budowa, zastosowanie kwasu hipobromawego

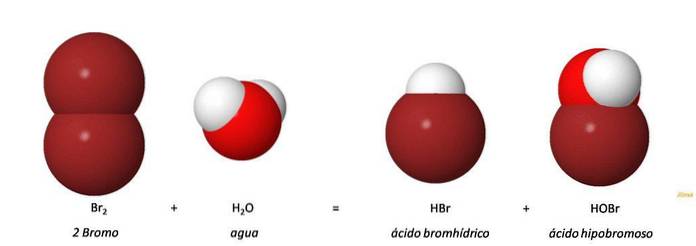
Plik kwas podbromawy (HOBr, HBrO) to nieorganiczny kwas powstający w wyniku utleniania anionu bromkowego (Br-). Dodatek bromu do wody prowadzi do powstania kwasu bromowodorowego (HBr) i kwasu podbromawego (HOBr) w wyniku reakcji dysproporcjonowania. Br2 + H2O = HOBr + HBr
Kwas hipobromawy to bardzo słaby kwas, nieco niestabilny, występujący w postaci rozcieńczonego roztworu w temperaturze pokojowej. Jest wytwarzany przez stałocieplne kręgowce (w tym ludzi) w wyniku działania enzymu peroksydazy eozynofili.
Odkrycie, że kwas podbromowy może regulować aktywność kolagenu IV, przyciągnęło wiele uwagi..
Indeks artykułów
- 1 Struktura
- 1.1 2D
- 1.2 3D
- 2 Właściwości fizyczne i chemiczne
- 3 Zastosowania
- 4 Oddziaływania biomolekularne
- 5 Referencje
Struktura
2D
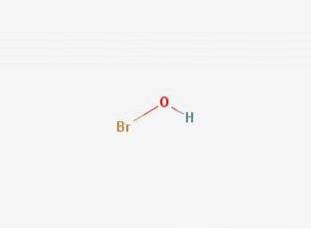
3D

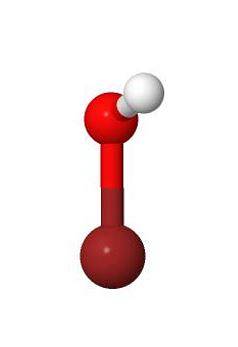
Fizyczne i chemiczne właściwości
- Wygląd Żółte ciało stałe: żółte ciało stałe.
- Wygląd: żółte ciało stałe.
- Masa cząsteczkowa: 96,911 g / mol.
- Temperatura wrzenia: 20-25 ° C.
- Gęstość: 2,470 g / cm3.
- Kwasowość (pKa): 8,65.
- Właściwości chemiczne i fizyczne kwasu podbromawego są podobne do innych podhalitów..
- Występuje jako rozcieńczony roztwór w temperaturze pokojowej.
- Substancje stałe hipobromitu są koloru żółtego i mają specyficzny aromatyczny zapach.
- Jest silnym środkiem bakteriobójczym i dezynfekującym wodę.
- Ma pKa 8,65 i częściowo dysocjuje w wodzie przy pH 7.
Aplikacje
- Kwas hipobromawy (HOBr) jest stosowany jako środek wybielający, utleniacz, dezodorant i środek dezynfekujący, ze względu na jego zdolność do zabijania komórek wielu patogenów.
- Jest stosowany w przemyśle tekstylnym jako środek wybielający i suszący.
- Stosowany również w wannach z hydromasażem i spa jako środek bakteriobójczy.
Oddziaływania biomolekularne
Brom jest wszechobecny u zwierząt jako bromek jonowy (Br-), ale do niedawna jego podstawowa funkcja była nieznana..
Ostatnie badania wykazały, że brom jest niezbędny dla architektury błony podstawnej i rozwoju tkanek.
Enzym peroksydaina wykorzystuje HOBr do sieciowania sulfiliminy, która jest usieciowana w rusztowaniach kolagenu IV błony podstawnej..
Kwas hipobromawy jest wytwarzany w organizmach stałocieplnych kręgowców w wyniku działania enzymu peroksydazy eozynofili (EPO).
EPO generuje HOBr z H2O2 i Br- w obecności stężenia Cl w osoczu-.
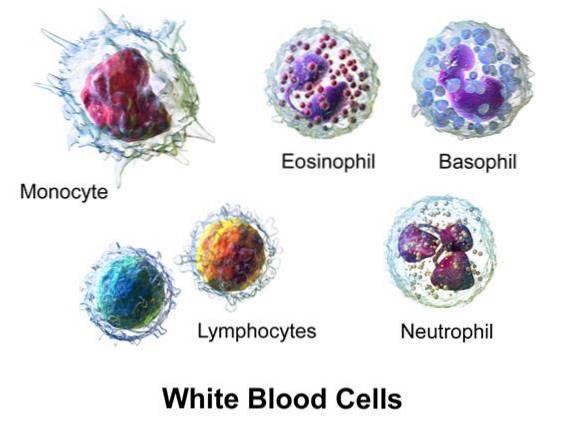
Mieloperoksydaza (MPO) z monocytów i neutrofili wytwarza kwas podchlorawy (HOCl) z H2O2 i Cl-.
EPO i MPO odgrywają ważną rolę w mechanizmach obronnych gospodarza przed patogenami, wykorzystując odpowiednio HOBr i HOCl.
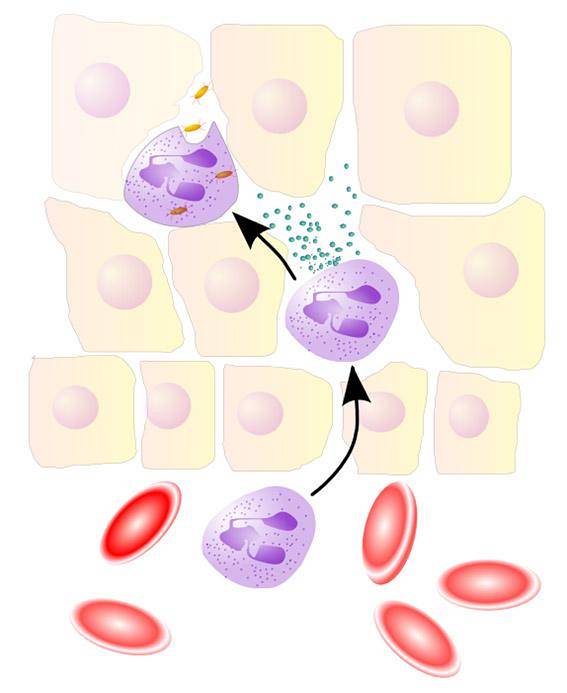
Układ MPO / H2O2 / Cl- w obecności Br- również generuje HOBr w reakcji utworzonego HOCl z Br-. HOBr jest czymś więcej niż silnym utleniaczem, ale także silnym elektrofilem.
Stężenie Br- w osoczu jest ponad 1000 razy niższe niż anionu chlorkowego (Cl-). W konsekwencji endogenna produkcja HOBr jest również niższa w porównaniu z HOCl.
Jednak HOBr jest znacznie bardziej reaktywny niż HOCl, gdy utlenianie badanych związków nie ma znaczenia, więc reaktywność HOBr może być bardziej związana z jego siłą elektrofilową niż z jego mocą utleniającą (Ximenes, Morgon & de Souza, 2015).
Chociaż jego potencjał redoks jest niższy niż HOCl, HOBr reaguje z aminokwasami szybciej niż HOCl.
Halogenowanie pierścienia tyrozynowego przez HOBr jest 5000 razy szybsze niż HOCl.
HOBr reaguje również z nukleozydowymi zasadami nukleotydowymi i DNA.
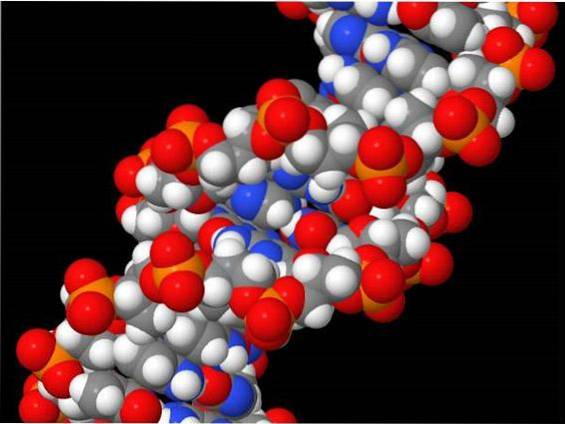
2'-deoksycytydyna, adenina i guanina, generują 5-bromo-2'-deoksycytydynę, 8-bromoadeninę i 8-bromoguaninę w układach EPO / H2O2 / Br- i MPO / H2O2 / Cl- / Br- (Suzuki, Kitabatake i Koide 2016).
McCall i in. (2014) wykazali, że Br jest niezbędnym kofaktorem do tworzenia wiązań krzyżowych sulfiloiminowych katalizowanych przez enzym peroksydazynę, modyfikację potranslacyjną niezbędną dla architektury kolagenu IV błon podstawnych i rozwoju tkanek..
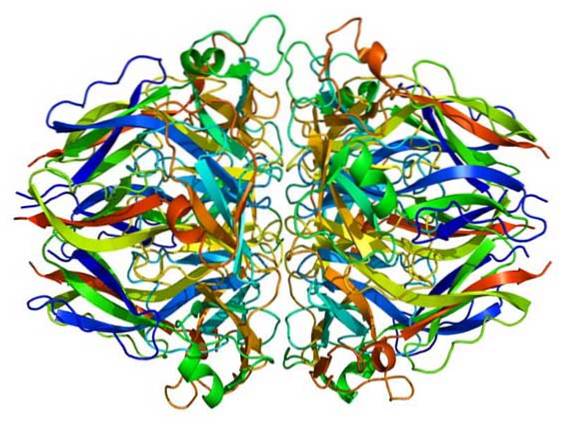
Błony podstawne to wyspecjalizowane macierze zewnątrzkomórkowe, które są kluczowymi mediatorami transdukcji sygnału i mechanicznego wsparcia komórek nabłonka..
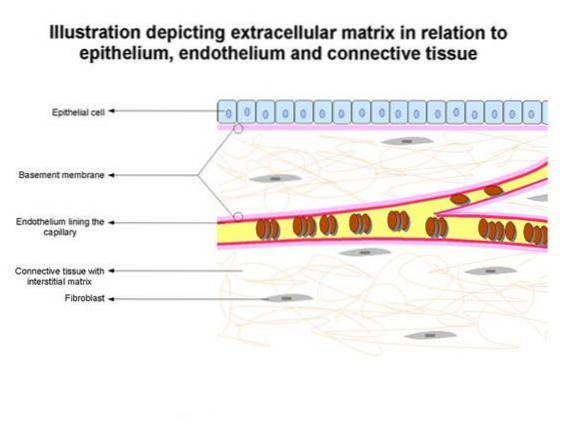
Błony podstawne określają architekturę tkanki nabłonkowej i między innymi ułatwiają naprawę tkanki po urazie..
W błonie podstawnej osadzone jest rusztowanie z kolagenu IV usieciowane sulfiloiminą, które zapewnia funkcjonalność macierzy w tkankach wielokomórkowych wszystkich zwierząt..
Rusztowania z kolagenu IV zapewniają wytrzymałość mechaniczną, służą jako ligand dla integryn i innych receptorów na powierzchni komórki oraz oddziałują z czynnikami wzrostu w celu ustalenia gradientów sygnalizacji..
Sulfilimina (sulfimid) to związek chemiczny zawierający podwójne wiązanie siarki z azotem. Wiązania sulfiloiminowe stabilizują nici kolagenu IV znajdujące się w macierzy zewnątrzkomórkowej.
Te wiązania kowalencyjnie łączą reszty metioniny 93 (Met93) i hydroksylizyny 211 (Hyl211) sąsiednich nici polipeptydowych, tworząc większy trimer kolagenu..
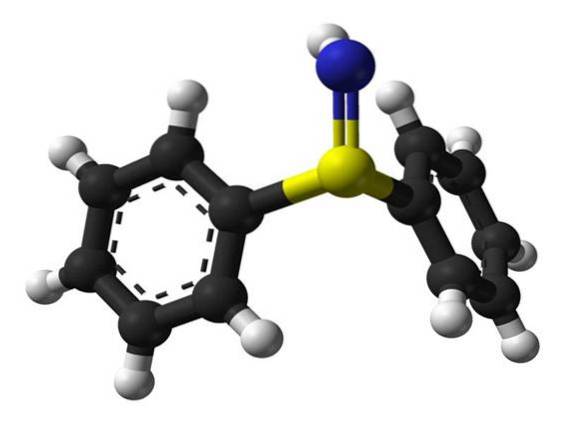
Peroksydaina tworzy kwas podbromawy (HOBr) i kwas podchlorawy (HOCl) odpowiednio z bromku i chlorku, które mogą pośredniczyć w tworzeniu wiązań sieciujących sulfiloiminowych..
Bromek, przekształcony w kwas podbromowy, tworzy związek pośredni jonu bromosulfoniowego (S-Br), który bierze udział w tworzeniu wiązań poprzecznych.
McCall i in. (2014) wykazali, że niedobór Br w diecie jest śmiertelny dla muchy Drosophila, podczas gdy zamiennik Br przywraca jej żywotność.
Ustalili również, że brom jest niezbędnym pierwiastkiem śladowym dla wszystkich zwierząt ze względu na jego rolę w tworzeniu wiązań sulfiloiminowych i kolagenu IV, który ma kluczowe znaczenie dla tworzenia błon podstawnych i rozwoju tkanek..
Bibliografia
- ChemIDplus (2017). Struktura 3D 13517-11-8 - kwas hipobromawy [obraz] Pobrane z nih.gov.
- ChemIDplus (2017). Struktura 3D 60-18-4 - tyrozyna [USAN: INN] [image] Pobrano z nih.gov.
- ChemIDplus (2017). Struktura 3D 7726-95-6 - Brom [obraz] Pobrano z nih.gov.
- ChemIDplus (2017). Struktura 3D 7732-18-5 - Woda [zdjęcie] Odzyskane z nih.gov.
- Emw, (2009). Białko COL4A1 PDB 1li1 [obraz] Odzyskane z wikipedia.org.
- Mills, B. (2009). Diphenylsulfimide-from-xtal-2002-3D-balls [image] Odzyskane z wikipedia.org.
- PubChem (2016). Kwas hipobromawy [obraz] Źródło z nih.gov.
- Steane, R. (2014). Cząsteczka DNA - obrotowa w 3 wymiarach [zdjęcie] Odzyskane z biotopics.co.uk
- Thormann, U. (2005). NeutrophilerAktion [obraz] Odzyskany z wikipedia.org.



Jeszcze bez komentarzy