
Formuła kwasu propanowego, właściwości, zagrożenia i zastosowania

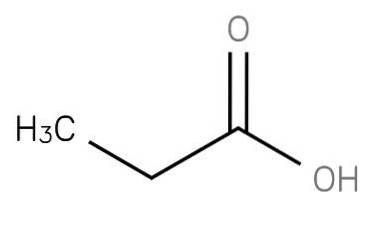
Plik kwas propanowy jest krótkołańcuchowym nasyconym kwasem tłuszczowym zawierającym etan przyłączony do węgla grupy karboksylowej. Jego formuła to CH3-CHdwa-COOH. CH3CH2COO- anion, a także sole i estry kwasu propionowego są znane jako propioniany (lub propioniany).
Można go otrzymać z pozostałości miazgi drzewnej w procesie fermentacji z wykorzystaniem bakterii z rodzaju propionibacterium. Jest również otrzymywany z etanolu i tlenku węgla przy użyciu katalizatora z trifluorku boru (O'Neil, 2001).
Innym sposobem otrzymywania kwasu propionowego jest utlenianie aldehydu propionowego w obecności jonów kobaltu lub manganu. Ta reakcja przebiega szybko w temperaturach tak niskich jak 40-50 ° C:
2CH3CHdwaCHO + Odwa → 2CH3CHdwaCOOH
Związek występuje naturalnie w niewielkich ilościach w produktach mlecznych i generalnie jest wytwarzany wraz z innymi krótkołańcuchowymi kwasami tłuszczowymi w przewodzie pokarmowym ludzi i innych ssaków jako produkt końcowy trawienia przez drobnoustroje węglowodanów..
Ma znaczącą aktywność fizjologiczną u zwierząt (Baza danych metabolomu człowieka, 2017).
Indeks artykułów
- 1 Właściwości fizyczne i chemiczne
- 2 Reaktywność i zagrożenia
- 3 Biochemistry
- 4 Zastosowania
- 5 Referencje
Fizyczne i chemiczne właściwości
Kwas propanowy to bezbarwna, oleista ciecz o ostrym, nieprzyjemnym, zjełczałym zapachu. Jego wygląd pokazano na rysunku 2 (National Center for Biotechnology Information, 2017).

Kwas propanowy ma masę cząsteczkową 74,08 g / mol i gęstość 0,992 g / ml. Jego punkty zamarzania i wrzenia wynoszą odpowiednio -20,5 ° C i 141,1 ° C. Kwas propanowy jest słabym kwasem, którego pKa wynosi 4,88.
Związek jest bardzo dobrze rozpuszczalny w wodzie, będąc w stanie rozpuścić 34,97 gramów związku na każde 100 ml rozpuszczalnika. Jest również rozpuszczalny w etanolu, eterze i chloroformie (Royal Society of Chemistry, 2015).
Kwas propanowy ma właściwości fizyczne pośrednie między mniejszymi kwasami karboksylowymi, kwasami mrówkowym i octowym oraz większymi kwasami tłuszczowymi..
Wykazuje ogólne właściwości kwasów karboksylowych i może tworzyć pochodne amidów, estrów, bezwodników i chlorków. Może ulegać alfa-fluorowcowaniu bromem w obecności PBr3 jako katalizatora (reakcja HVZ), tworząc CH3CHBrCOOH.
Reaktywność i zagrożenia
Kwas propanowy jest materiałem łatwopalnym i palnym. Może się zapalić od ciepła, iskier lub płomieni. Opary mogą tworzyć z powietrzem mieszaniny wybuchowe, mogą przemieszczać się do źródła zapłonu i eksplodować.
Większość oparów jest cięższa od powietrza. Będą rozrzucane po ziemi i zbierane w niskich lub zamkniętych obszarach (kanały ściekowe, piwnice, zbiorniki). Zagrożenie wybuchem oparów w pomieszczeniach, na zewnątrz lub w kanałach.
Substancje oznaczone (P) mogą polimeryzować wybuchowo po podgrzaniu lub w ogniu. Pojemniki mogą eksplodować po podgrzaniu (KWAS PROPIONOWY, 2016).
Związek należy trzymać z dala od ciepła lub źródeł zapłonu. Po podgrzaniu w celu rozkładu wydziela gryzący dym i drażniące opary.
Kwas propanowy działa drażniąco na skórę, oczy, nos i gardło, ale nie wywołuje ostrych skutków ogólnoustrojowych i nie ma widocznego potencjału genotoksycznego. W przypadku kontaktu zmyć dużą ilością wody (Karta Charakterystyki Kwas propionowy, 2013).
Biochemia
Sprzężona zasada kwasu propionowego, propionian, powstaje jako końcowy fragment trójwęglowy (aktywowany koenzymem A jako propionylo-CoA) podczas utleniania nieparzystych węglowych kwasów tłuszczowych i utleniania łańcuchów bocznych cholesterolu.
Eksperymenty z radioaktywnymi izotopami propionianu wstrzykiwanymi głodzonym szczurom wskazują, że może on występować w glikogenie, glukozie, związkach pośrednich cyklu kwasu cytrynowego, aminokwasach i białkach..
Szlak metabolizmu kwasu propanowego obejmuje interakcję z koenzymem A, karboksylację w celu utworzenia metylomalonylo-koenzymu A i konwersję do kwasu bursztynowego, który wchodzi w cykl kwasu cytrynowego.
Kwas propanowy można utleniać bez tworzenia ciał ketonowych i, w przeciwieństwie do kwasu octowego, jest włączany zarówno do węglowodanów, jak i lipidów (Bingham, Cohrssen i Powell, 2001).
Kwasuria propionowa jest jedną z najczęstszych kwasicy organicznej, choroby obejmującej wiele różnych zaburzeń.
Wyniki pacjentów urodzonych z kwasicą propionową są słabe pod względem wzorców rozwoju intelektualnego, przy czym 60% ma IQ poniżej 75 i wymaga specjalnego wykształcenia.
Pomyślne przeszczepienie wątroby i / lub nerki u kilku pacjentów spowodowało poprawę jakości życia, ale niekoniecznie zapobiegło powikłaniom trzewnym i neurologicznym.
Wyniki te podkreślają potrzebę stałego monitorowania metabolizmu, niezależnie od strategii terapeutycznej..
Aplikacje
Kwas propanowy hamuje rozwój bakterii i pleśni na poziomie od 0,1 do 1% wagowo. W rezultacie większość wyprodukowanego kwasu propanowego jest spożywana jako środek konserwujący zarówno paszę, jak i żywność przeznaczoną do spożycia przez ludzi, taką jak zboża i zboża..
Konserwacja pasz, zbóż i żywności oprócz produkcji propionianów wapnia i sodu, co stanowi prawie 80% światowego spożycia kwasu propanowego w 2016 r. W porównaniu z 78,5% w 2012 r..
Około 51% światowego spożycia kwasu propanowego przeznacza się na paszę dla zwierząt i konserwację ziarna, a prawie 29% wykorzystuje się do produkcji propionianów wapnia i sodu, które są również wykorzystywane w przemyśle spożywczym i paszowym..
Inne ważne rynki zbytu kwasu propanowego to produkcja herbicydów i ketonu dietylowego. Zastosowania o mniejszej objętości obejmują wytwarzanie propionianu octanu celulozy, farmaceutyków, estrów rozpuszczalników, aromatów i substancji zapachowych, plastyfikatorów, barwników do tekstyliów, skóry i gumy oraz środków pomocniczych.
Popyt na kwas propanowy jest silnie uzależniony od produkcji paszy i zbóż, a następnie żywności pakowanej i pieczywa.
Perspektywy globalnego wzrostu kwasu propanowego i jego soli w paszach dla zwierząt / zbożach i konserwowaniu żywności są znaczące (IHS Markit, 2016).
Inne szybko rozwijające się rynki obejmują estry propionianowe do rozpuszczalników, takie jak propionian n-butylu i pentylu; Estry te są coraz częściej stosowane jako substytuty rozpuszczalników wymienionych jako niebezpieczne zanieczyszczenia powietrza..
Bibliografia
- Bingham, E., Cohrssen, B., & Powell, C. (2001). Patty's Toxicology Tomy 1-9 5th ed. Nowy Jork: John Wiley & Sons.
- EMBL-EBI. (14 października 2016). kwas propionowy. Odzyskany z ChEBI: ebi.ac.uk.
- Baza danych metabolomów człowieka. (2017, 2 marca). Kwas propionowy. Odzyskany z hmdb.ca: hmdb.ca.
- IHS Markit. (2016, grudzień). Podręcznik ekonomii chemicznej Kwas propionowy. Odzyskany z ihs: ihs.com.
- Karta charakterystyki materiału Kwas propionowy. (2013, 21 maja). Odzyskany z sciencelab: sciencelab.com.
- National Center for Biotechnology Information… (22 kwietnia 2017). Baza danych PubChem Compound; CID = 1032. Odzyskany z pubchem.ncbi.nlm.nih.gov.
- O'Neil, M. (. (2001). The Merck Index - An Encyclopedia of Chemicals, Drugs, and Biologicals. 13th Edition. New Jersey: Merck and Co., Inc.
- KWAS PROPIONOWY. (2016). Odzyskany z cameochemicals: cameochemicals.noaa.gov.
- Królewskie Towarzystwo Chemii. (2015). Kwas propionowy. Odzyskany z chemspider: chemspider.com.


Jeszcze bez komentarzy