
Współstrącanie, z czego się składa, rodzaje i zastosowania

Plik współstrącanie Jest to zanieczyszczenie nierozpuszczalną substancją, która przenosi rozpuszczone substancje rozpuszczone z ciekłego ośrodka. Tutaj słowo „zanieczyszczenie” jest stosowane w tych przypadkach, w których rozpuszczalne substancje rozpuszczone wytrącane przez nierozpuszczalny nośnik są niepożądane; ale jeśli tak nie jest, dostępna jest alternatywna metoda analityczna lub syntetyczna.
Z drugiej strony nierozpuszczalnym nośnikiem jest wytrącona substancja. Może to przenosić rozpuszczalną substancję rozpuszczoną do środka (absorpcja) lub na jej powierzchni (adsorpcja). Sposób, w jaki to zrobisz, całkowicie zmieni właściwości fizykochemiczne powstałej substancji stałej..
Chociaż koncepcja współstrącania może wydawać się nieco zagmatwana, występuje częściej, niż mogłoby się wydawać. Dlaczego? Ponieważ powstają nie tylko zwykłe zanieczyszczone ciała stałe, ale także stałe roztwory o złożonych strukturach i bogate w nieocenione składniki. Gleba, z której odżywia się rośliny, jest przykładem współstrącania.
Podobnie, minerały, ceramika, gliny i zanieczyszczenia w lodzie są również produktem tego zjawiska. W przeciwnym razie gleby straciłyby dużą część swoich niezbędnych pierwiastków, minerały nie byłyby takie, jakie są obecnie znane i nie byłoby ważnej metody syntezy nowych materiałów..
Indeks artykułów
- 1 Co to jest współstrącanie?
- 2 rodzaje
- 2.1 Włączenie
- 2.2 Okluzja
- 2.3 Adsorpcja
- 3 Aplikacje
- 4 Odnośniki
Co to jest współstrącanie?
Aby lepiej zrozumieć ideę współstrącania, przedstawiono następujący przykład.
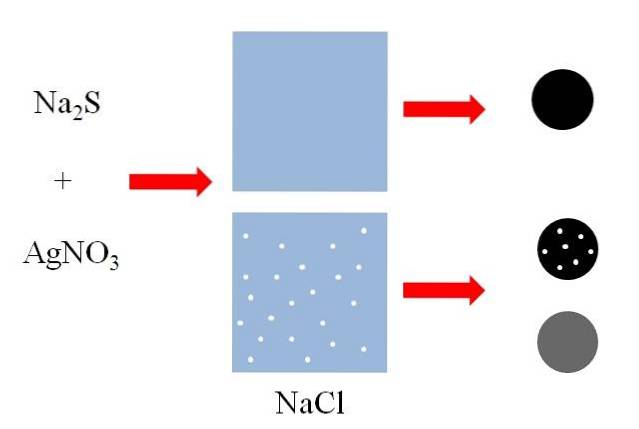
Powyżej (górne zdjęcie) znajdują się dwa pojemniki z wodą, z których jeden zawiera rozpuszczony NaCl. NaCl jest solą dobrze rozpuszczalną w wodzie, ale rozmiary białych kropek są wyolbrzymione w celu wyjaśnienia. Każdy biały punkt stanie się małymi agregatami NaCl w roztworze na granicy nasycenia.
Mieszanina siarczku sodu, NadwaS i azotan srebra AgNO3, wytrąci nierozpuszczalne czarne ciało stałe siarczku srebra, AgS:
NadwaS + AgNO3 => AgS + NaNO3
Jak widać w pierwszym zbiorniku z wodą, wytrąca się czarna substancja stała (czarna kula). Jednak to ciało stałe w pojemniku z rozpuszczonym NaCl niesie cząsteczki tej soli (czarna kula z białymi kropkami). NaCl jest rozpuszczalny w wodzie, ale kiedy wytrąca się AgS, jest adsorbowany na czarnej powierzchni.
Następnie mówi się, że NaCl współstrącał na AgS. Jeśli analizowano czarne ciało stałe, na powierzchni można było zobaczyć mikrokryształy NaCl.
Jednak te kryształy mogą również znajdować się wewnątrz AgS, więc ciało stałe „zmieniłoby się” w szarawe (biały + czarny = szary).
Rodzaje
Czarna kula z białymi kropkami i szara sfera pokazują, że rozpuszczalna substancja rozpuszczona może współstrącać się na różne sposoby..
W pierwszym robi to powierzchownie, adsorbowany na nierozpuszczalnym nośniku (AgS w poprzednim przykładzie); podczas gdy w drugiej robi to wewnętrznie, „zmieniając” czarny kolor osadu.
Czy możesz dostać inne rodzaje ciał stałych? Czyli kula z fazami czarno-białymi, czyli AgS i NaCl (razem z NaNO3 który również współstrąca). To tutaj rodzi się pomysłowość syntezy nowych ciał stałych i materiałów.
Jednak wracając do punktu wyjścia, zasadniczo rozpuszczalne substancje rozpuszczone współstrącają tworząc różne typy ciał stałych. Rodzaje współstrącania i wynikające z nich ciała stałe zostaną omówione poniżej..
Włączenie
O inkluzji mówimy, gdy w sieci krystalicznej jeden z jonów można zastąpić jednym z współstrąconych substancji rozpuszczalnych.
Na przykład, jeśli NaCl wytrącił się wspólnie przez inkluzję, jony Na+ zająłby miejsce Ag+ w sekcji układu kryształów.
Jednak ze wszystkich typów współstrącania jest to najmniej prawdopodobne; ponieważ aby tak się stało, promienie jonowe muszą być bardzo podobne. Wracając do szarej sfery obrazu, włączenie byłoby reprezentowane przez jeden z jaśniejszych szarawych tonów.
Jak już wspomniano, inkluzja zachodzi w krystalicznych ciałach stałych i aby je otrzymać, trzeba mieć biegłość w chemii roztworów i kilku czynnikach (T, pH, czas mieszania, stosunki molowe itp.).
Okluzja
W przypadku okluzji jony są uwięzione w sieci krystalicznej, ale nie zastępują żadnego jonu w macierzy. Na przykład okludowane kryształy NaCl mogą tworzyć się w AgS. Graficznie można to wizualizować jako biały kryształ otoczony czarnymi kryształami.
Ten rodzaj współstrącania należy do najpowszechniejszych, dzięki czemu zachodzi synteza nowych krystalicznych ciał stałych. Zakleszczonych cząstek nie można usunąć zwykłym praniem. Aby to zrobić, konieczna byłaby rekrystalizacja całego zestawu, czyli nierozpuszczalnego podłoża.
Zarówno inkluzja, jak i okluzja są procesami wchłaniania zachodzącymi w strukturach krystalicznych.
Adsorpcja
Podczas adsorpcji współstrącona substancja stała znajduje się na powierzchni nierozpuszczalnego nośnika. Wielkość cząstek tego nośnika określa rodzaj otrzymanej substancji stałej.
Jeśli są małe, powstanie skoagulowana substancja stała, z której łatwo będzie usunąć zanieczyszczenia; ale jeśli są bardzo małe, ciało stałe wchłonie duże ilości wody i będzie galaretowate.
Wracając do czarnej kuli z białymi kropkami, kryształy NaCl współstrącone na AgS można przemyć wodą destylowaną. Tak dalej, aż AgS zostanie oczyszczony, który można następnie podgrzać, aby odparować całą wodę.
Aplikacje
Jakie są zastosowania współstrącania? Oto niektóre z nich:
-Pozwala na ilościowe określenie rozpuszczalnych substancji, które nie są łatwo wytrącane z medium. Tak więc, poprzez nierozpuszczalny nośnik, przenosi na przykład izotopy promieniotwórcze, takie jak frans, do dalszych badań i analiz..
-Współstrącając jony w galaretowatych ciałach stałych, oczyszczasz płynny ośrodek. W takich przypadkach okluzja jest jeszcze bardziej pożądana, ponieważ nieczystość nie będzie mogła wydostać się na zewnątrz.
-Współstrącanie umożliwia wprowadzenie substancji do ciał stałych podczas ich formowania. Jeśli ciało stałe jest polimerem, będzie absorbować rozpuszczalne substancje rozpuszczone, które następnie będą współstrącać wewnątrz, nadając mu nowe właściwości. Jeśli jest to na przykład celuloza, może w niej współstrącać kobalt (lub inny metal).
-Oprócz wszystkich powyższych, współstrącanie jest jedną z kluczowych metod syntezy nanocząstek na nierozpuszczalnym podłożu. Dzięki temu zsyntetyzowano m.in.bionanomateriały i nanocząsteczki magnetytu..
Bibliografia
- Day, R., & Underwood, A. (1986). Ilościowa chemia analityczna (wyd. piąte). Sala PEARSON Prentice.
- Wikipedia. (2018). Współstrącanie. Odzyskane z: en.wikipedia.org
- NPTEL. (s.f.). Opad i współstrącanie. Odzyskany z: nptel.ac.in
- Wise Geek. (2018). Co to jest Coprecipitation. Odzyskany z: wisegeek.com
- Wilson Sacchi Peternele, Victoria Monge Fuentes, Maria Luiza Fascineli i wsp. (2014). Eksperymentalne badanie metody koprecypitacji: podejście do uzyskiwania nanocząstek magnetytu i maghemitu o ulepszonych właściwościach. Journal of Nanomaterials, vol. 2014, numer artykułu 682985, 10 stron.



Jeszcze bez komentarzy