
Charakterystyka fioletowego kryształu, sposób jego otrzymywania i wykorzystania
Plik Fioletowe szkło to organiczny, syntetyczny i zasadowy barwnik triaminotrifenylometanowy. Występuje jako ciemnozielony metaliczny proszek z połyskiem. Otrzymuje kilka nazw, wśród których możemy wymienić chlorek heksametyloparosaniliny lub fiolet metylowy, fiolet anilinowy, fiolet goryczki itp..
Nazwa fioletowego barwnika krystalicznego została zaczerpnięta od podobieństwa do koloru płatków kwiatów fioletu i goryczki; jego pochodzenie nie ma nic wspólnego z ekstraktami z tych kwiatów.

Fioletowy kryształ uzyskuje się kilkoma drogami, które obejmują między innymi kondensację, addycję, reakcje chlorowania. Wszystkie zawierają jako surowiec N, N-dimetyloanilinę.
Jest stosowany jako składnik tuszów używanych do drukowania i długopisów. Służy również do barwienia m.in. skór, papieru, detergentów, nawozów..
Był szeroko stosowany jako środek antyseptyczny. Posiada właściwości antymitotyczne, przeciwbakteryjne, przeciwpasożytnicze i przeciwgrzybicze. Jego mechanizm działania jest bakteriostatyczny.
Jest stosowany w histologii do barwienia skrawków tkanek oraz w mikrobiologii do barwienia i klasyfikowania bakterii zgodnie z ich właściwościami barwienia metodą Grama..
Indeks artykułów
- 1 Funkcje
- 1.1 Wzór cząsteczkowy
- 1.2 Masa formuły
- 1.3 Temperatura topnienia
- 1.4 Temperatura wrzenia
- 1.5 Gęstość
- 1.6 Rozpuszczalność
- 1,7 Pka
- 1.8 Reaktywność
- 2 Jak otrzymujesz?
- 3 Zastosowania
- 3.1 Składnik atramentu
- 3.2 W przypadku tymczasowego oznakowania skóry
- 3.3 W barwieniu Grama
- 3.4 W leczeniu niektórych chorób
- 3.5 W leczeniu infekcji
- 3.6 W laboratoriach i badaniach biomedycznych
- 4 Odnośniki
Charakterystyka
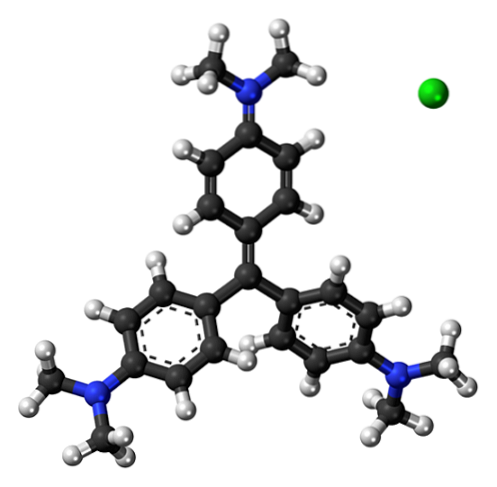
Górny obraz przedstawia strukturę cząsteczki triaminotrifenylometanu. Niebieskie kule odpowiadają atomom azotu, a na górze znajduje się azot z dodatnim ładunkiem formalnym, który przyciąga anion Cl- (zielona kula).
Struktura jest płaska w trzech pierścieniach aromatycznych z powodu hybrydyzacji spdwa jego atomów węgla. Zwróć uwagę, że chociaż górny pierścień jest aromatyczny, nie zawiera on kropkowanych linii w środku. Oznacza to, że rezonans jego podwójnych wiązań nie jest faworyzowany..
Cząsteczka fioletu krystalicznego jest wyraźnie polarna. Dlaczego? Ponieważ trzy elektroujemne atomy azotu oddają swoją parę wolnych elektronów do pierścieni aromatycznych, a część tej gęstości elektronowej jest przyciągana przez częściowo dodatnio naładowany atom azotu (N+). Ta biegunowość jest widoczna w jej wysokiej temperaturze wrzenia, znacznie wyższej niż w przypadku wody..
Formuła molekularna
do25H.30ClN3
Waga formuły
407,99 g / mol
Temperatura topnienia
205 ºC
Temperatura wrzenia
560,86 ° C
Gęstość
1,19 g / cm3 (20ºC)
Rozpuszczalność
Rozpuszczalny w wodzie 50 g / L przy 27ºC.
Fiolet krystaliczny jest nierozpuszczalny w eterze, jest rozpuszczalny w wodzie, chloroformie i alkoholu. Kiedy fioletowy kryształ rozpuści się w wodzie, przybiera kolor niebieski lub fioletowy..
Pka
9,4 w 25ºC
Kolor zmienia się w zależności od kwasowości roztworu, przy pH większym niż 1 barwnik jest zielony, a przy pH niższym niż 1 kolor jest żółty. Ta zmiana koloru odzwierciedla różne zmiany ładunku cząsteczki..
Reaktywność
Jest wrażliwy na światło, niekompatybilny między innymi z kwasami i silnymi utleniaczami.
Jak to się uzyskuje?
Fioletowy kryształ został pozyskany różnymi drogami. Został po raz pierwszy przygotowany przez Caro i Kern, dwóch niemieckich chemików, którzy przereagowali dimetyloanilinę z fosgenem..
W wyniku tej reakcji otrzymano produkt pośredni, 4,4'-bis (dimetyloamino) benzofenon, znany również jako keton Michlera. Ten keton poddano następnie reakcji z większą ilością dimetyloaniliny z tlenochlorkiem fosforu i kwasem solnym..
Zmieszany odczynnik jodu z chlorkiem fioletu krystalicznego nazywany jest fioletem goryczki. Innym sposobem przygotowania fioletu krystalicznego jest reakcja kondensacji dimetyloaminy i formaldehydu, w wyniku której powstaje biały barwnik..
W zależności od warunków pH, światła lub ciepła, ten biały barwnik może podlegać odwracalnym przemianom, które oscylują między dwoma kolorami, przechodząc przez bezbarwną.
Aplikacje
Składnik farb
Fiolet goryczki można stosować w tuszach, którymi barwi się różnorodne materiały, takie jak drewno, skóra, jedwab czy papier. Znajduje zastosowanie w farbach, nawozach, detergentach, czynnikach chłodniczych.
Znajduje zastosowanie w tuszach drukarskich, czarnych i granatowych tuszach do długopisów. Opisano również jego zastosowanie w farbach do włosów.
W przypadku tymczasowego przebarwienia skóry
Służy do znakowania skóry, wytyczając obszar do wykonywania zabiegów na ciele. Służy również do oznaczenia miejsca na skórze, w którym zostanie umieszczony piercing, i jest przydatny jako marker w testach alergicznych..
W barwieniu Grama
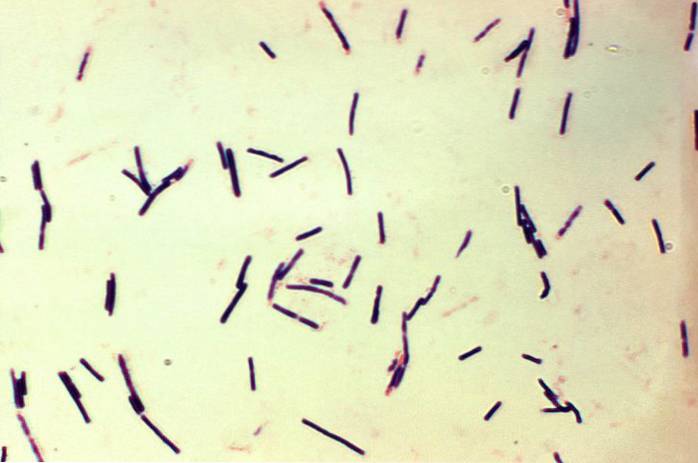
Fiolet krystaliczny jest jednym ze składników metody barwienia Grama. Pozwala to zaklasyfikować bakterie jako bakterie Gram-dodatnie lub Gram-ujemne. Niektóre z nich nie są jednak zabarwione Gramem.
Zastosowanie fioletowego kryształu polega na jego penetracji przez grubą ścianę komórkową bakterii. W ten sposób jego struktura komórkowa zatrzymuje barwnik, zabarwiając bakterie na fioletowo. Tak jest w przypadku bakterii Gram-dodatnich.
Natomiast jeśli bakterie mają cienką ścianę komórkową, klasyfikuje się je jako bakterie Gram-ujemne. Z tego powodu barwnik nie może pozostać w nich wystarczająco długo, aby je zabarwić (cząsteczka triamino-trifenylometanu łatwo wchodzi i wychodzi).
Następnie, w procesie barwienia kontrastowego prowadzonego tą samą metodą Grama, bakterie barwi się fenicada fuscin, pozostawiając je na różowo..
Kiedy bakterie nie mają ściany komórkowej i nie wykazują żadnego rodzaju zabarwienia, klasyfikuje się je jako bakterie, które nie wybarwiają się metodą Grama.
Jako lekarstwo w niektórych chorobach
-Fiolet krystaliczny był bardzo często stosowany jako środek odkażający na rany skóry i błon śluzowych (miejscowo lub zewnętrznie), a także w leczeniu różnych schorzeń, np. Atopowego zapalenia skóry..
-Opisano jego przydatność w leczeniu hemoroidów.
-Posiada właściwości przeciwnowotworowe.
-Był stosowany w chorobach neurodegeneracyjnych, w szpiczaku mnogim i raku piersi.
W leczeniu infekcji
-Fiolet krystaliczny ma właściwości pomagające zabijać różnego rodzaju mikroorganizmy. Wśród nich są grzyby; to znaczy jest przeciwgrzybiczy.
-Stosowany jest w leczeniu kandydozy jamy ustnej, likwidacji stopy atlety, grzybicy paznokci (grzybica paznokci), między innymi przy zakażeniach grzybiczych.
-Jest stosowany w leczeniu niektórych infekcji wywołanych przez bakterie, takie jak liszajec, który jest bardzo przydatny szczególnie dla osób uczulonych na niektóre antybiotyki, takie jak penicylina.
-Działa również przeciwpasożytniczo. Służy do eliminacji pasożytów robaków pasożytniczych (przeciwrobaczych) i jest skuteczny przeciwko pierwotniakom trypanosomalnym.
-Jest bardzo przydatny w leczeniu infekcji oczu i skóry u zwierząt, takich jak bydło, a nawet ryby. Stwierdzono, że w barwniku fioletu krystalicznego dominuje działanie bakteriostatyczne.
W laboratoriach i badaniach biomedycznych
-Fiolet krystaliczny jest używany w laboratoriach jako wskaźnik kwasowo-zasadowy, zmieniając swój kolor od zielonego przy pH 0,5 do niebieskiego przy pH 2. Może być stosowany do oznaczania jonów metali, takich jak cynk, kadm, złoto, rtęć., między innymi jony.
-Fiolet krystaliczny jest nietoksyczną alternatywą, stosowaną zamiast barwnika fluorescencyjnego bromku etydyny w przebiegach elektroforetycznych w żelu DNA..
-Fiolet krystaliczny i formalina są bardzo przydatne do barwienia i utrwalania komórek uzyskanych w pożywkach hodowlanych, ułatwiając ich widoczność..
Bibliografia
- Wikipedia. (2018). Krystaliczny fiolet. Odzyskane z: en.wikipedia.org
- Książka chemiczna. (2017). Krystaliczny fiolet. Odzyskane z: chemicalbook.com
- PubChem. (2018). Fiołek goryczki. Odzyskany z: pubchem.ncbi.nlm.nih.gov
- Monica Z. Bruckner. (3 listopada 2016). Gramowanie. Odzyskany z: serc.carleton.edu
- DrugBank. (2018). Fiołek goryczki. Odzyskany z: drugbank.ca

Jeszcze bez komentarzy