
Krzywa grzewcza co to jest, jak to się robi, przykłady
ZA krzywa grzania jest graficzną reprezentacją tego, jak zmienia się temperatura próbki w funkcji czasu, utrzymując ciśnienie na stałym poziomie i równomiernie dodając ciepło, to znaczy ze stałą szybkością.
Aby skonstruować wykres tego typu, pobierane są pary wartości temperatury i czasu, które są następnie wykreślane poprzez umieszczenie temperatury na osi pionowej (rzędnej), a czasu na osi poziomej (odciętych).

Następnie do tych punktów doświadczalnych dopasowuje się najbardziej odpowiednią krzywą i ostatecznie uzyskuje się wykres temperatury T w funkcji czasu t: T (t).
Indeks artykułów
- 1 Jaka jest krzywa grzania?
- 1.1 -Zmiana stanu substancji
- 2 Jak wykonać krzywą grzewczą?
- 3 przykłady (woda, żelazo ...)
- 3.1 Topienie lodu
- 3.2 Zamiana wody w parę
- 4 Odnośniki
Jaka jest krzywa grzewcza?
Substancja podczas podgrzewania przechodzi kolejno przez różne stany: z ciała stałego może stać się parą, prawie zawsze przechodząc przez stan ciekły. Procesy te nazywane są zmianami stanu, w których próbka zwiększa swoją energię wewnętrzną podczas dodawania ciepła, na co wskazuje teoria kinetyki molekularnej..
Podczas dodawania ciepła do próbki istnieją dwie możliwości:
- Substancja podnosi swoją temperaturę, ponieważ jej cząsteczki są mieszane z większą intensywnością.
- Materiał przechodzi przemianę fazową, w której temperatura pozostaje stała. Dodanie ciepła osłabia w pewnym stopniu siły, które trzymają cząstki razem, więc łatwo jest przejść na przykład z lodu do wody w stanie ciekłym..
Rysunek 2 przedstawia cztery stany skupienia materii: stały, ciekły, gaz i plazmę oraz nazwy procesów, które umożliwiają przejście między nimi. Strzałki wskazują kierunek procesu.
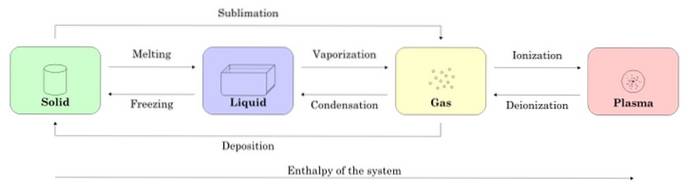
-Zmiany stanu substancji
Zaczynając od próbki w stanie stałym, po stopieniu przechodzi w stan ciekły, po odparowaniu zamienia się w gaz i poprzez jonizację zamienia się w plazmę.
Ciało stałe można przekształcić bezpośrednio w gaz w procesie znanym jako sublimacja. Istnieją substancje, które łatwo sublimują w temperaturze pokojowej. Najbardziej znanym jest COdwa lub suchy lód, a także naftalen i jod.
Podczas gdy próbka ulega zmianie stanu, temperatura pozostaje stała aż do osiągnięcia nowego stanu. Oznacza to, że jeśli na przykład masz porcję wody w stanie ciekłym, która osiągnęła punkt wrzenia, jej temperatura pozostaje stała, dopóki cała woda nie zamieni się w parę..
Z tego powodu oczekuje się, że krzywa ocieplenia będzie złożona z kombinacji rosnących sekcji i odcinków poziomych, przy czym te ostatnie odpowiadają przemianom fazowym. Rysunek 3 przedstawia jedną z tych krzywych dla danej substancji.
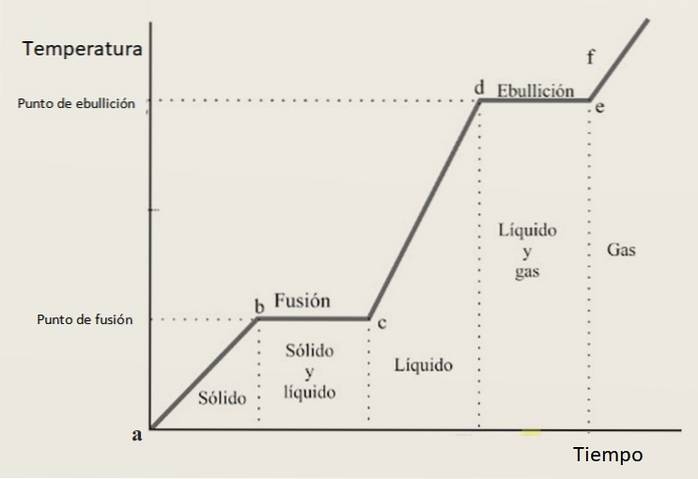
Interpretacja krzywej grzewczej
W okresach wzrostu ab, Płyta CD Y ef substancja występuje odpowiednio w postaci ciała stałego, cieczy i gazu. W tych regionach wzrasta energia kinetyczna, a wraz z nią temperatura.
Tymczasem w pne zmienia swój stan ze stałego na ciekły, dlatego te dwie fazy współistnieją. Tak to się dzieje w sekcji z, w którym próbka zmienia się z cieczy w gaz. Tutaj energia potencjalna się zmienia, a temperatura pozostaje stała.
Możliwa jest również procedura odwrotna, to znaczy próbkę można schłodzić, aby sukcesywnie przyjmować inne stany. W takim przypadku mówimy krzywa chłodzenia.
Krzywe grzewcze mają ten sam ogólny wygląd dla wszystkich substancji, chociaż oczywiście nie mają takich samych wartości liczbowych. Niektórym substancjom potrzeba więcej czasu niż innym, aby zmienić stan i topią się i odparowują w różnych temperaturach..
Punkty te nazywane są odpowiednio temperaturą topnienia i temperaturą wrzenia i stanowią charakterystykę każdej substancji..
Dlatego krzywe grzewcze są bardzo przydatne, ponieważ wskazują wartości liczbowe tych temperatur dla milionów substancji, które istnieją jako ciała stałe i ciecze w zakresie temperatur uznawanych za normalne i przy ciśnieniu atmosferycznym..
Jak zrobić krzywą rozgrzewki?
W zasadzie jest to bardzo proste: wystarczy umieścić próbkę substancji w pojemniku wyposażonym w mieszadło, włożyć termometr i równomiernie podgrzać..
Jednocześnie podczas uruchamiania procedury włączany jest stoper i od czasu do czasu zapisywane są odpowiednie pary temperatura-czas..
Źródłem ciepła może być palnik gazowy o dobrej szybkości ogrzewania lub opór elektryczny, który po podgrzaniu emituje ciepło, który można podłączyć do zmiennego źródła w celu uzyskania różnych mocy..
Aby uzyskać większą precyzję, w laboratorium chemicznym szeroko stosowane są dwie techniki:
- Różnicowa analiza termiczna.
- Różnicowa kalorymetria skaningowa.
Porównują różnicę temperatur między badaną próbką a inną próbką odniesienia o wysokiej temperaturze topnienia, prawie zawsze tlenku glinu. Tymi metodami łatwo jest określić temperaturę topnienia i wrzenia.
Przykłady (woda, żelazo ...)
Weź pod uwagę krzywe grzewcze dla wody i żelaza pokazane na rysunku. Skala czasu nie jest pokazana, jednak natychmiast można rozróżnić temperatury topnienia obu substancji, które odpowiadają punktowi B każdego wykresu: dla wody 0 º C, dla żelaza 1500 º C.
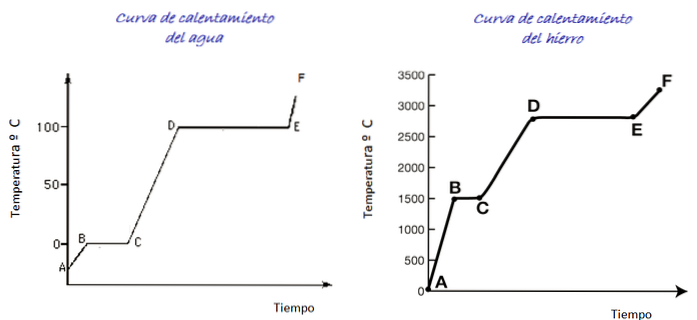
Woda jest substancją uniwersalną, a zakres temperatur niezbędny do zaobserwowania zmian jej stanu jest łatwy do osiągnięcia w laboratorium. Żelazo wymaga znacznie wyższych temperatur, ale jak wspomniano powyżej, kształt wykresu nie zmienia się zasadniczo..
Topniejący lód
Podczas ogrzewania próbki lodu zgodnie z wykresem znajdujemy się w punkcie A, w temperaturze poniżej 0º C. Obserwuje się, że temperatura rośnie ze stałą szybkością, aż do osiągnięcia 0º C.
Cząsteczki wody w lodzie wibrują z większą amplitudą. Po osiągnięciu temperatury topnienia (punkt B) cząsteczki mogą już poruszać się przed sobą.
Energia, która przybywa, jest inwestowana w zmniejszenie siły przyciągania między cząsteczkami, więc temperatura między B i C pozostaje stała, dopóki cały lód nie stopi się..
Zamiana wody w parę
Gdy woda jest całkowicie w stanie ciekłym, wibracje cząsteczek ponownie rosną, a temperatura gwałtownie rośnie między C i D, aż do temperatury wrzenia 100º C. Pomiędzy D i E temperatura pozostaje na tej wartości, podczas gdy energia, która dociera zapewnia, że cała woda z pojemnika odparuje.
Jeśli cała para wodna może być zawarta w zbiorniku, może on kontynuować ogrzewanie od punktu E do punktu F, którego granica nie jest pokazana na wykresie..
Próbka żelaza może podlegać tym samym zmianom. Jednak biorąc pod uwagę rodzaj materiału, zakresy temperatur są bardzo różne..
Bibliografia
- Atkins, P. Principles of Chemistry: The Paths of Discovery. Od redakcji Médica Panamericana. 219-221.
- Chung, P. Krzywe grzewcze. Źródło: chem.libretexts.org.
- Krzywe grzewcze. Ciepło topnienia i parowania. Odzyskany z: wikipremed.com.
- Hewitt, Paul. 2012. Konceptualne nauki fizyczne. 5. Ed Pearson. 174-180.
- Uniwersytet w Valladolid. Dyplom z chemii, odzyskany z: Lodging.uva.es.



Jeszcze bez komentarzy