
Charakterystyka i typy wiązań estrowych

ZA wiązanie estrowe definiuje się jako wiązanie między grupą alkoholową (-OH) a grupą kwasu karboksylowego (-COOH), utworzone przez eliminację cząsteczki wody (HdwaO) (Futura-Sciences ,, S.F.).
Strukturę octanu etylu przedstawiono na rysunku 1. Wiązanie estrowe jest tym pojedynczym wiązaniem, które tworzy się między tlenem kwasu karboksylowego i węglem etanolu.

R-COOH + R'-OH → R-COO-R '+ HdwaLUB
Na rysunku część niebieska odpowiada części związku pochodzącej z etanolu, a część żółta odpowiada kwasowi octowemu. Wiązanie estrowe zaznaczono w czerwonym kółku.
Indeks artykułów
- 1 Hydroliza wiązania estrowego
- 2 Rodzaje estrów
- 2.1 Ester węglanowy
- 2.2 Ester fosforowy
- 2.3 Ester siarkowy
- 3 Odnośniki
Hydroliza wiązania estrowego
Aby lepiej zrozumieć naturę wiązań estrowych, wyjaśniono mechanizm reakcji hydrolizy tych związków. Wiązanie estrowe jest stosunkowo słabe. W środowisku kwaśnym lub zasadowym hydrolizuje do odpowiednio alkoholu i kwasu karboksylowego. Mechanizm reakcji hydrolizy estrów jest dobrze poznany.
W podstawowym medium, nukleofilowe wodorotlenki najpierw atakują elektrofilowy C estru C = O, przerywając wiązanie π i tworząc tetraedryczny związek pośredni.
Następnie związek pośredni rozpada się, przekształcając C = O, powodując utratę grupy opuszczającej, alkoholanu, RO-, co prowadzi do kwasu karboksylowego..
Wreszcie reakcja kwas / zasada jest bardzo szybką równowagą, w której alkoholan RO- działa jako zasada deprotonująca kwas karboksylowy, RCO2H (traktowanie kwasem pozwoliłoby na otrzymanie kwasu karboksylowego z reakcji).

Mechanizm hydrolizy wiązania estrowego w środowisku kwaśnym jest nieco bardziej skomplikowany. Najpierw zachodzi reakcja kwasowo-zasadowa, ponieważ masz tylko słabego nukleofila i słabego elektrofilu, musisz aktywować ester.
Protonowanie estru karbonylowego czyni go bardziej elektrofilowym. W drugim etapie tlen w wodzie działa jako nukleofil, atakując elektrofilowe C w C = O, z elektronami poruszającymi się w kierunku jonu hydroniowego, tworząc tetraedryczny związek pośredni..
W trzecim etapie zachodzi reakcja kwas / zasada, odbezpieczająca tlen pochodzący z cząsteczki wody w celu zneutralizowania ładunku..
W czwartym etapie zachodzi kolejna reakcja kwasowo-zasadowa. Musisz wydobyć -OCH3, ale musisz uczynić z niej dobrą grupę opuszczającą przez protonowanie.
Na piątym etapie wykorzystują elektrony z sąsiedniego tlenu, aby pomóc „wypchnąć” grupę opuszczającą, tworząc neutralną cząsteczkę alkoholu..
W ostatnim etapie zachodzi reakcja kwasowo-zasadowa. Deprotonowanie jonu hydroniowego ujawnia karbonyl C = O w produkcie kwasu karboksylowego i regeneruje kwasowy katalizator (Dr Ian Hunt, S.F.).
Rodzaje estrów
Ester węglanowy
Estry węglanowe są najpowszechniejszymi tego typu związkami. Pierwszym estrem kwasu węglowego był octan etylu lub nazywany także etanianem etylu. Dawniej związek ten był znany jako eter octu, którego nazwa w języku niemieckim to Essig-Ęther, którego skrócenie pochodzi od nazwy tego typu związku.
Estry występują w przyrodzie i są szeroko stosowane w przemyśle. Wiele estrów ma charakterystyczny zapach owoców, a wiele z nich występuje naturalnie w olejkach eterycznych roślin. Doprowadziło to również do jego powszechnego stosowania w sztucznych zapachach i zapachach, gdy próbuje się naśladować zapachy..
Kilogram miliardów kilogramów poliestrów jest produkowanych w przemyśle rocznie, są to ważne produkty; tereftalan polietylenu, estry akrylanowe i octan celulozy.
Wiązanie estrowe estrów karboksylowych jest odpowiedzialne za tworzenie trójglicerydów w organizmach żywych.
Triglicerydy znajdują się we wszystkich komórkach, ale głównie w tkance tłuszczowej, stanowią główną rezerwę energii, jaką posiada organizm. Triacyloglicerydy (TAG) to cząsteczki glicerolu połączone wiązaniem estrowym z trzema kwasami tłuszczowymi. Kwasy tłuszczowe obecne w TAG są głównie nasycone (Wilkosz, 2013).
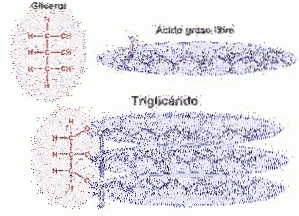
Triacyloglicerydy (trójglicerydy) są syntetyzowane praktycznie we wszystkich komórkach. Głównymi tkankami do syntezy TAG są jelito cienkie, wątroba i adipocyty. Z wyjątkiem jelita i adipocytów synteza TAG rozpoczyna się od glicerolu.
Glicerol jest najpierw fosforylowany kinazą glicerolową, a następnie aktywowane kwasy tłuszczowe (tłuszczowe acylo-CoA) służą jako substraty do dodawania kwasów tłuszczowych wytwarzających kwas fosfatydowy. Grupa fosforanowa jest usuwana i dodawany jest ostatni kwas tłuszczowy.
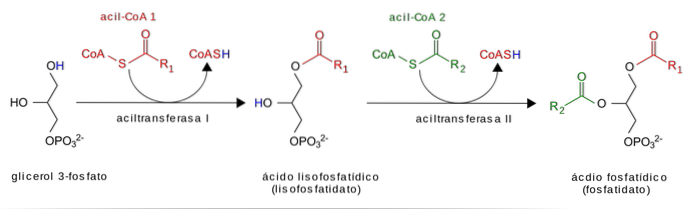
W jelicie cienkim dietetyczne TAG ulegają hydrolizie w celu uwolnienia kwasów tłuszczowych i monoacyloglicerydów (MAG) przed wchłonięciem przez enterocyty. Enterocytów MAG służą jako substraty do acylacji w dwuetapowym procesie, w którym powstaje TAG.
W tkance tłuszczowej nie ma ekspresji kinazy glicerolowej, więc budulcem TAG w tej tkance jest glikolityczny związek pośredni, fosforan dihydroksyacetonu, DHAP.
DHAP jest redukowany do glicerolo-3-fosforanu przez cytozolową dehydrogenazę glicerolo-3-fosforanu, a reakcja syntezy pozostałych TAG jest taka sama jak w przypadku wszystkich innych tkanek.
Ester fosforowy
Estry fosforowe są wytwarzane przez tworzenie wiązania estrowego między alkoholem a kwasem fosforowym. Biorąc pod uwagę strukturę kwasu, te estry mogą być mono-, di- i tripodstawione.
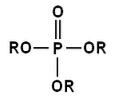
Te typy wiązań estrowych znajdują się w związkach, takich jak fosfolipidy, ATP, DNA i RNA..
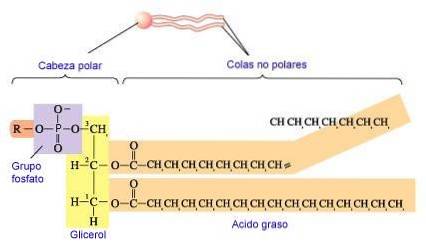
Fosfolipidy są syntetyzowane przez tworzenie wiązania estrowego między alkoholem a fosforanem kwasu fosfatydowego (3-fosforan 1,2-diacyloglicerolu). Większość fosfolipidów ma nasycony kwas tłuszczowy na C-1 i nienasycony kwas tłuszczowy na C-2 szkieletu glicerolu.
Najczęściej dodawane alkohole (seryna, etanoloamina i cholina) również zawierają azot, który może być naładowany dodatnio, podczas gdy glicerol i inozytol tego nie robią (King, 2017).
Trifosforan adenozyny (ATP) jest cząsteczką używaną jako waluta energetyczna w komórce. Ta cząsteczka składa się z cząsteczki adeniny połączonej z cząsteczką rybozy trzema grupami fosforanowymi (rysunek 8).
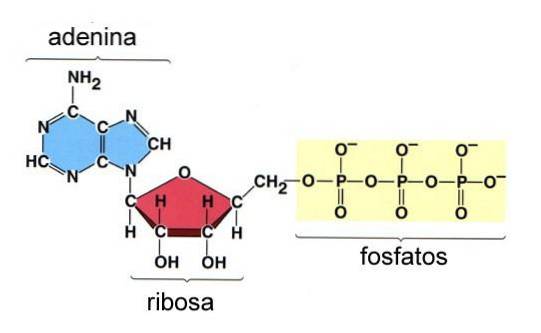
Trzy grupy fosforanowe cząsteczki nazywane są gamma (γ), beta (β) i Alpha (α), przy czym ta ostatnia estryfikuje grupę hydroksylową C-5 rybozy.
Wiązanie między rybozą a grupą α-fosforylową jest wiązaniem fosfoestrowym, ponieważ zawiera atom węgla i atom fosforu, podczas gdy grupy β- i γ-fosforylowe w ATP są połączone wiązaniami bezwodnikowymi, które nie obejmują atomów węgla..
Wszystkie fosfoanhydro mają znaczną chemiczną energię potencjalną, a ATP nie jest wyjątkiem. Ta potencjalna energia może być wykorzystana bezpośrednio w reakcjach biochemicznych (ATP, 2011).
Wiązanie fosfodiestrowe to wiązanie kowalencyjne, w którym grupa fosforanowa jest przyłączona do sąsiednich atomów węgla poprzez wiązania estrowe. Wiązanie jest wynikiem reakcji kondensacji między grupą hydroksylową dwóch grup cukrowych i grupą fosforanową.
Wiązanie diestrowe między kwasem fosforowym i dwiema cząsteczkami cukru w DNA i szkieletowym RNA łączy ze sobą dwa nukleotydy, tworząc polimery oligonukleotydowe. Wiązanie fosfodiestrowe łączy węgiel 3 'z węglem 5' w DNA i RNA.
(podstawa1) - (ryboza) -OH + HO-P (O) 2-O- (ryboza) - (podstawa 2)
(podstawa1) - (ryboza) - O - P (O) 2 - O- (ryboza) - (podstawa 2) + HdwaLUB
Podczas reakcji dwóch grup hydroksylowych w kwasie fosforowym z grupą hydroksylową w dwóch innych cząsteczkach powstają dwa wiązania estrowe w grupie fosfodiestrowej. Reakcja kondensacji, w której traci się cząsteczkę wody, generuje każde wiązanie estrowe.
Podczas polimeryzacji nukleotydów w celu utworzenia kwasów nukleinowych, grupa hydroksylowa grupy fosforanowej przyłącza się do węgla 3 'cukru jednego nukleotydu, tworząc wiązanie estrowe z fosforanem innego nukleotydu.
Reakcja tworzy wiązanie fosfodiestrowe i usuwa cząsteczkę wody (tworzenie wiązań fosfodiestrowych, S.F.).
Ester siarkowy
Estry lub tioestry kwasu siarkowego to związki z grupą funkcyjną R-S-CO-R '. Są produktem estryfikacji między kwasem karboksylowym a tiolem lub kwasem siarkowym (Block, 2016).
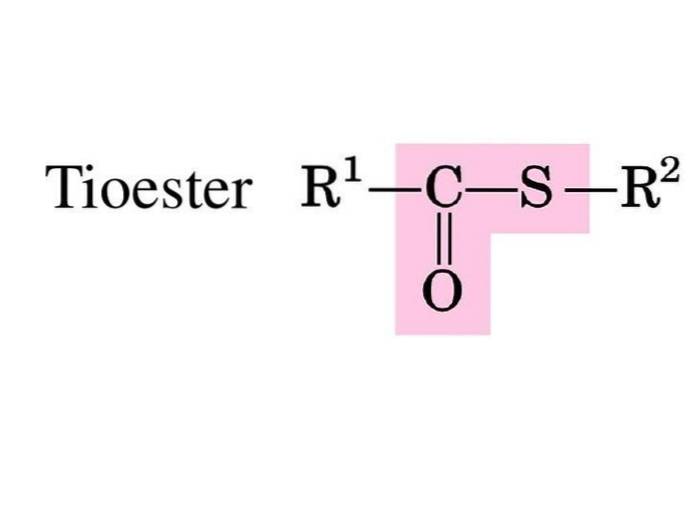
W biochemii najbardziej znanymi tioestrami są pochodne koenzymu A, np. Acetylo-CoA.
Acetylokoenzym A lub acetylo-CoA (ryc. 8) to cząsteczka biorąca udział w wielu reakcjach biochemicznych. Jest centralną cząsteczką w metabolizmie lipidów, białek i węglowodanów.
Jego główną funkcją jest dostarczanie grupy acetylowej do cyklu kwasu cytrynowego (cykl Krebsa) w celu utlenienia w celu produkcji energii. Jest również cząsteczką prekursorową do syntezy kwasów tłuszczowych i jest produktem degradacji niektórych aminokwasów.
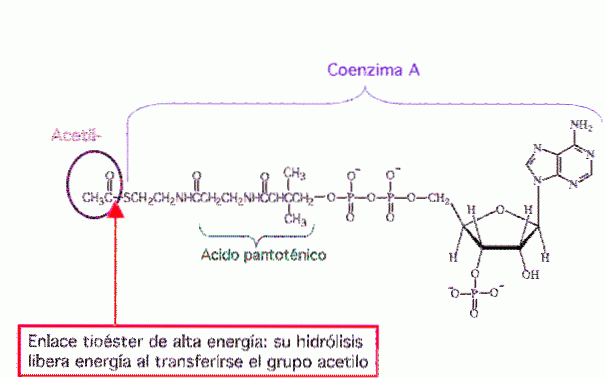
Wymienione powyżej kwasy tłuszczowe aktywowane przez CoA są innymi przykładami tioestrów pochodzących z komórki mięśniowej. Utlenianie tioestrów kwasów tłuszczowych-CoA faktycznie zachodzi w oddzielnych ciałach pęcherzykowych zwanych mitochondriami (Thompson, 2015).
Bibliografia
- ATP. (2011, 10 sierpnia). Odzyskany z learnbiochemistry.wordpress: learnbiochemistry.wordpress.com.
- Block, E. (22 kwietnia 2016). Związek siarki organicznej. Pobrane z britannica: britannica.com.
- Ian Hunt. (S.F.). Hydroliza estrów. Odzyskany z chem.ucalgary.ca: chem.ucalgary.ca.
- Futura-Sciences,. (S.F.). Wiązanie estrowe. Odzyskany z futura-sciences.us.
- King, M. W. (16 marca 2017). Kwasy tłuszczowe, trójglicerydy i fosfolipid synteza i metabolizm. Odzyskany z themedicalbiochemistrypage.org.
- tworzenie wiązań fosfodiestrowych. (S.F.). Odzyskany z biosyn: biosyn.com.
- Thompson, T. E. (19 sierpnia 2015). Lipid. Odzyskany z britannica: britannica.com.
- Wilkosz, R. (6 listopada 2013). Tworzenie wiązań estrowych w syntezie lipidów. Odzyskany z wisc-online.com.


Jeszcze bez komentarzy