
Erytroblasty, czym one są, erytropoeza, powiązane patologie
Plik erytroblasty są komórkami prekursorowymi erytrocytów kręgowców. Spadek stężenia tlenu w tkankach będzie sprzyjał zdarzeniom różnicowania komórkowego w tych komórkach, które doprowadzą do powstania dojrzałych erytrocytów. Zbiór wszystkich tych zdarzeń nazywany jest erytropoezą.
Podczas erytropoezy wzrasta synteza hemoglobiny. Obfite białko w erytrocytach, które pośredniczy w dostarczaniu tlenu do tkanek i detoksykacji dwutlenku węgla z tkanek, toksycznego dla komórek produktu odpadowego oddychania komórkowego.
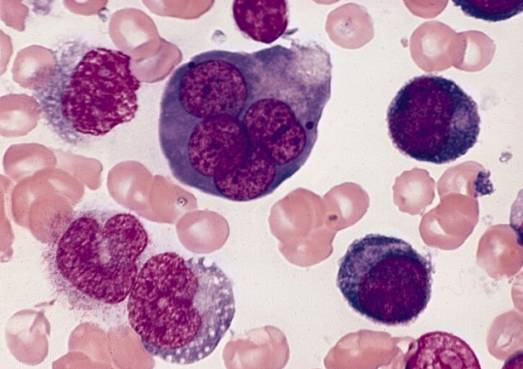
Błędy w procesie różnicowania erytroblastów powodują szereg patologii krwi, które razem nazywane są anemiami megaloblastycznymi.
Indeks artykułów
- 1 Czym są erytrocyty?
- 2 Czym są erytroblasty?
- 3 Czym jest erytropoeza?
- 4 Różnicowanie erytroblastów w erytrocyty
- 5 Różnicowanie komórek
- 6 Patologie związane z błędami w różnicowaniu erytroblastów
- 7 Referencje
Co to są erytrocyty?
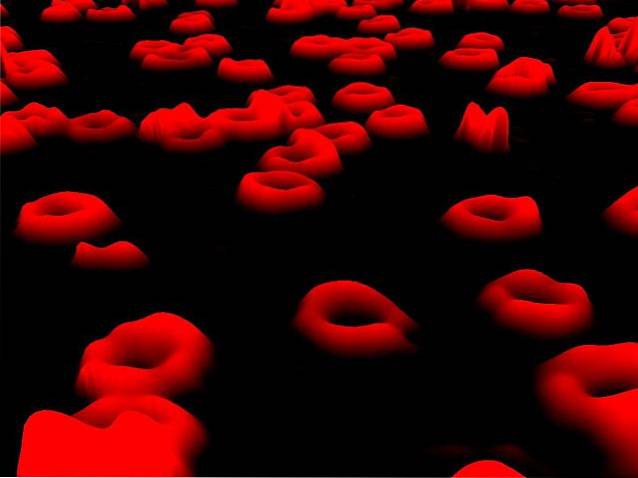
Mają charakterystyczną morfologię podobną do dwuwklęsłych dysków, a ich główną funkcją jest transport tlenu (O2) do różnych tkanek organizmu, jednocześnie odtruwając je z dwutlenku węgla (CO2) wytwarzanego podczas procesów komórkowych oddychanie..
Ta wymiana CO2 na O2 jest możliwa, ponieważ komórki te zawierają duże ilości charakterystycznego czerwonego białka zwanego hemoglobiną, zdolnego do interakcji z obydwoma rodzajami chemicznymi poprzez grupę hemową obecną w ich strukturze..
Osobliwością tych komórek u ssaków w stosunku do pozostałych kręgowców jest brak jądra komórkowego i organelli cytoplazmatycznych. Jednak w początkowych fazach produkcji we wczesnych stadiach rozwoju embrionalnego zaobserwowano, że prekursory komórkowe, z których pochodzą, stanowią przejściowe jądro.
To ostatnie nie jest zaskakujące, biorąc pod uwagę, że wczesne etapy rozwoju zarodka są zwykle podobne u wszystkich kręgowców, różniąc się tylko etapami, które utrudniają większe zróżnicowanie..
Co to są erytroblasty?
Erytroblasty to komórki, które dadzą początek dojrzałym erytrocytom po przejściu kolejnych zdarzeń różnicowania komórek..
Te komórki prekursorowe pochodzą od wspólnego progenitora szpiku kostnego kręgowców jako komórki jądrzaste, zaopatrzone w jądra i organelle komórkowe..
Zmiany w zawartości jego cytoplazmy oraz w przegrupowaniu cytoszkieletu zakończą się wytworzeniem gotowych do krążenia erytrocytów. Zmiany te odpowiadają na bodźce środowiskowe wskazujące na spadek tlenu w tkankach, a tym samym zapotrzebowanie na produkcję erytrocytów..
Co to jest erytropoeza?
Erytropoeza to termin używany do określenia procesu, w którym zachodzi produkcja i rozwój czerwonych krwinek, niezbędnych do utrzymania dopływu tlenu do różnych narządów i tkanek..
Proces ten jest precyzyjnie regulowany przez działanie erytropoetyny (EPO), hormonu syntezy nerek, który z kolei jest modulowany przez stężenie tlenu dostępnego w tkankach..
Niskie stężenia tlenu w tkankach indukują syntezę EPO przez czynnik transkrypcyjny indukowany przez hipoksję (HIF-1), który stymuluje proliferację erytrocytów poprzez wiązanie się z receptorami EpoR obecnymi na komórkach prekursorowych erytrocytów.
U ssaków erytropoeza przebiega w dwóch etapach, zwanych erytropoezą pierwotną i erytropoezą ostateczną..
Pierwsza występuje w woreczku żółtkowym podczas rozwoju embrionalnego, powodując powstanie dużych erytroblastów jądrzastych, podczas gdy druga występuje w wątrobie płodu i trwa w szpiku kostnym po drugim miesiącu ciąży, wytwarzając mniejsze erytrocyty wyłuszczone..
Inne białka, takie jak antypoptotyczna cytokina Bcl-X, której transkrypcja jest regulowana przez czynnik transkrypcyjny GATA-1, również wpływają pozytywnie na proces erytropoezy. Ponadto niezbędne są również podaż żelaza, witaminy B12 i kwasu foliowego.
Różnicowanie erytroblastów do erytrocytów
W procesie ostatecznej erytropoezy erytrocyty powstają w szpiku kostnym z niezróżnicowanej komórki progenitorowej lub wspólnego progenitora szpikowego zdolnego do zapoczątkowania innych komórek, takich jak granulocyty, monocyty i płytki krwi..
Ta komórka musi otrzymać odpowiednie sygnały zewnątrzkomórkowe, aby zagrozić jej różnicowaniu w kierunku linii erytroidalnej..
Po osiągnięciu tego zobowiązania rozpoczyna się sekwencja zdarzeń różnicowania, która rozpoczyna się od utworzenia pronormoblastu, znanego również jako proerytroblast. Duża komórka prekursorowa erytroblastów z jądrem.
Następnie proerytroblast będzie doświadczał stopniowego spadku objętości komórek jądrowych, któremu będzie towarzyszył wzrost syntezy hemoglobiny. Wszystkie te zmiany zachodzą powoli, gdy ta komórka przechodzi przez różne stadia komórkowe: zasadofilny erytroblast lub normoblast, polichromatyczny erytroblast i ortochromatyczny erytroblast.
Proces kończy się całkowitą utratą jądra, a także organelli obecnych w erytroblastach ortochromatycznych, które zapoczątkowały dojrzały erytrocyt.
Aby w końcu to osiągnąć, ta ostatnia musi przejść przez etap retikulocytów, wyłuszczoną komórkę, która nadal zawiera organelle i rybosomy w swojej cytoplazmie. Całkowite usunięcie jądra i organelli odbywa się przez egzocytozę.
Dojrzałe erytrocyty opuszczają szpik kostny do krwiobiegu, gdzie krążą przez około 120 dni, zanim zostaną pochłonięte przez makrofagi. Dlatego erytropoeza jest procesem, który zachodzi nieprzerwanie przez całe życie organizmu..
Różnicowanie komórek
W miarę postępów erytroblastów w kierunku całkowitego różnicowania do dojrzałych erytrocytów, ulegają one licznym zmianom w swoim cytoszkielecie, a także w ekspresji białek adhezyjnych komórek..
Mikrofilamenty aktyny ulegają depolimeryzacji i powstaje nowy cytoszkielet oparty na spektrynie. Spectrin to obwodowe białko błonowe zlokalizowane na powierzchni cytoplazmatycznej, które oddziałuje z ankiryną, białkiem, które pośredniczy w wiązaniu cytoszkieletu z transbłonowym białkiem pasma 3.
Te zmiany w cytoszkieletu oraz w ekspresji receptorów Epo, a także w mechanizmach, które je modulują, mają kluczowe znaczenie dla dojrzewania erytrocytów..
Wynika to z faktu, że pośredniczą w ustanowieniu interakcji między erytroblastami a komórkami obecnymi w mikrośrodowisku szpiku kostnego, ułatwiając przekazywanie sygnałów niezbędnych do rozpoczęcia i zakończenia różnicowania..
Po zakończeniu różnicowania zachodzą nowe zmiany, które sprzyjają utracie adhezji komórek do szpiku i ich uwolnieniu do krwiobiegu, gdzie będą spełniać swoją funkcję..
Patologie związane z błędami w różnicowaniu erytroblastów
Błędy podczas różnicowania erytroblastów w szpiku kostnym powodują pojawienie się patologii krwi, takich jak anemie megaloblastyczne. Wynikają one z niedoborów witaminy B12 i folianów niezbędnych do promowania różnicowania erytroblastów..
Termin megaloblastyczny odnosi się do dużych rozmiarów, które erytroblasty, a nawet erytrocyty osiągają jako produkt nieskutecznej erytropoezy charakteryzującej się wadliwą syntezą DNA.
Bibliografia
- Ferreira R, Ohneda K, Yamamoto M, Philipsen S.GATA1 function, a paradigm for transkrypcji factor in hematopoiesis. Biologia molekularna i komórkowa. 2005; 25 (4): 1215-1227.
- Kingsley PD, Malik J, Fantauzzo KA, Palis J. Prymitywne erytroblasty pochodzące z worka żółtkowego wyłuszczają się podczas embriogenezy ssaków. Blood (2004); 104 (1): 19–25.
- Konstantinidis DG, Pushkaran S, Johnson JF, Cancelas JA, Manganaris S, Harris CE, Williams AE, Zheng Y, Kalfa TA. Wymagania sygnalizacyjne i cytoszkieletowe w wyłuszczeniu erytroblastów. Krew. (2012); 119 (25): 6118–6127.
- Migliaccio AR. Enukleacja erytroblastów. Haematologica. 2010; 95: 1985-1988.
- Shivani Soni, Shashi Bala, Babette Gwynn, Kenneth E, Luanne L, Manjit Hanspal. Brak białka erytroblastów makrofagów (Emp) prowadzi do niepowodzenia ekstruzji jądrowej erytroblastów. Dziennik chemii biologicznej. 2006; 281 (29): 20181-20189.
- Skutelsky E, Danon D. Mikroskopowe badanie elektronowe eliminacji jądrowej z późnego erytroblastu. J Celi Biol, 1967; 33 (3): 625–635.
- Tordjman R, Delaire S, Plouet J, Ting S, Gaulard P, Fichelson S, Romeo P, Lemarchandel V. Erytroblasty są źródłem czynników angiogennych. Blood (2001); 97 (7): 1968-1974.


Jeszcze bez komentarzy