
Struktura wodorotlenku miedzi (II), właściwości, nazewnictwo, zastosowania

Plik wodorotlenek miedzi (II) o Wodorotlenek miedziowy to bladoniebieskie lub niebiesko-zielone krystaliczne nieorganiczne ciało stałe o wzorze chemicznym Cu (OH)dwa. Otrzymuje się go w postaci obszernego niebieskiego osadu poprzez dodanie wodorotlenku alkalicznego do roztworów miedzi (oznacza to, że zawierają jony Cudwa+). Jest to związek niestabilny.
Aby zwiększyć jego stabilność, przygotowywany jest w obecności amoniaku (NH3) lub fosforany Jeśli jest przygotowywany w obecności amoniaku, powstaje materiał o dobrej stabilności i dużej wielkości cząstek.

Po przygotowaniu z fosforanu miedzi (II), Cu3(PO4)dwa, Otrzymuje się materiał o drobniejszym rozmiarze cząstek i większej powierzchni. Wodorotlenek miedziowy jest szeroko stosowany jako środek grzybobójczy i bakteriobójczy w rolnictwie oraz do obróbki drewna, przedłużając jego żywotność..
Jest również stosowany jako suplement diety dla zwierząt. Jest stosowany jako surowiec do otrzymywania innych soli miedzi (II) oraz w galwanotechnice do powlekania powierzchni.
Trwają badania mające na celu oszacowanie jego potencjału w zwalczaniu infekcji bakteryjnych i grzybiczych u ludzi..
Indeks artykułów
- 1 Struktura
- 2 Nazewnictwo
- 3 Właściwości
- 3.1 Stan fizyczny
- 3.2 Masa cząsteczkowa
- 3.3 Temperatura topnienia
- 3.4 Gęstość
- 3.5 Rozpuszczalność
- 3.6 Inne właściwości
- 4 Zastosowania
- 4.1 W rolnictwie
- 4.2 W konserwacji drewna
- 4.3 W produkcji sztucznego jedwabiu
- 4.4 W przemyśle paszowym
- 4.5 Przy produkcji innych związków miedzi (II)
- 4.6 Inne zastosowania
- 4.7 Przyszłe zastosowania medyczne
- 5 Referencje
Struktura
Wodorotlenek miedzi (II) zawiera nieskończone łańcuchy jonów miedzi (Cudwa+) połączone mostkami grup hydroksylowych (OH-).
Łańcuchy są tak upakowane, że 2 atomy tlenu z innych łańcuchów znajdują się powyżej i poniżej każdego atomu miedzi, przyjmując w ten sposób zniekształconą konfigurację oktaedryczną, która jest powszechna w większości związków miedzi (II)..
W swojej strukturze cztery atomy tlenu znajdują się w odległości 1,93 A; dwa atomy tlenu mają wartość 2,63 A; a odległość Cu-Cu wynosi 2,95 A..
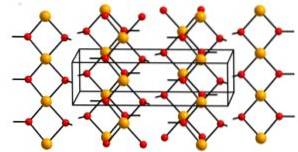
Nomenklatura
- Wodorotlenek miedzi (II).
- Wodorotlenek miedziowy.
- Diwodorotlenek miedzi.
Nieruchomości
Stan fizyczny
Krystaliczne ciało stałe.
Waga molekularna
99,58 g / mol.
Temperatura topnienia
Rozkłada się przed stopieniem. Temperatura rozkładu 229 ºC.
Gęstość
3,37 g / cm3
Rozpuszczalność
Jest praktycznie nierozpuszczalny w wodzie: 2,9 mikrograma / lw temperaturze 25ºC. Szybko rozpuszczalny w kwasach, stężonych roztworach zasad i wodorotlenku amonu. Nierozpuszczalny w rozpuszczalnikach organicznych. W gorącej wodzie rozkłada się tworząc tlenek miedzi (II), który jest bardziej stabilny.
Inne właściwości
Jest łatwo rozpuszczalny w mocnych kwasach, a także w stężonych roztworach wodorotlenków alkalicznych, dając ciemnoniebieskie aniony, prawdopodobnie [Cun(O)2n + 2]dwa-.
Jego stabilność zależy od metody przygotowania.
Może się rozkładać, dając czarny tlenek miedzi (II) (CuO), jeśli pozostaje w spoczynku przez kilka dni lub w trakcie ogrzewania.
W obecności nadmiaru alkaliów rozkłada się powyżej 50 ºC.
Aplikacje
W rolnictwie
Wodorotlenek miedzi (II) ma szerokie zastosowanie jako środek grzybobójczy i przeciwbakteryjny w uprawach rolniczych. Oto kilka przykładów:
- Działa przeciw plamom bakteryjnym (np Erwinia) na sałacie, jako zabieg na liście.
- Przeciw plamom bakteryjnym (np Xanthomonas pruni) w brzoskwiniach, w przypadku których stosuje się kurację usypiającą i dolistną.
- Stosuje się go przeciwko szkodnikom liści i łodyg borówek amerykańskich poprzez stosowanie utajone.
- Przed gniciem podczas przechowywania borówki spowodowanej przez Monilinia oxycocci, przez ukrytą aplikację.
Do zastosowań w rolnictwie stosuje się wodorotlenek miedzi (II), który jest przygotowywany w obecności fosforanów ze względu na mały rozmiar cząstek..

W konserwacji drewna
Drewno z natury organiczne jest wrażliwe na atak owadów i mikroorganizmów. Wodorotlenek miedzi (II) jest stosowany jako biocyd przeciwko grzybom atakującym drewno.
Zwykle jest stosowany w połączeniu z czwartorzędowym związkiem amoniowym (NH4+). Wodorotlenek miedzi działa jako środek grzybobójczy, a czwartorzędowy związek amoniowy działa jako środek owadobójczy..
W ten sposób impregnowane drewno wytrzymuje lub stawia opór warunkom użytkowania, osiągając poziom wydajności wymagany przez użytkownika. Jednak drewno impregnowane tymi związkami ma wysoką zawartość miedzi i jest bardzo korozyjne dla zwykłej stali, dlatego wymagany jest rodzaj stali nierdzewnej, który może wytrzymać obróbkę drewna poddanego obróbce..
Pomimo swojej przydatności wodorotlenek miedzi (II) jest uważany za lekko niebezpieczny biocyd.
Z tego powodu istnieje obawa, że będzie on uwalniany z impregnowanego drewna do środowiska w ilościach, które mogą być szkodliwe dla mikroorganizmów naturalnie występujących w wodach (rzekach, jeziorach, mokradłach i morzu) lub w glebie..
W produkcji sztucznego jedwabiu
Od XIX wieku do rozpuszczania celulozy stosuje się amoniakalne roztwory wodorotlenku miedzi (II). To jeden z pierwszych kroków w celu uzyskania włókna zwanego sztucznym jedwabiem przy użyciu technologii opracowanej przez firmę Bemberg w Niemczech..
Wodorotlenek miedzi (II) rozpuszcza się w roztworze amoniaku (NH3), tworząc złożoną sól.
Rafinowane krótkie włókna bawełniane dodaje się do roztworu amoniaku miedzi zawierającego wodorotlenek miedzi (II) w postaci wytrąconej substancji stałej..
Bawełniana celuloza tworzy kompleks z wodorotlenkiem tetraamonu miedzi rozpuszczonym w roztworze.
Roztwór ten jest następnie koagulowany podczas przepuszczania przez urządzenie do wytłaczania..
Ze względu na wysoki koszt technologia ta została już przewyższona wiskozą. Technologia Bemberg jest obecnie stosowana tylko w Japonii.
W przemyśle paszowym
Jest stosowany jako śladowe ilości w paszach dla zwierząt, ponieważ jest jedną z substancji wymaganych jako mikroelementy do pełnego żywienia zwierząt.

Dzieje się tak, ponieważ u wyższych istot żyjących miedź jest pierwiastkiem niezbędnym do działania różnych enzymów zawierających miedź..
Np. Zawarty jest w enzymie uczestniczącym w produkcji kolagenu oraz w enzymie niezbędnym do syntezy melaniny m.in..
Jest to związek powszechnie uznawany za bezpieczny, gdy dodaje się go w ilościach zgodnych z dobrą praktyką żywieniową..

Przy produkcji innych związków miedzi (II)
Aktywny prekursor w produkcji następujących związków miedzi (II): naftenian miedzi (II), 2-etyloheksanian miedzi (II) oraz mydła miedziane. W takich przypadkach stosuje się wodorotlenek miedzi (II), który jest syntetyzowany w obecności amoniaku..
Inne zastosowania
Służy do stabilizacji nylonu, w elektrodach akumulatorowych; jako utrwalacz koloru w operacjach barwienia; jako pigment; w środkach owadobójczych; w obróbce i barwieniu papieru; w katalizatorach jako katalizator w wulkanizacji kauczuku polisiarczkowego; jako pigment przeciwporostowy; oraz w elektrolizie, w galwanizacji.
Przyszłe zastosowania medyczne
Wodorotlenek miedzi (II) jest częścią związków miedzi, które są badane w postaci nanocząstek w celu eliminacji bakterii, takich jak E coli, K. pneumoniae, P. aeruginosa, Salmonella spp., między innymi powodując choroby u ludzi.
Stwierdzono również, że nanocząsteczki miedzi mogą być skuteczne przeciwko Candida albicans, grzyb, który jest częstą przyczyną patologii człowieka.
Wskazuje to, że nanotechnologia miedzi może odgrywać ważną rolę w zwalczaniu bakterii i grzybów wywołujących infekcje u ludzi, a wodorotlenek miedzi (II) może być bardzo przydatny w tych dziedzinach..
Bibliografia
- Cotton, F. Albert i Wilkinson, Geoffrey. (1980). Zaawansowana chemia nieorganiczna. Czwarta edycja. John Wiley & Sons.
- Kirk-Othmer (1994). Encyklopedia technologii chemicznej. Tom 7. Wydanie czwarte. John Wiley & Sons.
- Encyklopedia chemii przemysłowej Ullmanna. (1990). Piąta edycja. Tom A7. VCH Verlagsgesellschaft mbH.
- Bailar, J.C .; Emeléus, H.J.; Sir Ronald Nyholm i Trotman-Dickenson, A.F. (1973). Kompleksowa chemia nieorganiczna. Tom 3. Pergamon Press.
- National Library of Medicine. (2019). Hydroksyd miedzi (II). Odzyskany z: pubchem.ncbi.nlm.nih.gov
- Schiopu, N. i Tiruta-Barna, L. (2012). Środki do konserwacji drewna. W toksyczności materiałów budowlanych. Rozdział 6. Odzyskany z sciencedirect.com.
- Mordorski, B. i Friedman, A. (2017). Nanocząsteczki metali do infekcji bakteryjnych. W sfunkcjonalizowanych nanomateriałach do zarządzania infekcjami drobnoustrojami. Rozdział 4. Odzyskany z sciencedirect.com.
- Takashi Tsurumi. (1994). Rozwiązanie się kręci. W zaawansowanej technologii przędzenia włókien. Rozdział 3. Odzyskane z sciencedirect.com.



Jeszcze bez komentarzy