
Koncepcja sieci Bravais, charakterystyka, przykłady, ćwiczenia
Plik Siatki Bravais Są to zbiór czternastu trójwymiarowych komórek elementarnych, w których mogą znajdować się atomy kryształu. Komórki te składają się z trójwymiarowego układu punktów, które tworzą podstawową strukturę, która jest okresowo powtarzana w trzech kierunkach przestrzennych..
Pochodzenie tego określenia dla podstawowych struktur krystalicznych pochodzi z 1850 r., Kiedy Auguste Bravais wykazał, że istnieje tylko 14 możliwych trójwymiarowych podstawowych komórek elementarnych.

Zestaw 14 sieci Bravais jest podzielony na siedem grup lub struktur zgodnie z geometrią komórek, te siedem grup to:
1- sześcienny
2- Czworokątny
3- Rombowa
4- Trójkątne-sześciokątne
5- Jednoskośny
6- Triclinic
7- Trygonalny
Każda z tych struktur definiuje komórkę elementarną, będącą najmniejszą częścią, która zachowuje geometryczny układ atomów w krysztale..
Indeks artykułów
- 1 Charakterystyka sieci Bravais
- 1.1 Sieci sześcienne
- 2 Przykłady
- 2.1 - Żelazo
- 2.2 - Miedź
- 2.3 - Cenne klejnoty
- 2.4 Topaz
- 3 ćwiczenia rozwiązane
- 3.1 Ćwiczenie 1
- 3.2 Ćwiczenie 2
- 3.3 Ćwiczenie 3
- 4 Odnośniki
Charakterystyka sieci Bravais
Czternaście sieci Bravais, jak wspomniano powyżej, jest podzielonych na siedem grup. Ale każda z tych grup ma swoje komórki elementarne z charakterystycznymi parametrami, którymi są:
1- Parametr sieci (a, b, c)
2- Liczba atomów w komórce
3- Zależność między parametrem sieci a promieniem atomowym
4- Numer koordynacyjny
5- współczynnik pakowania
6- przestrzenie śródmiąższowe
7- Poprzez translacje wzdłuż wektorów a, b, c struktura kryształu jest powtarzana.
Sieci sześcienne
Składa się z prostej sześciennej lub sześciennej sieci P, sześciennej sieci centralnej lub sześciennej F i centrowanej sześciennej sieci lub sześciennej sieci I.
Wszystkie sieci sześcienne mają wszystkie trzy parametry sieciowe odpowiadające kierunkom x, y, z o tej samej wartości:
a = b = c
Sieć sześcienna P.
Należy zauważyć, że atomy są reprezentowane przez sfery, których środki znajdują się na wierzchołkach sześciennej komórki elementarnej P.
W przypadku sieci sześciennej P liczba atomów w komórce wynosi 1, ponieważ w każdym wierzchołku tylko jedna ósma atomu znajduje się w komórce elementarnej, więc 8 * ⅛ = 1.
Plik numer koordynacyjny wskazuje liczbę atomów, które są bliskimi sąsiadami w sieci krystalicznej. W przypadku sieci sześciennej P liczba koordynacyjna wynosi 6.
Sieć sześcienna I
W tego typu sieci oprócz atomów na wierzchołkach sześcianu w centrum sześcianu znajduje się atom. Więc liczba atomów na komórkę jednostka w sześciennej sieci P to 2 atomy.

Sieć sześcienna F
Jest to sieć sześcienna, w której oprócz atomów w wierzchołkach znajduje się atom w środku powierzchni każdego sześcianu. Plik liczba atomów w komórce wynosi 4, ponieważ każdy z sześciu atomów twarzy ma połowę wewnątrz komórki, to znaczy 6 * ½ = 3 plus 8 * ⅛ = 1 na wierzchołkach.

Siatka sześciokątna
W tym przypadku komórka elementarna jest prostym pryzmatem o sześciokątnej podstawie. Sieci sześciokątne mają wszystkie trzy parametry sieciowe odpowiadające spełniające następującą zależność:
a = b ≠ c
Kąt między wektorem a i b wynosi 120º, jak pokazano na rysunku. Podczas gdy między wektorami a i c, a także między b i c powstają kąty proste.

Plik liczba atomów w komórce zostanie obliczona w następujący sposób:
- W każdej z 2 podstaw sześciokątnego pryzmatu znajduje się 6 atomów na sześciu wierzchołkach. Każdy z tych atomów zajmuje ⅙ komórki elementarnej.
- W środku każdej z 2 sześciokątnych podstaw znajduje się 1 atom zajmujący 1/2 komórki elementarnej.
- Na 6 bocznych powierzchniach sześciokątnego graniastosłupa znajdują się 3 atomy, z których każdy zajmuje ⅔ komórki elementarnej, a po 3 atomy zajmują ⅓ objętości komórki elementarnej.
(6 x ⅙) x 2 + ½ x 2 + ⅔ x 3 + ⅓ x 3 = 6
Zależność między parametrami sieci a i b z promieniem atomowym R przy założeniu, że wszystkie atomy mają równy promień i są w kontakcie, jest następująca:
a / R = b / R = 2
Przykłady
Metale są głównymi przykładami struktur krystalicznych, a także najprostszymi, ponieważ zazwyczaj składają się tylko z jednego rodzaju atomu. Ale są też inne związki niemetaliczne, które również tworzą struktury krystaliczne, takie jak diament, kwarc i wiele innych..
- Żelazo
Żelazo ma pojedynczą sześcienną komórkę elementarną z parametrem sieci lub krawędzi a = 0,297 nm. W 1 mm znajduje się 3,48 x 10 ^ 6 ogniw jednostkowych.
- Miedź
Ma centralną sześcienną strukturę krystaliczną, składającą się wyłącznie z atomów miedzi..
- Kamienie szlachetne
Drogocenne klejnoty to krystaliczne struktury zasadniczo tego samego związku, ale z niewielkimi ilościami zanieczyszczeń, które często są odpowiedzialne za ich kolor..
Diament
Składa się wyłącznie z węgla i nie zawiera zanieczyszczeń, dlatego jest bezbarwny. Diament ma sześcienna struktura kryształu (izometryczny-heksoktaedryczny) i jest najtwardszym znanym materiałem.
Kwarc
Składa się z tlenku krzemionki, jest zazwyczaj bezbarwny lub biały. Jego krystaliczna struktura jest trygonalno-trapezoedryczna.
Rubin
Składa się z tlenku glinu z domieszkami chromu, które nadają mu charakterystyczny czerwony kolor. Formularz a sześciokątna sieć krystaliczna.
Szafir
To także kryształ tlenku glinu, ale z domieszką tytanu i żelaza, które odpowiadają za jego niebieski kolor w różnych odcieniach. Podobnie jak rubin struktura heksagonalna.
Jadeit
Kamień szlachetny ma zazwyczaj zielony kolor struktura jednoskośna i składa się z krzemianu żelazowo-magnezowo-wapniowego.
Topaz
Jest bezbarwny z struktura rombowa krzemian-wodorotlenek glinu.
Rozwiązane ćwiczenia
Ćwiczenie 1
Znajdź związek między parametrem sieciowym a promieniem atomowym dla sześciennej sieci F.
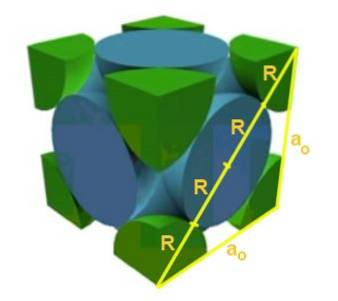
Rozwiązanie: Po pierwsze, zakłada się, że atomy są reprezentowane jako kule o promieniu R w „kontakcie” ze sobą, jak pokazano na rysunku. Tworzy się trójkąt prostokątny, w którym prawdą jest, że:
(4 R) ^ 2 = a ^ 2 + a ^ 2 = 2 a ^ 2
Dlatego zależność krawędź-promień jest następująca:
a / R = 4 / √2
Ćwiczenie 2
Znajdź związek między parametrem sieciowym a promieniem atomowym dla sześciennej sieci I (z centrum ciała).
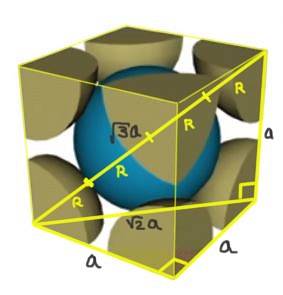
Rozwiązanie: Atomy mają być reprezentowane jako sfery o całym promieniu R w „kontakcie” ze sobą, jak pokazano na rysunku.
Powstają dwa trójkąty prostokątne, jeden z przeciwprostokątną √2a, a drugi z przeciwprostokątną √3a, co można udowodnić za pomocą twierdzenia Pitagorasa. Z tego wynika, że zależność między parametrem sieciowym a promieniem atomowym dla sześciennej sieci I (wyśrodkowanej w ciele) jest następująca:
a / R = 4 / √3
Ćwiczenie 3
Znajdź współczynnik upakowania F dla komórki elementarnej o strukturze sześciennej F (sześciennej centralnej), w której atomy mają promień R i są w „kontakcie”.
Rozwiązanie: Współczynnik upakowania F definiuje się jako iloraz objętości zajmowanej przez atomy w komórce elementarnej i objętości komórki:
F = Vatomy / Vkomórka
Jak wykazano powyżej, liczba atomów na komórkę elementarną w siatce sześciennej wyśrodkowanej na twarz wynosi 4, więc współczynnik upakowania będzie następujący:
F = 4 [4πR ^ 3/3] / [a ^ 3] =…
… 4 [4πR ^ 3/3] / [4R / √2] ^ 3 = (√2) π / 6 = 0,74
Bibliografia
- Centrum zasobów akademickich Crystal Structures. [PDF]. Pobrane 24 maja 2018 r. Z: web.iit.edu
- Kryształy. Pobrane 26 maja 2018 r.Z: thinkco.com
- Pressbooki. 10.6 Struktury kratowe w krystalicznych ciałach stałych. Pobrane 26 maja 2018 z: opentextbc.ca
- Ming. (30 czerwca 2015). Rodzaje struktur krystalicznych. Pobrane 26 maja 2018 z: crystalvisions-film.com
- Helmenstine, dr Anne Marie (31 stycznia 2018). Rodzaje
- Kittel Charles (2013) Fizyka ciała stałego, Fizyka materii skondensowanej (8. edycja). Wiley.
- KHI. (2007). Struktury krystaliczne. Pobrane 26 maja 2018 z: folk.ntnu.no
- Wikipedia. Kraty Bravais. Odzyskany z: en.wikipedia.com.



Jeszcze bez komentarzy