
Trójpolifosforan sodu (Na5P3O10) struktura, właściwości, zastosowanie, wpływ
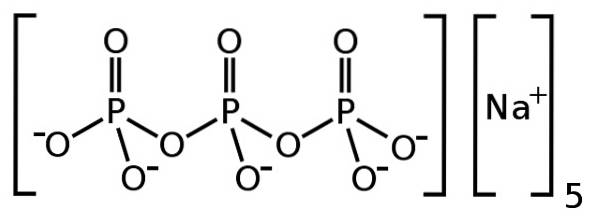
Plik tripolifosforan sodu jest nieorganicznym związkiem utworzonym przez pięć jonów sodu Na+ i jon tripolifosforanowy P.3LUB105-. Jego wzór chemiczny to Na5P.3LUB10. Jon tripolifosforanowy zawiera trzy połączone ze sobą jednostki fosforanowe i jest to tak zwany fosforan skondensowany.
Anion tripolifosforanowy P.3LUB105- ma zdolność zatrzymywania jonów, takich jak wapń Cadwa+ i magnezu Mgdwa+, Dlatego trójpolifosforan sodu jest stosowany jako środek pomocniczy w detergentach, aby lepiej działały w niektórych rodzajach wody..
Trójpolifosforan sodu znajduje również zastosowanie jako źródło fosforu w diecie zwierząt wypasanych oraz w leczeniu niektórych dolegliwości innych gatunków zwierząt. Służy również do zagęszczania i nadawania tekstury niektórym przetworzonym produktom, takim jak kremy, puddingi i sery..
W rolnictwie jest stosowany w nawozach granulowanych, aby zapobiec ich sklejaniu się i pozostawaniu luźnym..
Chociaż toczono dyskusje na temat wpływu tripolifosforanu sodu dodawanego do detergentów na środowisko, obecnie szacuje się, że nie przyczynia się on w znaczący sposób do niszczenia środowiska, przynajmniej poprzez detergenty..
Indeks artykułów
- 1 Struktura chemiczna
- 2 Nazewnictwo
- 3 Właściwości
- 3.1 Stan fizyczny
- 3.2 Masa cząsteczkowa
- 3.3 Temperatura topnienia
- 3.4 Gęstość
- 3.5 Rozpuszczalność
- 3,6 pH
- 3.7 Właściwości chemiczne
- 3.8 Inne właściwości
- 4 Otrzymywanie
- 5 zastosowań
- 5.1 W detergentach
- 5.2 Do użytku weterynaryjnego
- 5.3 W medycynie
- 5.4 W przemyśle spożywczym
- 5.5 Inne zastosowania
- 6 Wpływ na środowisko
- 7 Ryzyka
- 8 Odniesienia
Struktura chemiczna
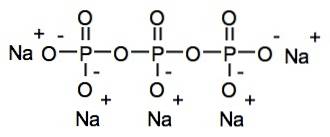
Trójpolifosforan sodu jest jednym z tak zwanych fosforanów skondensowanych, ponieważ składa się z kilku połączonych ze sobą jednostek fosforanowych. W tym przypadku jon tripolifosforanowy jest liniowym skondensowanym fosforanem, ponieważ ma liniową strukturę podobną do łańcucha, z wiązaniami fosfor-tlen-fosfor (P-O-P).
Nomenklatura
- Trójpolifosforan sodu
- Trifosforan sodu
- Trifosforan pentasodowy
- STPP (akronim od angielskiego Trójpolifosforan sodu)
Nieruchomości
Stan fizyczny
Bezbarwna do białej krystalicznej substancji stałej.
Waga molekularna
367,86 g / mol.
Temperatura topnienia
622 ° C.
Gęstość
2,52 g / cm3
Rozpuszczalność
Rozpuszczalny w wodzie: 20 g / 100 ml w 25 ° C i 86,5 g / 100 ml w 100 ° C.
pH
1% roztwór tripolifosforanu sodu ma pH 9,7-9,8.
Właściwości chemiczne
Jest to środek wiążący jony, co oznacza, że może wychwytywać jony i pozostawać do nich przyczepiony. Tworzy kompleksy z wieloma metalami.
Jeśli roztwór tripolifosforanu sodu jest ogrzewany przez długi czas, ma on tendencję do przekształcania się w ortofosforan sodu.3PO4.
Inne właściwości
Jest lekko higroskopijny. Tworzy stabilne hydraty, czyli związki z przyłączonymi cząsteczkami wody (bez przereagowania z nią) o wzorze Na5P.3LUB10.nHdwaLub gdzie n może wynosić od 1 do 6.
Według niektórych źródeł, 20 mg tripolifosforanu sodu w jednym litrze wody nie wpływa na zapach, smak ani pH tej wody..
Otrzymywanie
Trójpolifosforan sodu jest przygotowywany przez odwodnienie ortofosforanów (takich jak fosforan monosodowy NaHdwaPO4 i fosforan disodu NadwaHPO4) w bardzo wysokich temperaturach (300-1200 ° C):
NaHdwaPO4 + 2 NadwaHPO4 → Na5P.3LUB10 + 2 godzdwaLUB
Można go również otrzymać poprzez kontrolowaną kalcynację (czyli ogrzewanie w bardzo wysokiej temperaturze) ortofosforanu sodu.3PO4 z węglanem sodu NadwaWSPÓŁ3 i kwas fosforowy H.3PO4.
Aplikacje
W detergentach
Trójpolifosforan sodu ma właściwość tworzenia związków z pewnymi jonami, zatrzymując je. Posiada również właściwości dyspergujące cząsteczki brudu i utrzymuje je w zawiesinie..
Z tego powodu jest szeroko stosowany w kompozycjach detergentów do wyłapywania i unieruchamiania jonów wapnia Ca.dwa+ i magnezu Mgdwa+ wody (tzw. woda twarda) oraz do zatrzymywania brudu zawieszonego w wodzie.
Wspomniane jony zakłócają działanie czyszczące. Wychwytując je, tripolifosforan zapobiega wytrącaniu się tych jonów wraz ze środkiem czyszczącym lub przywieraniu brudu do tkaniny, zapobiegając oderwaniu się plamy z niej..
W tym przypadku mówi się, że tripolifosforan sodu „zmiękcza” wodę. Z tego powodu jest stosowany w detergentach do prania i detergentach do automatycznych zmywarek do naczyń..
Ponieważ tworzy stabilne hydraty, detergenty, które mają go w swoim składzie, można natychmiast wysuszyć przez rozpylanie (bardzo drobny spray), tworząc suche proszki..

Do użytku weterynaryjnego
Trójpolifosforan sodu stosowany jest jako dodatek w roztworach płynnych jako źródło fosforu dla zwierząt gospodarskich.

Jest również stosowany w celu zapobiegania kamicy nerkowej u kotów, w przypadku którego podaje się go tym zwierzętom doustnie. Należy jednak zwrócić uwagę na dawkowanie, ponieważ może powodować biegunkę..

W medycynie
Trójpolifosforan sodu został wykorzystany do przygotowania nanocząstek do prawidłowego transportu i dostarczania leków stosowanych w chemioterapii raka. Był również stosowany w nanocząsteczkach do leczenia infekcji grzybiczych płuc..
W przemyśle spożywczym
Używany w produktach mlecznych, takich jak puddingi, bita śmietana, śmietana i sery.

W innych produktach spożywczych jest stosowany jako sekwestrant jonów, nadający teksturę, jako zagęszczacz i jako środek konserwujący.
Inne zastosowania
- Jako stabilizator nadtlenku
- W płuczkach wiertniczych działa jako emulgator i dyspergator do kontrolowania lepkości płuczki.
- W rolnictwie stosowany jest jako środek przeciwzbrylający do niektórych nawozów lub produktów rolnych, co oznacza, że zapobiega ich sklejaniu się, a nawóz można łatwo rozprowadzić. Jest również stosowany w formułach pestycydów stosowanych w uprawach roślin.

Wpływ środowiska
Stosowanie produktów fosforanowych zostało zidentyfikowane jako jeden z czynników przyczyniających się do eutrofizacji wody na naszej planecie.
Eutrofizacja to przesadny i przyspieszony wzrost glonów i gatunków roślin wodnych, który prowadzi do gwałtownego spadku dostępnego tlenu w wodzie, prowadząc do zniszczenia dotkniętego ekosystemu (śmierć większości gatunków zwierząt w nim).

W latach osiemdziesiątych XX wieku pojawiły się kontrowersje, że stosowanie tripolifosforanu sodu w detergentach przyczynia się do eutrofizacji.
Obecnie wiadomo, że ograniczenie stosowania detergentów zawierających tripolifosforan sodu w niewielkim stopniu przyczyniłoby się do wyeliminowania eutrofizacji, ponieważ fosforany pochodzą w większych ilościach z innych źródeł rolniczych i przemysłowych.
W rzeczywistości są kraje, które traktują tripolifosforan sodu jako przyjazny dla środowiska składnik detergentów i promują jego stosowanie.
Ryzyka
Trójpolifosforan sodu działa drażniąco na skórę i oczy. Kontakt z oczami może spowodować uszkodzenie oczu. Długotrwały kontakt ze skórą może powodować zapalenie skóry.
W przypadku spożycia w dużych ilościach może powodować nudności, wymioty i biegunkę, powodując również poważne obniżenie poziomu jonów wapnia we krwi. U zwierząt spowodował spadek poziomu wapnia w kościach.
Jest uważany za bezpieczny związek, o ile przestrzegane są standardy produkcyjne produktu, w którym jest stosowany..
Bibliografia
- Liu, Y. and Chen, J. (2014). Cykl fosforu. Moduł referencyjny w dziedzinie systemów Ziemi i nauk o środowisku. Encyklopedia ekologii (drugie wydanie). Vol. 4, 2014, s. 181–191. Odzyskany z sciencedirect.com
- NAS. National Library of Medicine. (2019). Trójpolifosforan sodu. Narodowe Centrum Informacji Biotechnologicznej. Odzyskany z pubchem.ncbi.nlm.nih.gov.
- Mukherjee, B. i in. (2017). Podawanie do płuc biodegradowalnych nanonośników leków w celu skuteczniejszego leczenia zakażeń grzybiczych w płucach: spostrzeżenia oparte na ostatnich ustaleniach. W wielofunkcyjnych systemach dostarczania łączonego, wykrywania biologicznego i diagnostyki. Odzyskany z sciencedirect.com.
- Kirk-Othmer. (1991). Encyklopedia technologii chemicznej. 4th Nowy Jork, John Wiley and Sons.
- Burckett St. Laurent, J. i in. (2007). Pranie i czyszczenie tekstyliów. W Podręczniku czyszczenia / odkażania powierzchni. Odzyskany z sciencedirect.com.
- Budavari, S. (redaktor). (tysiąc dziewięćset dziewięćdziesiąty szósty). Indeks Merck. NJ: Merck and Co., Inc.
- Salahuddin, N. i Galal, A. (2017). Poprawa dostarczania leków do chemioterapii dzięki narzędziom nanoprecyzyjnym. W nanostrukturach do terapii raka. Odzyskany z sciencedirect.com.


Jeszcze bez komentarzy